整理重要讲解第八讲晶体结构试题分类解析.docx
《整理重要讲解第八讲晶体结构试题分类解析.docx》由会员分享,可在线阅读,更多相关《整理重要讲解第八讲晶体结构试题分类解析.docx(14页珍藏版)》请在冰豆网上搜索。
整理重要讲解第八讲晶体结构试题分类解析
高考化学专题复习第八讲晶体结构试题分类解析
有关晶体结构的推断和计算是高中化学中的一个难点,这些题目能很好地考察学生的观察能力和三维想象能力,而且又很容易与数学、物理特别是立体几何知识相结合,自然也就成为近年高考的热点之一。
此类题目的解答,要求学生在熟练掌握NaCl、CsCl、CO2、SiO2、金刚石等晶体结构的基础上,进一步理解和掌握一些重要的分析方法与原则。
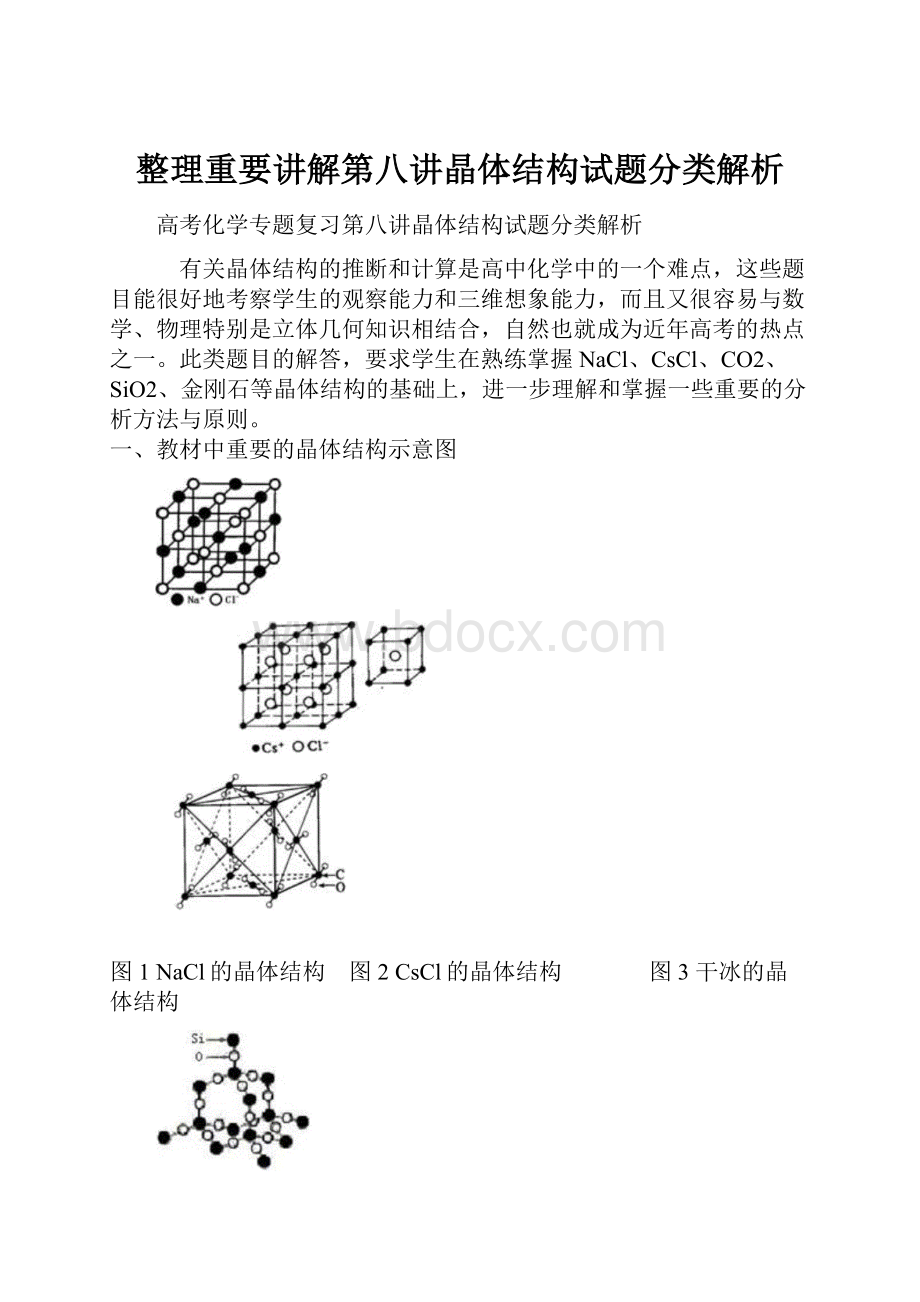
一、教材中重要的晶体结构示意图
图1NaCl的晶体结构 图2CsCl的晶体结构 图3干冰的晶体结构
图4SiO2的晶体结构图5金刚石的晶体结构图6石墨的晶体结构俯视图
练习图
1、请将上面练习图中NaCl晶体结构中代表Na+的圆圈涂黑(不考虑体积大小),以完成NaCl晶体的结构示意图。
在该晶体中每个Na+周围与之最接近且距离相等的Na+共有个;与每个Na+等距离且最近的Cl-所围成的空间几何构型为。
2、在CsCl晶体中,每个Cs+周围与之最接近的且距离相等的Cs+有个。
3、在干冰晶体中,每个CO2分子周围与之最接近的且距离相等的CO2分子有个。
4、在金刚石的网状结构中,含有由共价键形成的碳原子环,其中最小的环上有个碳原子,每个碳原子上的任意两个C—C键的夹角都是。
5、石墨是层状结构,每一层内,碳原子排列成而成平面网状结构。
每一个碳原子跟其它个碳原子相连。
二、根据晶体结构或晶胞结构示意图推断晶体的化学式
解答这类试题,通常采用分摊法。
因为在一个晶胞结构中出现的多个原子,并不是只为这一个晶胞所独立占有,而是为多个晶胞共用,所以每一个晶胞只能按比例分摊。
分摊的根本原则是:
晶胞任意位置上的原子如果是被n个晶胞所共有,则每个晶胞只能分得这个原子的1/n。
具体地,根据晶胞(晶体中最小重复单位)求晶体中粒子个数比的方法是:
①处于顶点的粒子,同时为8个晶胞共有,每个粒子有1/8属于晶胞;②处于棱上的粒子,同时为4个晶胞共有,每个粒子有1/4属于晶胞;③处于面上的粒子,同时为两个晶胞共有,每个粒子有1/2属于晶胞。
例⒈现在四种晶体,其离子排列方式如图所示,其中化学式正确的是()
AB2EF2XY3ZAB
(A)(B)(C)(D)
【分析】根据题意应选C、D。
这类题解题的思维方法为平均法,即先分析基本结构单元中的一个点或一条边为几个结构单元所共有,若为n个基本结构单元共有,则这个基本结构单元就只占有这个点或这条边的1/n。
这种求晶胞中粒子个数的方法还可类推到求晶胞中化学键数目,如:
例⒉石墨是层状晶体,每一层内碳原子排列成正六边形,一个个正六边形排列成平面网状结构,如果将每对相邻碳原子间的短线看成一个化学键,则石墨晶体中每一层内碳原子数与C—C键数的比是()
(A)2∶3 (B)1∶3 (C)1∶1 (D)1∶2
【分析】据石墨的晶体结构可知:
每个碳原子为三个正六边形共用,每个正六边形占有该碳原子的1/3,因此,每个正六边形占有碳原子数为6×
个;晶体中每个C—C键即为每个正六边形的边,每个边为2个正六边形共用,每个正六边形占有该C—C键的
,故每个正六边形占有C—C键数目为6×
=3个,选(A)。
例⒊最近发现一种由钛原子和碳原子构成的气态团簇分子(如下图所示),顶角和面心的原子是钛原子,棱的中心和体心的原子是碳原子,它的化学式是。
【分析】你的答案是TiC吗?
这是错的,为什么呢?
这只不过是一个具有规则结构的大分子,而不是一个空间结构中的最小重复单位,按例1的方法计算自然是错的了。
在这个问题中,我们只需数出两种原子的数目就可以了(Ti14C13),而不必进行上面的计算。
练习:
6、水分子间由于氢键的作用彼此结合而形成(H2O)n,在冰中每个水分子被4个水分子包围形成变形的四面体,通过氢键相互连接成晶体,其结构如下图所示。
则1mol冰中有mol氢键。
7、科学家发现钇钡铜氧化合物在90K具有超导性,若该化合物的结构如下图所示,则该化合物的化学式可能是()
(A)YBa2Cu3O4(B)YBa2Cu2O5(C)YBa2Cu3O5(D)YBaCu4O4
(例三题图) (第6题图) (第7题图)
(第10题图)
(第8题图) (第9题图)
8、石墨晶体是层状结构,在每一层内,每一个碳原子都跟其它3个碳原子相结合。
上图是其晶体结构的俯视图,则图中7个六元环完全占有的碳原子数是()
(A)10个(B)18个(C)24个(D)14个
解析:
一个环6个碳,一个碳由三个环共用,7*6/3=14
9、上图所示为高温超导领域的一种化合物——钙钛矿的结构,该结构是具有代表性的最小重复单元。
试确定该结构单元的质量。
(相对原子质量:
Ca40Ti48O16)
10、二氧化硅是立体的网状结构,其晶体模型如上图所示,请认真观察该晶体模型后回答以下问题:
(1)二氧化硅晶体中最小环为元环;
(2)每个硅原子为个最小环共有;
(3)每个最小环平均拥有个硅原子,个氧原子。
三、晶胞结构与晶体密度的计算
例⒊如图是CsCl晶体的晶胞(晶体中最小重复单元),已知晶体中两个最近的Cs+核间距为acm,氯化铯的式量为M,NA为阿伏加德罗常数,则氯化铯晶体的密度为()
A .
B.
C.
D.
【分析】解法一:
晶体的密度等于晶体的质量与晶体在该质量下的体积的比值(即晶体的密度=
),据式量可知,1molCsCl的质量为M克,故需求出1molCsCl的体积。
因晶体是由晶胞构成的,而1个CsCl晶胞的体积为a3cm3。
因此,此题解题的关键是找出1molCsCl晶体中的晶胞数目,由晶胞的示意图可知,1个晶胞中含1个Cs+和1个Clˉ,所以,在1molCsCl晶体中含NA个的晶胞。
由此可得,晶体的密度为
。
解法二:
一个晶胞的体积为a3cm3,若求出一个晶胞的质量,则可以求出晶胞的密度,也就是晶体的密度(因为晶胞是晶体中最小的结构单元)。
根据晶胞的结构示意图可知,1个晶胞中含1个Cs+和1个Clˉ,所以一个晶胞的质量也就是1个Cs+和1个Clˉ的质量,所以晶胞的质量为
+
,即
=
,因此也可得出晶体的密度。
四、分子内或晶体中化学键数目及多面体面数等的计算
例⒋德国和美国科学家首次制造出了由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成的(如右图所示)。
请回答:
C20分子中共有_____个正五边形,共有_______条棱边。
C20晶体属于___________(填晶体类型)。
【分析】解法一:
从分子结构示意图可以看出,在C20分子内每个碳原子与另外3个碳原子成键,因此,C20分子键总数=20×3×
(因为2个原子形成一个键),也即C20分子中共有30条棱边(因为化学键总数=多面体棱边总数)。
从数学角度,多面体棱边数=多面体面数×每个面的棱边数×
(因为2个面共用一条棱边),设正五边形的个数为x,则有:
30=x×5×
,所以,正五边形的个数为12。
实际上C20与C60都属于碳的同素异形体,应属于分子晶体。
解法二:
设C20分子中含x个正五边形,通过观察图形可知,每一个顶点为三个正五边形共用,则每个正五边形占有该顶点的
,因此,每个正五边形占有碳原子数为5×
个,这个基本结构单元的碳原子数为x×5×
=20,因此,C20分子中含有正五边形个数x=12;每一条边为两个正五边形共用,每个正五边形只占有这条边的
,故C—C键的数目为12×5×
=30个,即C20分子中共有30条棱边。
【总结】在分子内或晶体中:
化学键总数=多面体棱边总数
其中,化学键总数=参与成键的微粒总数×每个微粒的成键数×
(例四题图)
(练习11图)
练习11、已知晶体硼的基本结构单元是由硼原子组成的正二十面体(如下图)。
其中有二十个等边三角形的面和一定数目的顶点,每个顶点各有一个硼原子,则这个基本结构单元由_12___个硼原子构成,共含有_30___个B—B键。
解析:
每个三角形有三个顶点,每个顶点由五个三角形共用,顶点数=20*3/5=12,即为硼原子个数。
每个三角形三个键,每个键两个三角形共用,20*3/2=30,即为棱边数。
五、综合性试题分析
在有关晶体结构的推断和计算试题中,综合性试题往往是试卷中难度最大的题目。
其实,这类试题只是把以上有关分析与计算综合到了一个题中,因此,我们可以采用以上有关解
题方法对其做出分析解答。
例⒌在离子晶体中,阴、阳离子按一定规律在空间排列,右图(a)是NaCl的晶体结构,在离子晶体中,阴、阳离子具有或近似具有球形对称结构,它们可以被看作是不等径的刚性圆球,并彼此相切如NaCl晶体结构图(b),已知a为常数。
(1)在NaCl晶体中,每个Na+同时吸引个Cl-;Na+数目和Cl-数目之比为;
(2)Na+半径与Cl-半径之比=(已知
=1.414);
(3)NaCl晶体中不存在分子,但在1.013×105Pa,1413℃时,NaCl晶体形成气体,并以分子形式存在。
现有29.25克NaCl晶体,在1.013×105Pa时强热使温度达到1501.5℃,测得气体体积为36.4L,试应用有关物理、化学知识计算此时氯化钠气体的分子式(不写计算过程);
(4)若a=5.6×10-8cm,求NaCl晶体的密度(已知5.63=175.6,NaCl的摩尔质量为58.5g/mol)。
【解析】
(1)6,1∶1
(2)由图(b),因为r(Cl-)>r(Na+),则r(Cl-)=
2r(Na+)=a-2r(Cl-)=a-2×
,即r(Na+)=
所以,
=
=0.414
(3)摩尔质量M=
=117g/mol
设NaCl分子式为(NaCl)n,则有58.5n=117n=2,即NaCl气体的分子式为Na2Cl2。
(4)由NaCl晶体结构分析,每个晶体中含有4个“NaCl分子”,则有ρV=
,所以ρ=
/(5.6×10-8)3=2.2g/cm3
12、某离子晶体晶胞结构如下图所示,X位于立方体的顶点,Y位于立方体的中心,试回答:
(1)晶体中每个Y同时吸引着个X,每个X同时吸引着个Y,该晶体的化学式为。
(2)晶体中在每个X周围与它最接近且距离相等的X共有个。
(3)晶体中距离最近的2个X与一个Y形成的夹角(∠XYX)为(填角的度数)。
(4)设该晶体的摩尔质量为Mg·mol-1,晶体密度为ρg·cm-3,阿伏加德罗常数为NA,则晶体中两个距离最近的X中心间的距离为cm。
13、根据石墨晶体结构示意图及提供的数据计算(保留三位有效数字)。
有关公式、数据见框图。
(练习12图) (练习13图)
(1)12g石墨中,正六边形的数目有多少?
(二)规划环境影响评价的技术依据和基本内容
(2)求石墨的密度。
一、环境影响评价的发展与管理体系、相关法律法规体系和技术导则的应用(3)求12g石墨的体积(cm3)。
练习题答案:
1、12,八面体;2、6;3、12;4、6,109°28;
(2)规划编制机关在报送审批专项规划草案时,将环境影响报告书一并附送。
5、正六边形,3;6、27、C;8、D;
(2)评价方法的适当性;9、2.26×10-22g;(提示:
该结构单元的质量即为属于该结构单元中的原子的总质量);
(1)可能造成重大环境影响的建设项目,编制环境影响报告书,对产生的环境影响应进行全面评价;10、
(1)12,
(2)12,(3)1/2,1;
3)选择价值。
选择价值(OV)又称期权价值。
我们在利用环境资源的时候,并不希望它的功能很快消耗殆尽,也许会设想未来该资源的使用价值会更大。
11、12,30
12、
(1)4;8;XY2或Y2X;
(2)12;(3)109°28′(提示:
4个X原子位于正四面体的四个顶点上,Y原子位于该正四面体的中心)(4)
(提示:
每个晶体中含个
X和1个Y,则1molXY2中含有2NA个晶胞,故每个晶胞的边长为
,距离最近的两个X位于面对角线上,据勾股定理可求出其距离)。
2)按发布权限分。
环境标准按发布权限可分为国家环境标准、地方环境标准和行业环境标准。
13、
(1)3.01×1023;
(2)2.28g/cm3;(3)5.26cm3
解析:
(1)每个C为三个正六边形共有,每个六边形占有
个碳原子,六边形碳数=6×
=2,所以正六边形个=
市场价格在有些情况下(如对市场物品)可以近似地衡量物品的价值,但不能准确度量一个物品的价值。
三者的关系为:
=3.01x1023
(2)由于层与层可滑动,抽象出一个正六棱柱,
六棱柱体积=6
sin60°a2b=
由于每个正六边形为两个正六棱柱共有,所以每个正六棱柱占有2个C
(6)评价结论。
密度=
(5)法律、行政法规和国务院规定的其他建设项目。
(3)12g石墨体积=
=5.26cm3