人教版春秋版九年级上学期期末考试化学试题II卷Word文档格式.docx
《人教版春秋版九年级上学期期末考试化学试题II卷Word文档格式.docx》由会员分享,可在线阅读,更多相关《人教版春秋版九年级上学期期末考试化学试题II卷Word文档格式.docx(15页珍藏版)》请在冰豆网上搜索。
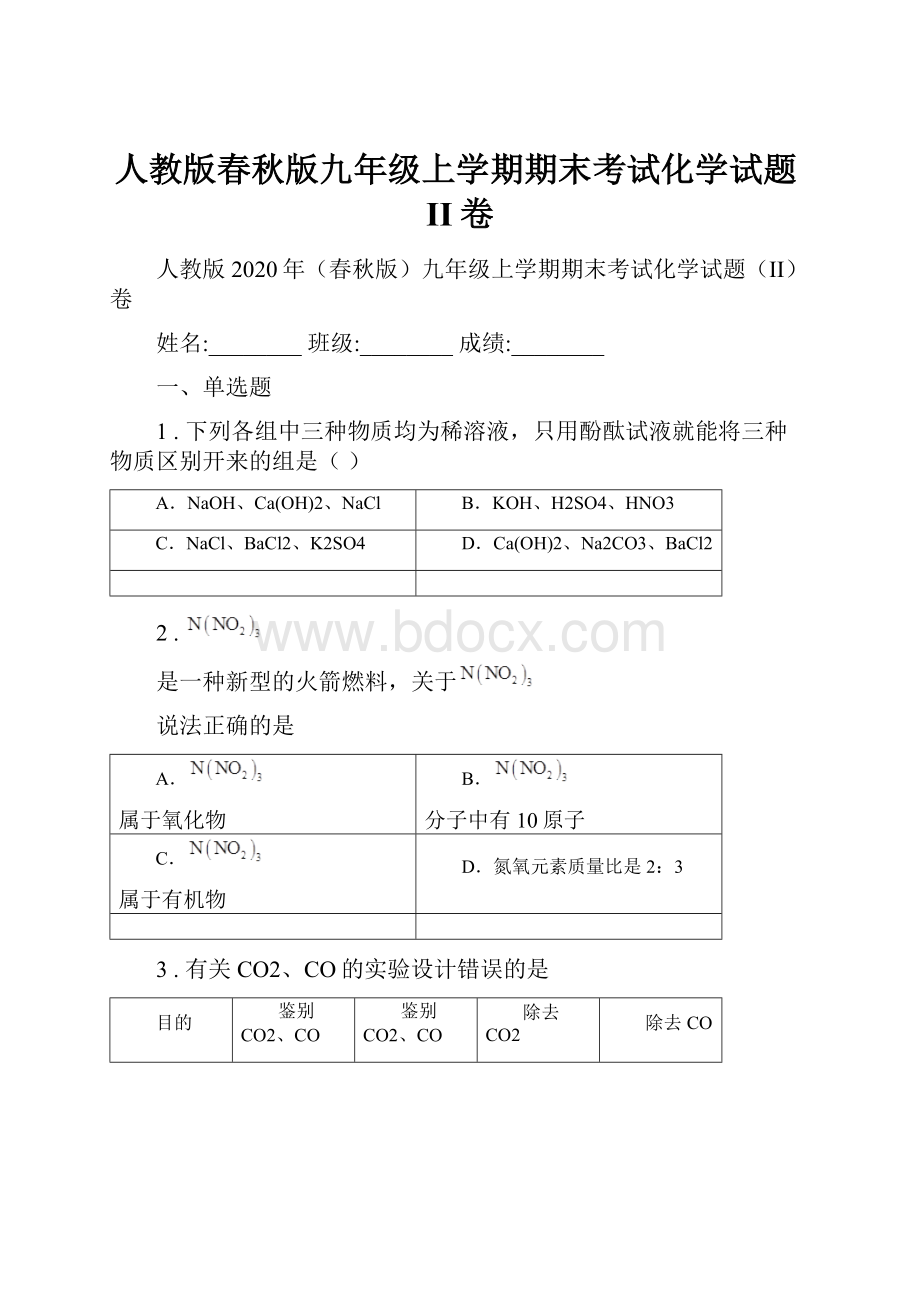
A
B
C
D
A.A
B.B
C.C
D.D
4.铝跟盐酸或氢氧化钠溶液都能反应且产生H2。
反应的化学方程式如下:
2Al+6HCl=2AlCl3+3H2↑;
2Al+2NaOH+2H2O=2NaAlO2+3H2↑。
甲、乙两烧杯中各盛有109.5g10%的盐酸和120g10%NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体质量比为甲∶乙=1∶2,则加入铝粉的质量为
A.1.8g
B.2.7g
C.3.6g
D.5.4g
5.下列有关溶液的说法,正确的是()
A.溶液一定是无色液体
B.溶液一定是均一稳定的混合物
C.将KNO3的不饱和溶液变成饱和溶液,溶液中溶质的质量分数一定变大
D.20℃时硝酸钾的溶解度是31.6g,说明该温度下100g硝酸钾溶液中含有硝酸钾31.6g
6.下列图示实验操作中,正确的是()
A.读出液体的体积
B.用灯帽熄灭酒精灯
C.将NaOH固体直接放在托盘上称量质量
D.加热试管中的液体
7.存放下列物品的区域不需要张贴
的是()
A.浓硫酸
B.氢氧化钠固体
C.汽油
D.纯净水
8.关于金属物品的使用正确的是()
A.铝合金门窗变旧变暗后可用砂纸或钢丝球打磨
B.铝壶内的水垢可用溶质质量分数为18%的盐酸长时间浸泡
C.校内用钢架制作的自行车防雨棚应定期喷涂油漆防锈
D.铁桶可以长时间保存波尔多液
9.下列有关分子、原子的说法正确的是()
A.水壶中的水烧开时壶盖被顶起是因为水分子受热变大的缘故
B.所有的原子都是由质子、中子和电子构成的
C.分子、原子的本质区别是化学变化中是否可分
D.水变成冰后水分子停止运动
10.将一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量见表:
物质
甲
乙
丙
丁
反应前质量/g
6.0
2.2
2.6
0.7
反应后质量/g
待测
4.0
3.6
关于这四种物质,下列说法正确的是()
A.甲、乙是反应物,丙是生成物
B.丁定是该反应的催化剂
C.参加反应的甲的质量为
D.甲一定是化合物
11.下列物质的转变,只有通过加酸才能实现的是()
A.Zn→ZnSO4
B.MgO→MgCl2
C.CaCO3→CO2
D.BaCl2→BaSO4
12.逻辑推理是化学学习中常用的思维方法。
下列推理正确的是()
A.中和反应生成盐和水,则生成盐和水的反应一定是中和反应
B.化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物
C.Na2SO4溶液与BaCl2溶液反应生成白色沉淀,所以加入BaCl2溶液生成白色沉淀的原溶液中必含可溶性硫酸盐
D.活泼金属能与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属
13.中华文化博大精深,在许多成语中蕴含着物理变化、化学变化.下列成语中蕴含化学变化的是()
A.水滴石穿
B.火烧赤壁
C.刻舟求剑
D.杯弓蛇影
14.化学与生活、生产、科技密不可分。
下列叙述中正确的是()
A.用甲醛浸泡过的水产品可以放心食用
B.用氮气做金属焊接保护气
C.利用烧碱改良酸性土壤
D.用食盐水除去水壶上的水垢
15.马铃薯富含淀粉、蛋白质、维生素C、磷、钙等。
下列说法错误的是
A.钙元素可以预防佝偻病
B.蛋白质、淀粉属于有机高分子化合物
C.维生素C可以预防坏血病
D.钙、磷都属于微量元素
16.甲、乙、丙三种固体物质的溶解度曲线如图所示,从中获取的信息正确的是
A.t2℃,甲、丙的溶解度相等
B.降低温度可使接近饱和的丙溶液变饱和
C.使乙从溶液中结晶,多采用冷却热饱和溶液的方法
D.t1℃时,甲、丙饱和溶液的溶质质量分数均为16.7%
17.下列有关说法:
①CO、CO2、SO2、NO2和O3是污染空气的气体成分。
②水占地球表面积3/4,因而水资源取之不尽,用之不竭。
③煤、石油、天然气和乙醇汽油都是不可再生资源。
④水、蛋白质、糖类等是人体六大营养素之一。
⑤在田里焚烧秸秆既浪费了资源,也造成了空气污染,是不可取的。
⑥木材是造纸的主要原料之一,节约纸张有利于保护森林。
⑦铜有良好的导电性,因而大量用于制作电线。
正确的组合是()
A.①②③④
B.④⑤⑥⑦
C.①④⑤⑦
D.②③⑤⑦
18.物质性质决定用途。
下列说法正确的是
A.浓硫酸具有吸水性,可用于干燥氨气
B.熟石灰能与酸反应,可用于改良酸性土壤
C.甲醛能使蛋白质变性,可用于食用水产品防腐
D.铵态氮肥能增大土壤酸性,应和碱性物质混合使用
19.下列物质中,属于盐的是()
A.氯化钠
B.盐酸
C.氧化镁
D.氢氧化铝
20.引起酸雨的主要气体是
A.二氧化硫
B.二氧化碳
C.甲烷
D.氨气
二、填空题
21.
(1)保护环境,大力提倡“低碳生活”,“石头纸”是倡导“低碳生活”的一个例子.它是以地壳内最为丰富的矿产资源碳酸钙为主要原料,经特殊工艺加工而成的一种可逆性循环利用纸,其外观与普通纸相似.请鉴别“石头纸”与“普通纸”:
①可分别燃烧这两种纸,易燃烧的是_____纸;
②可向纸上分别滴加_____,有明显现象的是_____纸;
③为验证上述②中的气体可将该气体通入到_____中.
(2)现有H、C、O、Ca、Na五种元素,选用其中的元素写出符合下列要求的物质的化学式
①有还原性的气体化合物_____②西气东输的气体是_____
③侯氏制碱法制得的“碱”是_____④常用的食品干燥剂_____.
22.很多金属都能与氧气、盐酸、稀硫酸等发生反应,但反应的难易和剧烈程度不同。
(______)
23.下列是探究分子基本特性的实验。
回答下列问题:
I得出的结论是____。
III中A、B两烧杯中的物质没有____,其中A杯中的无色溶液却产生与II中相同的实验现象,证明____。
三、实验题
24.水是人类赖以生存的物质之一,人们的生活需要干净的水。
试回答下列问题:
(1)下列净水方法:
①静置沉淀;
②蒸馏;
③吸附沉淀;
④过滤,净水程度由高到低的顺序是______。
B.①③④②
C.②④③①
D.④③②①
(2)如图为过滤装置。
写出下列仪器、用品的名称:
A______(作用:
______),C______;
某同学用如图的装置进行过滤操作,实验后发现滤液仍浑浊,请你写出可能的两点原因:
①__________________,②__________________;
试举出生活中利用过滤原理的实例:
________________________。
(3)净水时,常用______(填序号,下同)作为吸附剂来除去水中的色素和异味,净化后水变澄清:
用______来区分净化后的水是软水还是硬水。
①明矾
②食盐水
③活性炭
④肥皂水
⑤漂白粉[主要成分是Ca(ClO)2]
(4)生活中常用______方法使硬水转化成软水。
25.化学实验是学习化学和进行科学研究的重要方法和途径。
学会气体物质的制备方法是研究气体、利用气体的基础。
请根据下图回答有关问题:
①
②
③
④
⑤
⑥
(1)在常温下实验室欲制取氧气所选用的装置是
(填序号),为了便于调控反应的进行,可以对发生装置进行改进,请简要说明你的改进措施
。
(2)从上述仪器中选择一种你比较熟悉的仪器,写出它的名称
,简要写出它的用途
(3)同学们以“化学反应中,反应物与生成物的质量关系”为课题进行探究。
经讨论分析、查阅资料后设计了A、B两套实验装置,并在实验过程中做到操作规范、准确称量和细致观察。
实验完毕后,使用A装置进行实验得到的结果是:
反应前后反应物的总质量与生成物的总质量相等;
而使用B装置进行实验得到的结果是:
反应前后反应物的总质量与生成物的总质量不相等。
请你分析导致出现两种不同结果的原因是
写出B装置中发生反应的化学方程式
-。
26.某化学兴趣小组用一氧化碳与氧化铁的反应来探究炼铁的原理,装置如下图所示。
请回答有关问题:
(1)为避免一氧化碳污染空气,a处应该如何处理____。
(2)实验开始时,先通CO,目的是____。
(3)实验进行一段时间后,玻璃管A中出现的现象为_____,由此可推断出一氧化碳的化学性质具有_____性。
四、推断题
27.现有木炭、一氧化碳、氧化铜、氧化铁、稀硫酸五种物质,它们之间发生的反应,可用“A+B→C+D”表示.
(1)若A为单质,A与B在高温下反应,可观察到固体粉末由黑色逐渐变红,则B是_____,有关反应的化学方程式为_____.
(2)若A为气体化合物,A与B在高温下反应,可观察到固体粉末由红色逐渐变黑,则A是_____,B是_____.
(3)若A溶液pH<7,A与B在常温下反应,可观察到溶液由无色变为黄色,则A与B反应的化学方程式为_____.
五、科学探究题
28.科学方法对化学学习起着事半功倍的作用。
(一)微观粒子模型化是研究化学变化的重要方法。
(1)图甲是钠与氯气反应生成氯化钠示意图。
该图说明在化学反应过程中一定发生变化的是_____(填序号)。
a.原子核 b.原子的最外层电子数 c.原子的电子层数
(2)图乙是硫酸铜溶液与氯化钡溶液反应的示意图。
该反应的实质是A+B→C,请用微粒符号表示该反应的实质_________________________________________________________。
(二)控制变量、设计对比实验是实验探究的重要方法。
(3)实验1振荡3个塑料瓶,观察到塑料瓶变瘪的程度由大到小为_______________________(用A、B、C填写),其中变浑浊的瓶内发生反应的化学方程式为__________;
对比A瓶与______(填“B”或”C”)瓶的实验现象,可证明CO2能与NaOH发生反应。
(4)实验2探究物质燃烧的条件。
将大小相同的红磷和白磷放在薄铜片的两侧,加热铜片的中部,观察现象。
通过此实验,可说明燃烧的条件之一的是_____________(填序号)。
A.可燃物
B.空气
C.温度达到着火点
(5)实验3是探究铁钉条件的实验,会出现明显现象的是试管______(填“I”“II”或“III”),说明铁生锈实际上是铁与____________________________________发生反应。
29.NaCl、Na2CO3、NaHCO3、CaCO3是生活中常见的盐,为学习鉴别他们的方法,老师拿来了标有A、B、C、D的这四种白色固体,并提供以下资料。
查阅资料:
(1)Ca(HCO3)2可溶于水
(2)NaHCO3
Na2CO3+H2O+CO2↑;
Na2CO3的热稳定性好,受热不分解。
(3)不同温度下,Na2CO3、NaHCO3的溶解度如下表:
设计方案:
为完成鉴别,同学们分别设计了自己的实验方案
(1)小芳的实验中,步骤1鉴别出来的物质是__________。
(2)小明和小刚的步骤1都是溶解,该步实验的目的是__________。
进行实验:
小刚的步骤1溶解的具体操作为________________________;
小刚在进行步骤2时,发现在两只试管中产生了白色沉淀,小刚推测它们是Na2CO3、NaHCO3。
则NaHCO3与石灰水反应的产物可能是__________。
(用化学方程式表示)
反思与评价:
(1)小刚的设计能不能完成鉴别,理由是__________。
(2)小丽觉得大家的方案太麻烦,她跟老师要了一些氯化钠,做了下图所示的实验,由该实验得出的结论是__________。
在此实验基础上,小芳用一步完成了鉴别,她的实验方法是__________。
六、计算题
30.造纸是我国古代四大发明之一。
农作物的秸秆可作为造纸原料,其主要成分是纤维素[
]
(1)纤维素属于________(填“糖类”、“油脂”或“蛋白质”)。
(2)纤维素由________种元素组成,其中氢、氧元素的质量之比为________。
31.今天是某校实验室开放日,晓明同学用锌和稀硫酸反应制取氢气。
先向气体发生装置中加入一定量的锌粒,然后将60克稀硫酸分三次加入,每次生成气体的质量如下表:
次数
第一次
第二次
第三次
加入稀硫酸质量/g
20
生成氢气的质量g
0.08
0.04
试计算:
(1)共制得氢气_____g。
(2)反应中消耗的锌粒的质量。
_____(写出计算过程)
参考答案
1、
2、
3、
4、
5、
6、
7、
8、
9、
10、
11、
12、
13、
14、
15、
16、
17、
18、
19、
20、