校级联考福建省泉州市学年度 高二化学上学期期末教学质量跟踪监测试题Word格式文档下载.docx
《校级联考福建省泉州市学年度 高二化学上学期期末教学质量跟踪监测试题Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《校级联考福建省泉州市学年度 高二化学上学期期末教学质量跟踪监测试题Word格式文档下载.docx(35页珍藏版)》请在冰豆网上搜索。
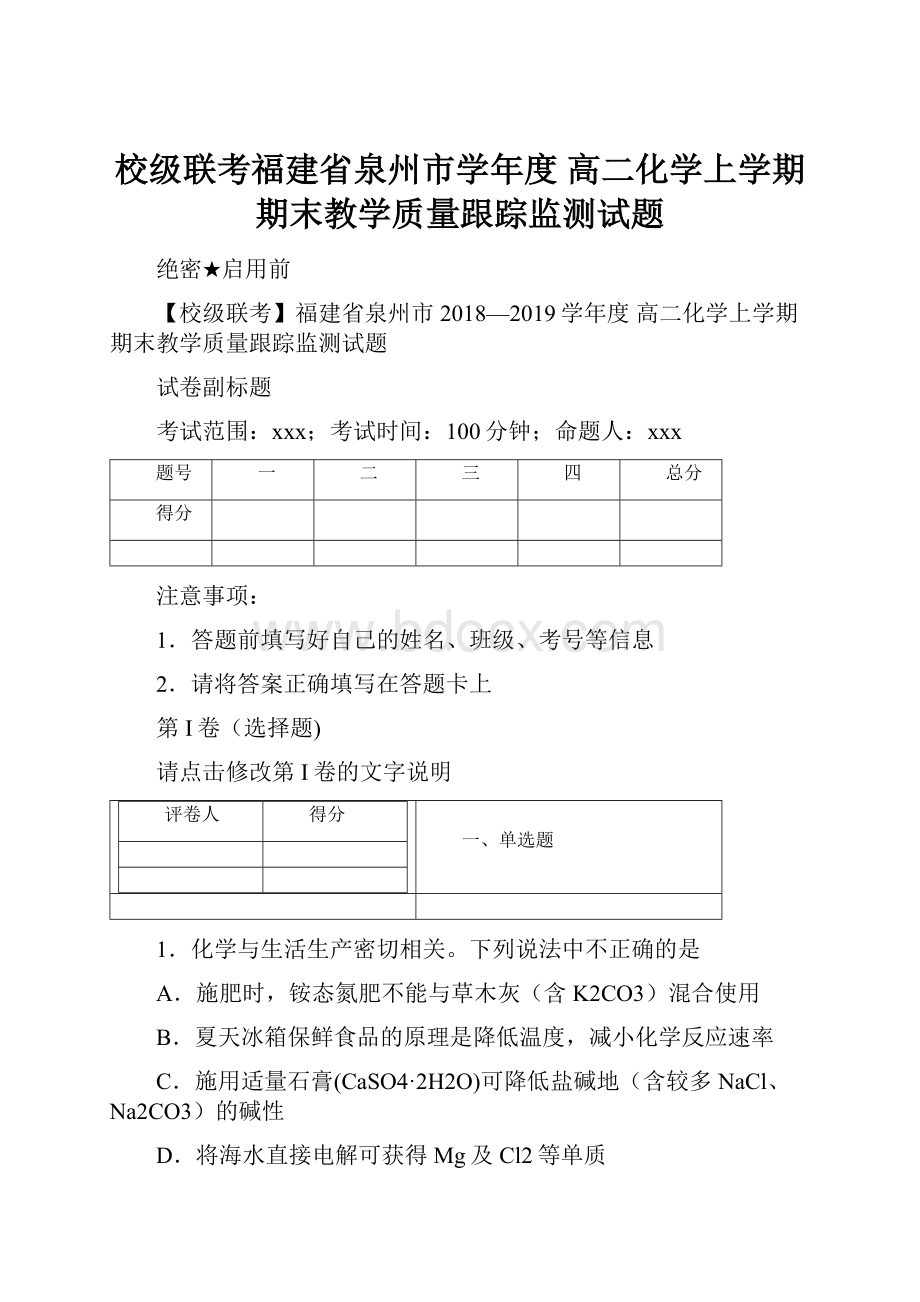
D.KF溶液:
F-+H2O=HF+OH-
4.下表中物质的分类组合完全正确的是
编号
A
B
C
D
强电解质
KNO3
H2SO4
BaSO4
HClO4
弱电解质
NH3·
H2O
CaCO3
HClO
C2H5OH
非电解质
SO2
Al
CH3COOH
A.AB.BC.CD.D
5.一定体积的稀盐酸与过量的铝条反应,为了减缓反应速率且不影响生成氢气的总量,可向盐酸中加入适量的
A.NaCl固体B.CH3COOK溶液
C.Na2CO3溶液D.CuCl2溶液
6.下列说法或表示方法中不正确的是
A.在同温同压下,等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.室温下,pH=2的盐酸与pH=12的氨水等体积混合,溶液呈碱性
C.氢氧化钡晶体与氯化铵晶体的反应属于吸热反应
D.常温下,0.1mol·
L-1的NaOH溶液和0.06mol·
L-1的H2SO4溶液等体积混合,混合溶液的pH=2
7.下列事实能用勒夏特列原理解释的是
A.SO2氧化成SO3的反应,往往需要使用催化剂
B.H2、I2(g)、HI平衡混合气加压后颜色加深
C.工业上采用高压条件合成氨气
D.在硫酸亚铁溶液中加入铁粉以防止氧化变质
8.为证明某一元酸HR是弱酸,下列实验方法错误的是
A.室温时,测定0.01mol·
L-1的HR溶液的pH=4
B.室温时,往NaR溶液中滴加无色酚酞试液,溶液变红色
C.相同条件下,对浓度均为0.1mol·
L-1盐酸和HR溶液进行导电性实验
D.0.1mol·
L-1的HR溶液与同体积0.1mol·
L-1的氢氧化钠溶液恰好完全反应
9.常温下,下列各组离子在指定溶液中,一定能大量共存的是
A.在pH=13的溶液中:
K+、Mg2+、Cl-、SO32-
B.c(H+)/c(OH-)=1×
1012的溶液:
Cu2+、Na+、Cl-、NO3-
C.无色溶液中:
Fe3+、NH4+、Cl‾、SO42‾
D.由水电离出c(OH-)=1.0×
10-12mol·
L-1的溶液中:
Al3+、NH4+、Cl-、SO42-
10.下列有关装置图的叙述中正确的是
A.用装置①给铜镀银,则b极为单质银,电解质溶液为AgNO3溶液
B.装置②的总反应式:
Cu+2Fe3+=Cu2++2Fe2+
C.装置③中钢闸门应与电源的负极相连被保护,该方法叫做外加电流的阴极保护法
D.装置④中插入海水中的铁棒,越靠近底端腐蚀越严重
11.下列实验操作能达到目的的是
A.在中和热的测定实验中,可将稀盐酸换成浓硫酸
B.欲除去水垢中的CaSO4,可先用碳酸钠溶液处理,再用盐酸处理
C.用标准盐酸滴定未知浓度的NaOH溶液,用蒸馏水洗净滴定管后,可直接装入标准盐酸进行滴定
D.配制氯化铁溶液时,将氯化铁固体溶解在较浓的硫酸中再加水稀释
12.下列有关电解质溶液的说法正确的是
A.向0.1mol·
L-1CH3COOH溶液中加入少量水,溶液中导电粒子的数目减少
B.升高CH3COONa溶液的温度,溶液中
增大
C.盐酸与氨水恰好完全反应,则溶液中c(H+)=c(OH-)
D.向AgCl的饱和溶液中加入少量AgNO3溶液,则溶液中c(Ag+)·
c(Cl-)保持不变
13.常温下,几种弱酸的电离平衡常数如下表所示,下列说法正确的是
化学式
HCOOH
H2CO3
HCN
电离平衡常数
K=1.8×
10-4
K1=4.3×
10-7K2=5.6×
10-11
K=4.9×
10-10
A.酸性强弱顺序是:
HCOOH>
HCN>
H2CO3
B.物质的量浓度均为0.1mol·
L-1的HCOONa溶液和NaCN溶液,pH大小顺序:
HCOONa<
NaCN
C.HCOOH的电离平衡常数表达式为K=
D.H2CO3溶液和NaCN溶液反应的离子方程式为H2CO3+2CN-=2HCN+CO32-
14.在一定条件下,密闭容器中进行反应CH4(g)+H2O(g)
CO(g)+3H2(g)
,测得CH4的体积百分含量随温度和压强的变化如图所示。
下列说法正确的是
A.p1>
p2
B.ΔH<
C.加入催化剂可以提高甲烷的转化率
D.恒温下,缩小容器体积,平衡后CH4浓度减小
15.将等物质的量的A、B混合于2L的密闭容器中,发生下列反应
2A(g)+B(g)
xC(g)+2D(g),经4min后达平衡,测得D的浓度为1.0mol·
L-1,
c(A):
c(B)=2:
3,以C表示的平均速率v(C)=0.125mol·
L-1·
min-1,下列说法不正确的是
A.反应速率v(A)=0.25mol·
min-1
B.该反应方程式中,x=1
C.4min时,B的物质的量为2mol
D.该反应的平衡常数K=1/3
16.含有某些含氧酸根杂质的粗KOH溶液可用电解法提纯,其工作原理如图所示。
下列有关说法正确是
A.装置右侧发生的电极反应式为:
4OH--4e-=2H2O+O2↑
B.通电后阴极区附近溶液pH会减小
C.m是电源负极
D.纯净的KOH溶液从b出口导出
17.硫代硫酸钠溶液与稀硫酸可发生反应:
Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,某同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。
设计实验如下
实验编号
反应温度/℃
Na2S2O3溶液
稀H2SO4
V/mL
c/(mol·
L-1)
①
25
5
0.1
10
②
0.2
③
④
50
⑤
8
V1
A.实验①和实验④中最先出现浑浊的是实验①
B.其他条件不变时,探究温度对化学反应速率的影响,应选择实验③和实验④
C.选择实验①和实验③,测定混合液变浑浊的时间,可探究硫酸浓度对化学反应速率的影响
D.选择实验④和实验⑤,可探究Na2S2O3
的浓度对反应速率的影响,则V1=10mL
18.室温下,将0.1000mol·
L-1盐酸滴入20.00mL未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如右图所示,下列说法正确的是
A.b点处的溶液中c(Cl-)>
c(M+)>
c(OH-)>
c(H+)
B.室温下,MOH的电离平衡常数Kb为1×
10-5
C.c点处的溶液中c(M+)=c(Cl-)=c(H+)=c(OH-)
D.d点处的溶液中c(MOH)+c(H+)=c(OH-)
二、新添加的题型
19.回收的废旧锌锰干电池经过处理后可得到锰粉(含MnO2、Mn(OH)2、Fe和炭粉等),由锰粉为主要原料制备高性能磁性材料碳酸锰(MnCO3)的工艺流程如下:
已知:
①2H2SO4+MnO2+2FeSO4=MnSO4+Fe2(SO4)3+2H2O
②部分氢氧化物的Ksp(近似值)如下表(25℃)
物质
Mn(OH)2
Fe(OH)2
Fe(OH)3
Ksp
10-13
10-17
10-38
根据上图流程及有关数据回答下列问题。
(1)锰粉酸溶时,过量FeSO4所起的作用为______________________。
(2)往滤液1中先加入H2O2的目的是氧化Fe2+,该反应的离子方程式为________________,后加入氨水的目的是调节pH除去杂质离子,使滤液中的杂质离子沉淀完全(残留在溶液中的离子浓度≤l0-5mol·
L-1),常温下测得溶液中c(Mn2+)=0.1mol·
L-1,则需调节溶液的pH范围为_______________。
(3)沉锰工序中,加入氨水的目的是(从化学平衡移动的角度解释)__________________,
沉锰工序中判断沉淀已经洗涤干净的实验操作是________________________________。
(4)沉锰后废液中的主要成份为_____________________________。
第II卷(非选择题)
请点击修改第II卷的文字说明
三、综合题
20.
(1)S8分子可形成单斜硫和斜方硫,转化过程如下:
S(s,单斜)
S(s,斜方)ΔH=-0.398kJ·
mol-1,则S(单斜)、S(斜方)相比,较稳定的是______(填“S(单斜)”或“S(斜方)”)。
(2)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJ·
mol-1)
化学键
H—H
H—Cl
键能
436
431
热化学方程式:
H2(g)+Cl2(g)=2HCl(g)ΔH=-183kJ·
mol-1,则Cl2的键能为____kJ·
mol-1。
(3)标准状况下,6.72LC2H2(g)在O2(g)中完全燃烧生成CO2(g)和H2O(l),放出389.7kJ热量,请写出表示C2H2燃烧热的热化学方程式:
____________________________。
(4)已知:
C(石墨)+O2(g)=CO2(g)ΔH1=-akJ·
mol-1
H2(g)+1/2O2(g)=H2O(l)ΔH2=-bkJ·
CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH3=-ckJ·
计算C(石墨)与H2(g)反应生成1molCH4(g)的ΔH为____kJ·
mol-1(用含a,b,c的式子表示)。
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示。
则反应过程中,每生成2molN2理论上放出的热量为__________。
21.电化学原理在能量转换、金属冶炼等方面应用广泛。
(1)图①是碱性锌锰电池,在负极发生反应的物质是__________(填“Zn”或“MnO2”),正极发生_________反应(填“氧化”或“还原”)。
(2)图②是碱性电解质的氢氧燃料电池,B极通入的气体为________,A极发生的电极反应式____________________________________________。
(3)电解法可以提纯粗镓,具体原理如图③所示:
①粗镓与电源___________极相连(填“正”或“负”)。
②镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2-,GaO2-在阴极放电的电极反应式______________________________________________________。
(4)由下列物质冶炼相应金属,须采用电解法的是________(选填字母序号)。
a.NaClb.Fe2O3 c.Cu2S d.Al2O3
22.二甲醚(CH3OCH3),是一种易燃气体。
主要作为甲基化试剂和各类气雾推进剂,在制药、染料、农药工业中有许多独特的用途。
其制备方法之一可由H2和CO合成:
2CO(g)+4H2(g)
CH3OCH3(g)+H2O(g)ΔH<
(1)该反应的ΔS_____0(填“>”、“<”或“=”)。
(2)在恒温恒容容器中,不能判断该反应达到化学平衡状态的依据是____(选填字母序号)。
a.二甲醚和水蒸气的体积比等于1︰1b.容器中压强保持不变
c.v正(H2)=4v逆(CH3OCH3)d.容器中一氧化碳的物质的量不再改变
(3)在密闭容器中,反应达到平衡后下列措施能加快反应速率并提高CO转化率的是___(选填字母序号)。
a.将H2O(g)从体系中分离出来b.缩小容器体积,使体系压强增大
c.加入合适的催化剂d.升高体系温度
(4)T℃时,在2L密闭容器中,充入4molCO和8molH2发生反应,测得H2的物质的量随时间变化如图中状态Ⅰ(图中实线)所示:
①T℃时,在状态Ⅰ的条件下,反应达到C点时体系处于平衡状态,以H2
表示该反应的平均速率v(H2)=_________,CO的转化率是________,反应的平衡常数KⅠ=_________。
②若仅改变某一条件,测得H2物质的量随时间变化如图状态Ⅱ所示,则KⅠ_____KⅡ(填“>”、“<”或“=”)。
③若仅改变某一条件时,测得H2的物质的量随时间变化如图状态Ⅲ所示,则改变的条件可能是_____________________________。
23.常温下,某水溶液M中存在的粒子有Na+、A2-、HA-、H+、OH-、H2O和H2A。
根据题意回答下列问题:
(1)H2A为_____酸(填“强”或“弱”),往H2A溶液中加水会使c(H+)/c(H2A)的值________(填“增大”、“减小”或“不变”)。
(2)若M是由一种溶质组成的溶液,则M的溶质可以是Na2A或________。
①Na2A的水溶液pH________(填“<”、“>”或“=”)7,
原因是:
______________________________(用离子方程式表示)
②往Na2A溶液中加入_______________
可抑制其水解
(选填字母序号)。
a.氯化铵固体
b.
KOH固体
c.水
d.
升高温度
③已知Ksp(CuA)=1.3×
10-36,往20mL1mol·
L-1Na2A溶液中加入10mL1mol·
L-1CuCl2溶液,混合后溶液中的Cu2+浓度为________mol·
L-1。
(忽略A2-的水解)
(3)若溶液M由10mL1.00mol·
L-1H2A溶液与10mL1.00mol·
L-1NaOH溶液混合而成,下列关于溶液M的说法正确的是________(选填字母序号)。
a.c(A2-)+c(HA-)+c(H2A)=1mol·
L-1
b.若溶液显酸性,则c(Na+)>c(HA-)>c(H+)
>c(A2-)>c(OH-)
c.离子浓度关系:
c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-)
d.25℃时,加水稀释后,n(H+)与n(OH-)的乘积变大
(4)浓度均为0.1mol·
L-1的Na2A、NaHA混合溶液中:
=______。
四、实验题
24.化学兴趣小组用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
①称量1.0g样品溶于水,配成250mL溶液;
②用碱式滴定管准确量取25.00mL所配溶液于锥形瓶中,滴加2~3滴酚酞溶液;
③用0.1000mol·
L-1的标准盐酸滴定并重复三次,每次实验数据记录如下:
滴定次数
待测液体积/mL
所消耗盐酸标准溶液的体积/mL
滴定前
滴定后
1
25.00
1.50
21.40
2
2.50
22.60
3
0.60
23.20
(1)称量时,样品应放在________称量(选填字母序号)。
a.小烧杯中 b.洁净纸片上 c.托盘上
(2)如图是某次滴定时的滴定管中的液面,其读数为________mL。
(3)判断滴定终点到达时的现象为_______________________________。
(4)若出现下列情况,测定结果偏高的是________(选填字母序号)。
a.滴定前用蒸馏水冲洗锥形瓶
b.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
c.滴定过程中不慎将数滴酸液滴在锥形瓶外
d.酸式滴定管在滴定前有气泡,滴定后气泡消失
(5)通过计算可知该烧碱样品的纯度为________。
(杂质不与酸反应)。
参考答案
1.D
【解析】
【详解】
A.铵态氮肥与草木灰混合可双水解,造成营养流失,故A正确;
B.降温可降低活化分子百分数,减小有效碰撞次数,反应速率减小,故B正确;
C.“盐碱地”中Na2CO3水解使土壤成碱性,即:
CO32-+H2O
HCO3-+OH-,通过加石膏生成更难溶的碳酸钙沉淀,c(CO32-)减少,使水解平衡向逆反应方向移动,土壤碱性减弱,故C正确;
D.制备活泼金属单质Mg是电解熔融状态MgCl2,故D错误,
故选D。
2.B
A.NaHCO3溶于水后,HCO3-水解使溶液显碱性,故A不符合题意;
B.NH4NO3溶于水后,NH4+水解使溶液显酸性,故B符合题意;
C.Na2SO4是强酸强碱盐,溶于水后,不发生水解,溶液呈中性,故C不符合题意;
D.CH3OH是非电解质,溶于水后,不发生电离,不发生水解,溶液不显酸碱性,故D不符合题意,
故选B。
3.C
A.碳酸是二元弱酸,多元弱酸的强碱盐的水解是分步进行的,不能合并,以第一步为主,故A错误;
B.NaHCO3溶液,离子方程式:
HCO3-+H2O⇌H2CO3+OH-,故B错误;
C.NaHS溶液,离子方程式:
HS-+H2O⇌H2S+OH-,故C正确;
D.KF溶液,离子方程式:
F-+H2O
HF+OH-,应使用可逆符号,故D错误,
故选C。
4.A
【分析】
在水溶液中完全电离的电解质为强电解质,包括强酸、强碱、大多数盐;
在水溶液中只能部分电离的电解质为弱电解质,包括弱酸、弱碱、水等;
在水溶液和熔融状态下都不能导电的化合物称为非电解质。
A.KNO3在水溶液中完全电离,KNO3属于强电解质;
H2O在水溶液中只能部分电离,NH3·
H2O属于弱电解质;
SO2在纯液态时不能导电,SO2为非电解质,A项正确;
B.H2SO4在水溶液中完全电离,H2SO4属于强电解质;
CaCO3难溶于水,但溶解的CaCO3是完全电离的,CaCO3属于强电解质;
Al是单质,不属于非电解质,B项错误;
C.BaSO4难溶于水,但溶解的BaSO4是完全电离的,BaSO4属于强电解质;
HClO在水溶液中只能部分电离,HClO属于弱电解质;
H2O能极微弱的电离,H2O属于弱电解质,C项错误;
D.HClO4在水溶液中完全电离,HClO4属于强电解质;
C2H5OH在水溶液和熔融状态下都不导电,C2H5OH属于非电解质;
CH3COOH在水溶液中只能部分电离,属于弱电解质,D项错误;
答案选A。
5.B
A.加入氯化钠固体,溶液的浓度变化不大,H
+
离子的物质的量不变,不影响生成氢气的总量,基本不影响化学反应速率,故A错误;
B.CH3COOK固体与盐酸反应生成弱电解质醋酸,溶液H+离子浓度降低,化学反应速率减小,但不影响生成氢气的总量,故B正确;
C.Na2CO3溶液与盐酸反应,影响生成氢气的总量,故C错误;
D.CuCl2溶液与Al反应生成Cu,从而形成原电池加快反应速率,故D错误,
6.A
A.硫蒸气具有的能量高于硫固体,所以在同温同压下,等质量的硫蒸气和硫固体分别完全燃烧,硫蒸气燃烧放出能量大于硫固体,故A错误;
B.一水合氨是弱电解质,只有部分发生电离,当氨水的pH=12时,一水合氨的浓度一定远远大于pH=2的盐酸,所以室温下,pH=2的盐酸与pH=12的氨水等体积混合,溶液呈碱性,故B正确;
C.氢氧化钡晶体与氯化铵晶体的反应过程吸收热量,属于吸热反应,故C正确;
D.0.1mol/LNaOH中c(OH-)=0.1mol/L,0.06mol/LH2SO4溶液中c(H+)=0.12mol/L,设溶液的体积是1L,二者等体积混合,则硫酸过量,溶液中剩余c(H+)=
=0.01mol/L,所以溶液pH=-lgc(H+)=2,故D正确,
故选A。
7.C
A.SO2氧化成SO3的反应,往往需要使用催化剂,可以加快化学反应速率,但平衡不移动,不能用勒夏特列原理解释,故A错误;
B.H2(g)+I2(g)⇌2HI(g)反应前后气体系数不变,H2、I2(g)、HI平衡混合气加压后,I2蒸气的浓度变大,颜色加深,但是平衡不移动,不能用勒夏特列原理解释,故B错误;
C.工业上使用高压条件下合成氨气,是增大压强,使化学平衡向气体体积减小的方向移动,即增大氨气的生成率,能用勒夏特列原理解释,故C正确;
D.硫酸亚铁溶液中加入铁粉防止Fe2+氧化变质,与化学平衡无关,故D错误,
8.D
A.室温时,测定0.01mol·
L-1的HR溶液的pH=4,说明溶液中存在电离平衡,则HR是弱酸,故A不符合题意;
B.室温时,往NaR溶液中滴加无色酚酞试液,溶液变红色,说明NaR溶液显碱性,即R-发生水解,则HR为弱酸,故B不符合题意;
C.相同条件下,对浓度均为0.1mol·
L-1盐酸和HR溶液进行导电性实验,盐酸的导电能力强,说明溶液中离子浓度大,HR的导电能力弱,即HR溶液中离子浓度小,说明HR没有完全电离,即证明HR是弱酸,故C不符合题意;
D.0.1mol·
L-1的氢氧化钠溶液恰好完全反应不能说明HR是弱酸,故D符合题意,
9.B
A.pH=13的溶液显碱性,说明该溶液中含有大量OH-,Mg2+和OH-反应生成难溶于水的Mg(OH)2,所以不能大量共存,故A错误;
B.在c(H+)/c(OH-)=1×
1012的溶液中,c(H+)远远大于c(OH-),溶液显酸性,Cu2+、Na+、Cl-、NO3-之间不反应,可以大量共存,故B正确;
C.Fe3+显黄色,所以无色溶