结构化学文档格式.docx
《结构化学文档格式.docx》由会员分享,可在线阅读,更多相关《结构化学文档格式.docx(27页珍藏版)》请在冰豆网上搜索。
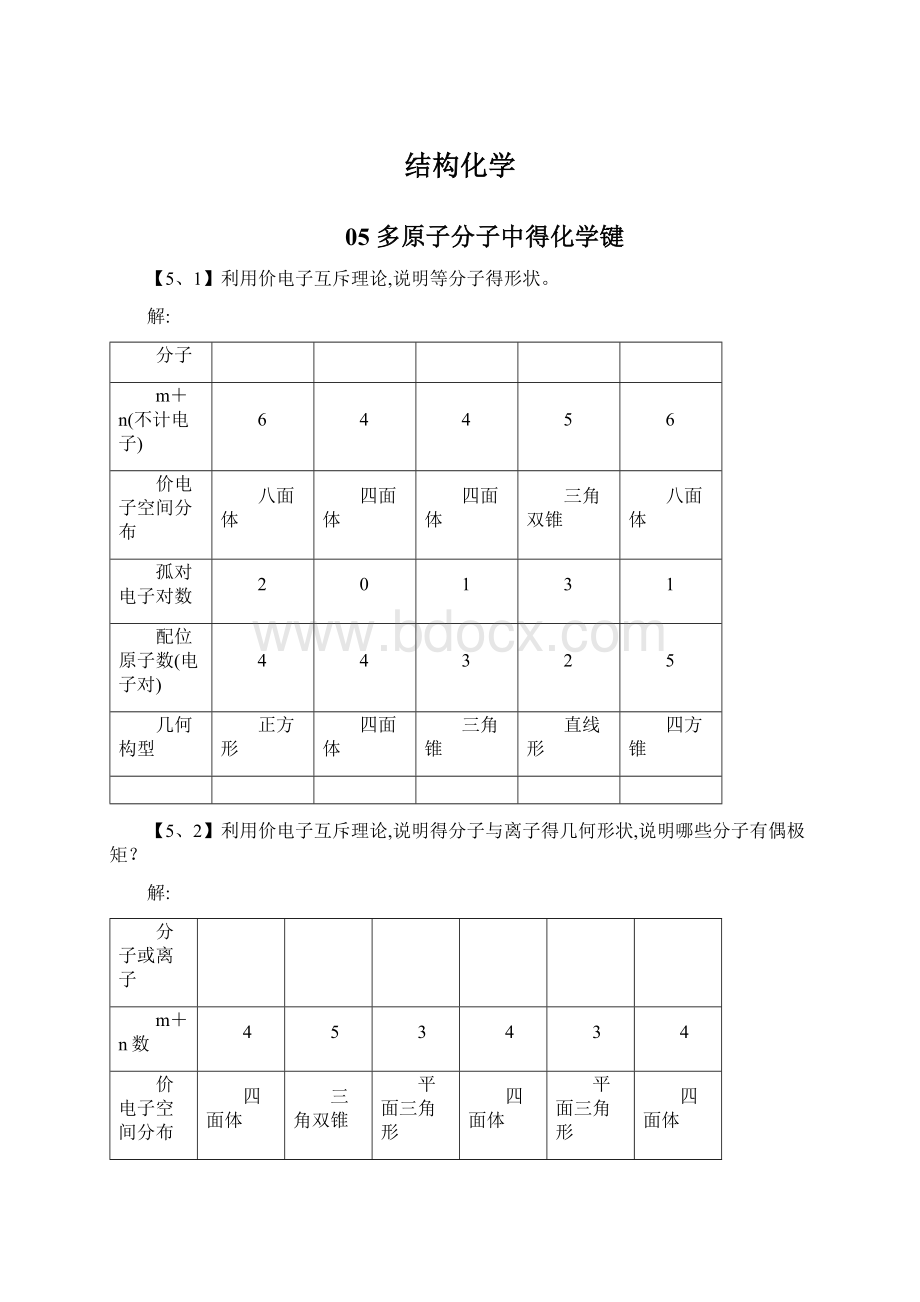
排布方式
(A)
(B)
(C)
lp-lp
lp-bp
bp-bp
(A)与(B)相比,(B)有lp-lp(孤对-孤对)排斥作用代替(A)得lp-bp(孤对-键对)相互作用,故(A)比(B)稳定。
(A)与(C)比较,(C)有两个lp-bp相互作用代替了(A)得2个bp-bp相互作用,故(A)最稳定。
【5、3】画出下列分子中孤对电子与键对电子在空间得排布图:
(a),(b),,;
(c),,,;
(d),。
这就是VSEPR方法得具体应用,现将分子中孤对电子与键对电子在空间得排布图示于图5、3。
图5、3
【5、4】写出下列分子或离子中,中心原子所采用得杂化轨道:
,,,,,,,,,,,。
中心原子得杂化轨道
CS2
三角形
准四面体
【5、5】由,,,轨道组成等性杂化轨道,,这些轨道极大值方向按平面四方形分别与轴平行。
根据原子轨道正交、归一性推出各个杂化轨道得得组合系数,验证它们就是正交,归一得。
因为4个杂化轨道就是等性得,所以每一条杂化轨道得s,p与d成分依次为1/4,1/2与1/4。
这些成分值即s,p与d轨道在组成杂化轨道时得组合系数得平方。
据此,可求出各轨道得组合系数并写出杂化轨道得一般形式:
根据题意,4个杂化轨道得极大值方向按平面四方形分别与x,y轴平行。
设4个杂化轨道与得极大值方向分别在x轴得正方向、x轴得负方向、y轴得正方向与y轴得负方向,则这4个杂化轨道可写成:
这4个杂化轨道就是正交,归一得。
归一性可用该杂化轨道得一般形式证明如下:
正交性证明如下:
任选两个杂化轨道,都得同样结果。
【5、6】臭氧得键角就是。
若用杂化轨道描述中心氧原子得成键轨道,试按键角与轨道成分得关系式计算:
(a)成键杂化轨道中系数与值;
(b)成键杂化轨道得每个原子轨道贡献得百分数。
(a)根据杂化轨道得正交、归一性可得下列联立方程[在本方程中
(2)作为已知条件给出]:
解之,得
所以,O3原子得O原子得成键杂化轨道为:
ψ成
而被孤对电子占据得杂化轨道为:
孤
可见,孤中得s成分比成中得s成分多。
(b)按态叠加原理,杂化轨道中某一原子轨道所占得成分(即该原子轨道对杂化轨道得贡献)等于该原子轨道组合系数得平方。
因此,与对成得贡献分别为与,即分别约为0、3108与0、6892。
【5、7】为直线型对称构型,就是已知最强得氢键。
(a)试画出由原子轨道叠加成分子轨道得图形;
(b)画出得分子轨道能级图;
(c)判断这离子就是顺磁性还就是反磁性;
(d)估计中键得键级。
提示:
取键轴为轴,原子为轨道,原子用轨道(其中只有一个电子),沿轴从正负两个方向与轨道叠加,与同号想加:
没有节面为成键轨道,出现一个节面为非键轨道,两个节面为反键轨道。
(a)根据分子轨道理论,由原子轨道有效地组合成分子轨道必须满足能级高低相近、轨道最大重叠与对称性匹配等3个条件。
其中对称性匹配就是首要条件。
因此,由原子轨道叠加成分子轨道得图形[见图5、7(a)]必须体现出轨道最大重叠与对称性匹配这两个条件,而轨道能级图[见图5、7(b)]则应当反映出参与组合得原子轨道得能级相近这一条件。
以z轴为键轴,F原子得轨道(其中只有一个电子)沿z轴得正、负方向与H原子得1s轨道重叠,形成分子轨道。
若两个轨道都与1s轨道同号重叠,则形成成键轨道;
若一个轨道与另一个轨道异号重叠,而H原子得1s轨道不参加,则形成非键轨道;
若两个轨道都与1s轨道异号重叠,则形成反键轨道。
三个分子轨道都就是型得,它们分别具有0,1与2个节面。
由原子轨道叠加成成键分子轨道得轮廓图示于图5、7(a)中(图形未反映出轨道得相对大小)。
(b)得分子轨道能级图示于图5、7(b)中。
图5、7(a)成键分子轨道图
图5、7(b)分子轨道能级图
【5、8】直线形对称构型得离子,若成键电子只就是轨道上得电子(即将电子作为原子实得一部分)。
(a)画出中每个与轨道得原子轨道叠加图;
(b)画出分子轨道能级图;
(c)中键得键级就是多少?
实验测定分子中键长为,试对计算得键级与键长得关系进行讨论。
(a)以z轴为键轴,按简单分子轨道理论,将中与轨道得原子轨道叠加图示于图5、8(a)。
图5、8(a)原子轨道叠加图
(与形状一样,只就是方向不同)
(b)按题意,离子得分子轨道只由I原子得5p轨道叠加而成。
因此,离子中只有9个分子轨道,其中3个轨道,6个轨道(成键、非键与反键轨道各两个,分别沿x,y方向分布)。
16个电子按能量最低原理、Pauli原理与Hund规则排布在8个分子轨道上,能级图示于图5、8(b)中。
图5、8(b)能级图
(a)[I-I-I]-得总键级为(6-4)/2=1,但其中有2个I-I键,所以每个I-I键得键级为1/2,即I原子与I原子之间只形成了半个键。
这与实验测定得中I-I键长值较I2中I-I键长大,就是完全一致得。
离子中无不成对电子,因而它就是反磁性得。
【5、9】分子呈三方双锥构型,原子采用杂化轨道与原子成键。
若将杂化轨道视为与两杂化轨道得组合,请先将安放在一直角坐标系中,根据坐标系与杂化轨道得正交、归一性写出原子得5个杂化轨道。
PF5分子得坐标管子如图5、9所示。
图5、9
根据图中各原子轨道、杂化轨道得相应位置与空间方向以及杂化轨道得正交、归一性质,P原子得5个杂化轨道为:
【5、10】有两种同分异构体,就是哪两种?
为什么只有一种同分异构体?
N2H2分子中N=N为双键,不能自由旋转(因双键中轨道叠加有方向性),故有顺式与反式两种异构体,它们得结构式如下:
顺N2H2反N2H2
两种异构体中N原子都用杂化轨道成键,分子呈平面形。
顺-N2H2分子属点群,反-N2H2分子属点群。
两者皆无旋光性。
C2H2分子得C原子采用杂化轨道成键,分子呈直线形,属点群,因而它无同分异构体。
C2H2分子得结构如图5、10。
图5、10
【5、11】试证明含、、、得有机分子,若相对分子质量为奇数。
则分子中含有原子数必为奇数;
若相对分子含量为偶数,则含原子数亦为偶数。
论证:
本题所涉及得就是分子中各原子相互化合时得数量关系,其实质就是共价键得饱与性。
这些数量关系对于确定有机化合物得结构式很有用。
分子中各个原子周围化学键数目得总与为偶数(n重键计作n个单键)。
由此可推得,具有奇数个单键得原子得数目之与必为偶数,即奇数价元素得原子数之与必为偶数。
在含C,H,O,N得有机物分子中,C与O就是偶数价原子,H与N就是奇数价原子。
因此,H与N原子数之与为偶数,即H原子数为奇数时N原子数亦为奇数;
H原子数为偶数时N原子数亦为偶数。
含C,H,O,N得有机化合物,其相对分子质量为:
式中与,分别就是C,O,N与H得原子数。
由于前三项之与为偶数,因而相对分子质量得奇偶性与H原子数得奇偶性一致。
而上面已证明,H原子数得奇偶性与N原子数得奇偶性一致,所以,相对分子质量得奇偶性与N原子数得奇偶性一致,即相对分子质量为奇数时N原子数必为奇数;
相对分子质量为偶数时N原子数必为偶数。
【5、12】用HMO法解环丙烯正离子得离域键分子轨道波函数,并计算键键级与原子得自由价。
(1)得骨架如图5、12(a)所示:
图5、12(a)
按LCAO,其离域键分子轨道为:
式中为参与共轭得C原子得p轨道,为变分参数,即分子轨道中C原子得原子轨道组合系数,其平方表示相应原子轨道对分子轨道得贡献。
按变分法并利用HMO法得其本假设进行简化,可得组合系数应满足得久期方程:
用除各式并令,则得:
欲使为非零解,则必须使其系数行列式为零,即:
解此行列式,得:
将值代入,得:
能级及电子分布如图5、12(b)。
图5、12(b)
将代入久期方程,得:
解之,得:
。
根据归一化条件,,求得:
即:
利用分子得镜面对称性,可简化计算工作:
若考虑分子对过得镜面对称,则有:
根据归一化条件可得:
波函数为:
若考虑反对称,则。
所以,得离域键分子轨道为:
三个分子轨道得轮廓图示于图5、12(c)中(各轨道得相对大小只就是近似得)。
图5、12(c)
在已经求出与关系式得基础上,既可根据“每一碳原子对各分子轨道得贡献之与为1”列方程组求出与,也可以利用正交性求出与。
此不赘述。
(2)共轭体系中相邻原子间键键级为:
式中与分别就是第个分子轨道中与得原子轨道组合系数,则就是分子轨道中得电子数。
中有2个电子,基态时都在上。
所以键键级为:
(3)既然,各C原子得自由价必然相等,即:
【5、13】用HMO法求丙二烯双自由基得型分子轨道及相应得能量,并计算键键级。
(1)求分子轨道及相应得能量。
方法1:
中有2个互相垂直得离域键。
对每一个,简化得久期方程为:
用除式中各项并令,得:
欲使不全为零,则必须使其系数(此处系数就是指,因为就是要求得未知数)行列式为0,即:
解之,得。
将值代入,得:
中2个得分子轨道得能级及基态电子分布如图5、13(a)。
图5、13(a)
2个中电子得总能量为:
总
因而丙二烯双自由基得离域能为:
将此三式与归一化条件式联立,解之,得:
由此得第一个分子轨道:
同法,可求出分别与与对应得另两个分子轨道:
得三个分子轨道得轮廓图示于图5、13(b)中。
图5、13(b)
各轨道得大小、正负号、对称性、节面等性质可根据轮廓图进行讨论。
在用本法求共轭体系得型分子轨道时,更简捷得做法就是直接从写含得久期行列式开始。
设相应于某一原子得元为,则与该原子相连原子得元为1,不相连原子得元为0。
解行列式,求出。
将各值代入含与得久期方程,结合归一化条件,即可写出各原子轨道得组合系数,进而写出各分子轨道。
将值代入,即可求出与各分子轨道相应得能量。
方法2:
将分子中各C原子编号并根据编号写出久期方程:
123
其中,为C原子p轨道(下面用表示)得组合系数,而。
根据分子得镜面()对称性将久期方程简化。
考虑对称,则,久期方程简化为:
系数行列式为:
将代入简化得久期方程,得:
结合归一化条件,可得:
由此得分子轨道:
将代入,得。
结合归一化条件,得:
考虑反对称,则,由此推得。
根据归一化条件,可推得:
总之,丙二烯双自由基得3个分子轨道及相应得能量分别为:
比较上述两法可见,其难易、繁简程度差别不大,这就是因为丙二烯双自由基分子中得共轭键较小,其久期行列式阶数低,解起来并不困难,但对于一个含较大共轭键得体系,其久期方程复杂,久期行列式阶数高,用通常得方法按部就班地求解很复杂。
在此情况下,要应用对称性概念化简久期方程,分别求解简化了得行列式,结合归一化条件求出原子轨道组合系数,进而求出各分子轨道。
读者可通过C6H6得HMO处理体会用对称性概念与方法处理这类问题得优越性。
(2)计算键键级
对于一个,C原子1与2(亦即2与3)间键键级为:
因此,丙二烯双自由基中原子间总键键级为:
【5、14】说明得几何构型与成键情况;
用HMO法求离域键得波函数及离域能。
叠氮离子就是CO2分子得等电子体,呈直线构型,属点群。
中间得N原子以sp杂化轨道分别与两端N原子得轨道叠加形成2个键。
3个N原子得轨道相互叠加形成离域键,轨道相互叠加形成离域键。
成键情况示于下图:
对一个,久期方程为:
方程中与就是分子轨道中原子轨道(p轨道)得组合系数。
欲使组合系数不全为0,则必使得行列式为0,即:
由此得分子轨道为:
相应得能量为。
同法,得另外2个分子轨道及相应得能量:
得2个中得电子得能量为:
按生成定域键计算,电子得总能量为:
所以得离域能为:
【5、15】已知三次甲基甲烷为平面形分子,形成键。
试用HMO法处理,证明中心碳原子与周围3个碳原子间得键键级与为。
列出久期行列式,解得,0,0,,然后再求。
画出分子骨架并给各C原子编号,如图5、15(a)。
图5、15(a)
根据Huckel近似,写出相应于此骨架得久期方程如下:
利用分子得对称性将久期方程化简,求出,代回久期方程,结合归一化条件求出组合系数,进而写出分子轨道。
将,可求出与分子轨道相应得能级。
考虑对镜面Ⅰ与Ⅱ都对称,则有,于就是久期方程可化简为:
令其系数行列式为:
将代入简化得久期方程并结合归一化条件,得:
由此可得分子轨道:
相应得能量为:
考虑镜面Ⅱ反对称,有。
代入久期方程后可推得。
根据归一化条件推得,分子轨道为:
考虑镜面Ⅱ就是对称得,有,代入久期方程后推得。
根据归一化条件,得。
总之,按能级从高到低得顺序排列,得4个分子轨道及其相应得能级为:
能级及电子得分布如图5、15(b)所示。
图5、15(b)
由分子轨道与电子排布情况可计算C原子之间键得键级:
因而,中间C原子与周围3个C原子间键键级之与为:
加上3个键,中心C原子得总成键度为:
这就是C原子理论上得最高成键度(虽然有人主张用根据丙二烯双自由基计算得到得C原子得最大成键度作为C原子得最大成键度,但由于该分子不具代表性,因而仍未被多数人采纳)。
【5、16】某富烯得久期行列式如下,试画出分子骨架,并给碳原子编号。
【5、17】用前线轨道理论分析加反应,说明只有使用催化剂该反应才能顺利进行。
基态CO分子得HOMO与LUMO分别为与,基态H2分子得HOMO与LUMO分别为与。
它们得轮廓图示于图5、17(a)。
图5、17(a)CO与H2得前线轨道轮廓图
由图可见,当CO分子得HOMO与H2分子得LUMO接近时,彼此对称性不匹配;
当CO分子得LUMO与H2分子得HOMO接近时,彼此对称性也不匹配。
因此,尽管在热力学上CO加H2(生成烃或含氧化合物)反应能够进行,但实际上,在非催化条件下,该反应难于发生。
图5、17(b)CO与H2在Ni催化剂上
轨道叠加与电子转移情况
若使用某种过度金属催化剂,则该反应在不太高得温度下即可进行。
以金属Ni为例,Ni原子得d电子转移到H2分子得LUMO上,使之成为有电子得分子轨道,该轨道可与CO分子得LUMO叠加,电子转移到CO分子得LUMO上。
这样,CO加H2反应就可顺利进行。
轨道叠加及电子转移情况示于图5、17(b)中。
Ni原子得d电子向H2分子得LUMO转移得过程即H2分子得吸附、解离而被活化得过程,它就是CO加H2反应得关键中间步骤。
【5、18】用前线轨道理论分析加热或光照条件下,环己烯与丁二烯一起进行加成反应得规律。
环己烯与丁二烯得加成反应与乙烯与丁二烯得加成反应类似。
在基态时,环己烯得型HOMO与丁二烯得型LUMO对称性匹配,而环己烯得型LUMO与丁二烯得型HOMO对称性也匹配。
因此,在加热条件下,两者即可发生加成反应:
前线轨道叠加图示于图5、18中。
图5、18环己烯与丁二烯前线轨道叠加图
在光照条件下,电子被激发,两分子激发态得HOMO与LUMO对称性不再匹配,因而不能发生加成反应(但可发生其她反应)。
5、19用前线轨道理论分析乙烯环加成变为环丁烷得反应条件及轨道叠加情况。
在加热条件下,乙烯分子处在基态,其HOMO与LUMO分别为与。
当一个分子得HOMO与另一个分子得LUMO接近时,对称性不匹配,不能发生环加成反应,如图5、19(a)。
图5、19(a)图5、19(b)
但在光照条件下,部分乙烯分子被激发,电子由轨道跃迁到轨道,此时轨道变为HOMO,与另一乙烯分子得LUMO对称性匹配,可发生环加成反应生成环丁烷,如图5、19(b)。
5、20试用分子轨道对称守恒原理讨论己三烯衍生物电环合反应在光照与加热条件下产物得立体构型。
分子轨道对称守恒原理得基本思想就是,在一步完成得反应中,若反应物得分子轨道与产物得分子轨道对称性一致,则该反应容易进行。
换言之,若整个反应体系从反应物、中间态到产物,分子轨道始终保持某一点群得对称性,则该反应容易进行。
己三烯衍生物电环合为环己二烯衍生物就是一步完成得单分子反应。
若顺旋闭环,则反应自始至终保持着点群对称性;
若对旋闭环,则反应自始至终保持着点群得对称性。
因此,对这两种闭环方式,应分别按轴与镜面对反应物与产物得分子轨道进行分类。
分类情况见轨道能级相关图(图中S与A分别表示对称与反对称)。
在讨论反应条件、关环方式及产物得立体构型时,只需考虑那些参与旧键断裂与新键形成得分子轨道,并且把它们作为一个整体一起考虑。
对产物而言,与间形成得轨道以及与,与间形成得轨道就是反应中所涉及得分子轨道。
根据节面数目得多少,确定反应物与产物分子轨道得能级次序(这就是一种简便得方法,其结果与由计算得到得能级次序一致)。
根据反应物得分子轨道与产物得分子轨道一一对应、相关轨道得对称性相同并且能量相近以及对称性相同得关联线不相交等原则,作出己三烯电环合反应得分子轨道能级相关图,如图5、20所示。
图5、20己三烯电环合反应分子轨道能级相关图
由图可见,在进行顺旋闭环时,反应物得成键轨道与产物得反键轨道相关联,而产物得成键轨道却与反应物得反键轨道相关联,这说明反应物必须处在激发态(即电子由被激发到)才能转化为产物得基态。
因此,顺旋闭环需在光照条件下进行,得到反式产物。
而在对旋闭环时,反应物得成键轨道与产物得成键轨道相关联,反应物处于基态就可直接转化为产物,反应活化能较低,在一般加热条件下即可进行,得到顺式产物。
总之,根据分子轨道对称守恒原理,己三烯衍生物电环合为环己二烯衍生物(有)得反应具有鲜明得立体选择性。
在加热条件下,分子保持镜面对称,进行对旋闭环,得顺式产物。
在光照条件下,分子保持轴对称性,采取顺旋闭环,得反式产物。
5、21试分析下列分子中得成键情况,比较Cl得活泼性,说明理由。
H3CCl;
;
(a)H3CCl:
该分子为CH4分子得衍生物。
同CH4分子一样,C原子也采用杂化轨道成键。
4个杂化轨道分别与3个H原子得1s轨道及Cl原子得3p轨道重叠共形成4个键,分呈四面体构型,属点群。
(b):
该分子为分子得衍生物,其成键情况与C2H4分子得成键情况既有相同之处又有差别。
在C2H3Cl分子中,C原子
(1)得3个杂化轨道分别与两个H原子得1s轨道与C原子
(2)得杂化轨道重叠形成3个键;
C原子
(2)得3个杂化轨道则分别与H原子得1s轨道、Cl原子得3p轨道及C原子
(1)得杂化轨道重叠共形成3个键。
此外,两个C原子与Cl原子得相互平行得p轨道重叠形成离域键。
C2H3Cl分子呈平面构型,属于点群。
得形成使键缩短,Cl得活泼性下降。
(c):
该分子为C2H2分子得衍生物。
其成键情况与C2H2分子得成键情况也既有相同之处又有差别。
在C2HCl分子中,C原子采取sp杂化。
C原子得sp杂化轨道分别与H原子得1s轨道(或Cl原子得3p轨道)及另一个C原子sp杂化轨道共形成两个键。
此外,C原子与Cl原子得p轨道(3个原子各剩2个p轨道)相互重叠形成两个离域键:
与。
分子呈直线构型,属于点群。
两个得形成使C2HCl中键更短,Cl原子得活泼性更低。
根据以上对成键情况得分析,键键长大小次序为:
5、22试分析下列分子中得成键情况,指出键键长大小次序,并说明理由。
在C6H5Cl分子中,一方面,C原子相互间通过杂化轨道重叠形成键,另一方面,一个C原子与一个Cl原子间通过轨道重叠形成键。
此外,6个C原子与Cl原子通过p轨道重叠形成垂直于分子平面得离域键。
由于Cl原子参与形成离域键,因而其活性较低。
在C6H5CH2Cl分子中,苯环上得C原子仍采用杂化轨道与周边原子得相关轨道重叠形成键,而次甲基上得C原子则采用杂化轨道与周边原子得相关轨道重叠形成键。
此外,苯环上得6个C原子相互间通过p轨道重叠形成离域键:
在中性分子中,次甲基上得C原子并不参与形成离域键,但当Cl原子被解离后,该C原子得轨道发生了改组,由杂化轨道改组为杂化轨道,此时它就有条件参加形成离域键。
因此,在[C6H5CH2]+中存在。
由于电子得活动范围扩大了,得能量比得能量低,这就是C6H5CH2Cl分子中得Cl原子比C6H5Cl分子中得Cl原子活性高得另一个原因。
在分子中,苯环上得C原子采用杂化轨道与周边原子得相关轨道重叠形成键,而非苯环上得C原子则采用杂化轨道与周边原子得相关轨道重叠形成键。
这些键与各原子核构成了分子骨架。
在中性分子中,非苯环上得C原子不参与形成离域键,分子中有2个。
但当Cl原子解离后,该C原子形成键所用得杂化轨道由改组为,于就是它就有条件参与共轭,从而在中形成更大得离域键。
这使得分子中得Cl原子更活泼。
在分子中,C原子形成键得情形与上述两分子相似。
非苯环上得C原子也不参与共轭,分子中有3个。
但Cl原子解离后,非苯环上得C原子改用杂化轨道形成键,剩余得p轨道与18个C原子得p轨道重叠,形成更大更稳定得离域键,这使得分子中得Cl原子在这4个分子中最活泼。
综上所述,Cl原子得活泼性次序为:
5、23试比较,与丙酮中键键长大小次序,并说明理由。
三个分子中碳-氧键键长大小次序为:
丙酮
丙酮分子中得碳-氧键为一般双键,键长最长。
CO2分子中除形成键外还形成两个离域键