合格考化学复习有机化学的复习Word格式.docx
《合格考化学复习有机化学的复习Word格式.docx》由会员分享,可在线阅读,更多相关《合格考化学复习有机化学的复习Word格式.docx(15页珍藏版)》请在冰豆网上搜索。
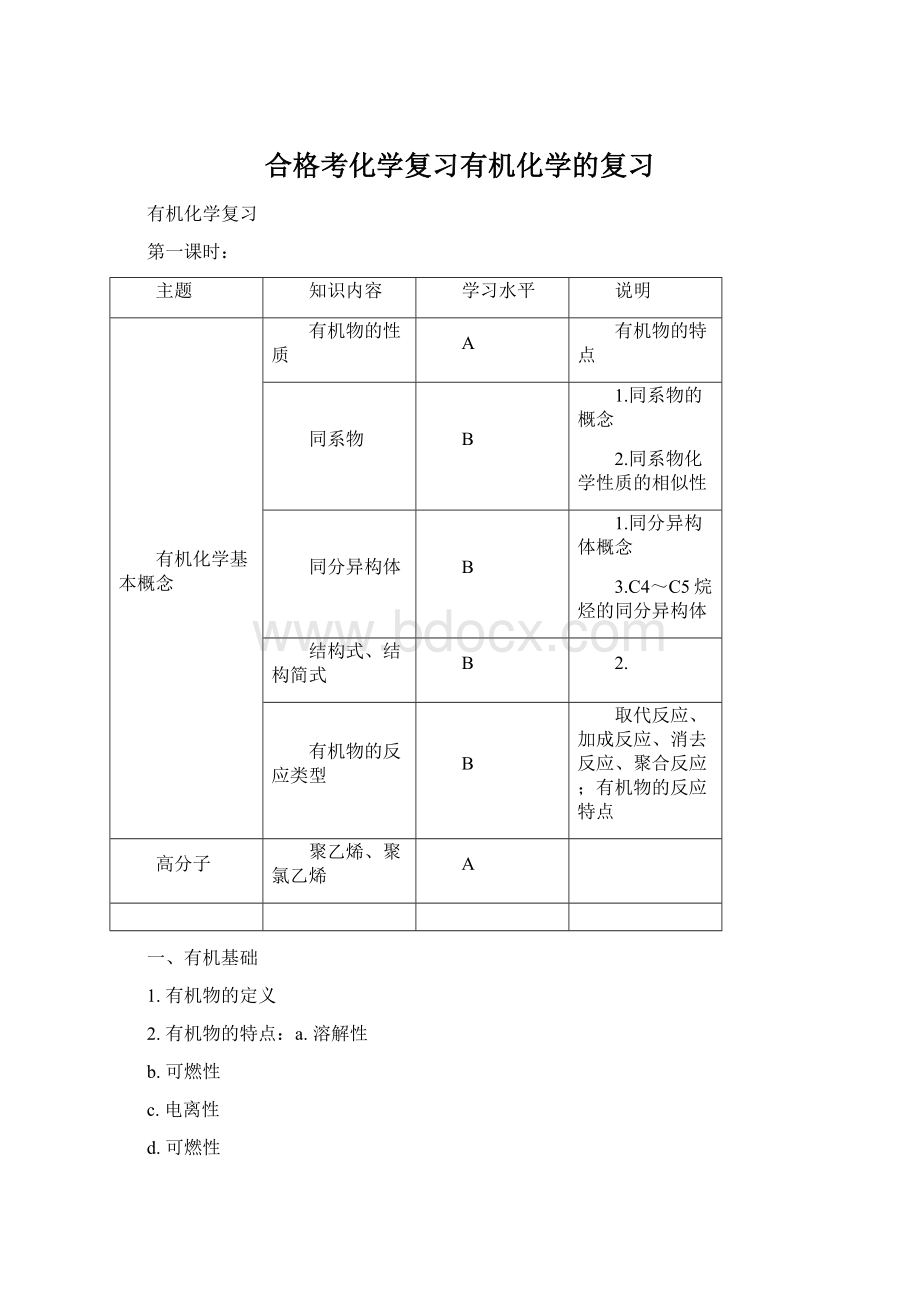
①②H、D、T③S4和S8
35Cl和37Cl
和
*写出C4H10和C5H12的同分异构体并用系统命名法命名之。
C4H10命名:
俗名:
命名:
C5H12命名:
4.结构式、结构简式
写出下列有机物模型的结构式、结构简式及名称:
、、、
5.有机反应类型
⑴取代反应:
实例:
⑵加成反应:
⑶消去反应:
⑷聚合反应:
⑸酯化反应:
⑹氧化反应:
⑺还原反应:
*判断下列生产或生活中涉及的有机反应属于哪种反应类型:
(1)工业上以乙烯为原料制备乙醇
(2)工业上以乙醇为原料生产乙醛
(3)实验室以乙醇为原料制备乙烯
(4)工业上用氯乙烯制备聚氯乙烯
(5)工业上用乙酸、乙醇制备乙酸乙酯
(6)苯和氢气在一定条件下反应生成环己烷
第二课时:
二、烃
甲烷和烷烃
甲烷的分子结构
正四面体结构及空间对称性
甲烷的物理性质
甲烷的化学性质
1.甲烷和氧气、氯气的反应
2.甲烷的分解反应及其产物的用途
烷烃
烷基、通式、命名、同分异构体、同系物、结构式和结构简式
乙烯
乙烯的分子结构
碳碳双键官能团、双键的不饱和性
乙烯的物理性质
乙烯的化学性质
1.官能团与化学性质的关系
2.乙烯的加成反应(氢气、溴水、氯化氢、水)、加聚反应
乙烯的实验室制法
反应原理和反应装置
乙烯的用途
乙炔
乙炔的分子结构
碳碳叁键官能团、叁键的不饱和性
乙炔的物理性质
乙炔的化学性质
2.乙炔与氢气、溴水、氯化氢的加成反应
3.乙炔加成产物氯乙烯的性质
乙炔的实验室制法
苯
苯的结构
苯分子中碳碳键的特殊性
苯的物理性质
苯的化学性质
苯与液溴的取代反应、硝化反应、与氢气的加成反应
有机化工和矿物原料
石油
1.石油的成分
2.石油的分馏和裂化
煤
煤的干馏及其产物
天然气
天然气的主要成分及其用途
1.烃的结构特点
物质
分子式
结构式
结构简式
电子式
空间结构
成键特点
甲烷
乙烷
2.烃的主要化学性质
主要反应(写出反应方程式)
鉴别
1取代(与氯气):
;
现象:
2氧化(燃烧):
现象:
③分解(制炭黑):
使溴水和酸性KMnO4溶液褪色
①加成
与溴水:
与氢气:
与氯化氢:
与水:
②聚合
3氧化(燃烧):
1加成
(1:
1)
(1:
2)
氯乙烯加聚:
②氧化(燃烧)
1取代反应
与液溴(卤代)
反应装置中的现象:
与硝酸(硝化)
②加成(与H2)
③氧化(燃烧)
使溴水
和酸性KMnO4溶液褪色
3.苯
(1)苯的来源——我们可以通过的方法,分离出煤焦油中的苯及其同系物。
(2)苯的物理性质:
苯是色、气味的毒体,溶于水,密度比水,熔点为5.5℃,沸点80.1℃,易。
(3)苯的用途:
_____________________________________________________________
(4)苯的结构:
苯之所以是一种特殊的碳氢化合物,在于苯分子中六根碳键,是一种共价键。
4.烷烃
(一)通式:
(二)性质递变规律
(1)烷烃均为色,常温下随着碳原子数的由气态递变到液态再到固态。
(2)随着碳原子数的增多,熔、沸点,密度比水。
(3)烷烃都溶于水,溶于有机溶剂。
5.煤和石油以及天然气的利用
(1)石油的成分
(2)石油的分馏
温度计的位置,分离状态的混合物
(3)石油的裂化
(4)煤的成分
(5)煤的综合利用包括
(6)煤的干馏是指
(7)天然气的主要成分,用途为
【练习】
1.下列物质属于纯净物的是()
A.甲烷与氯气在光照下取代的有机产物B.铝热剂C.明矾D.汽油
2.下列有关有机化合物的说法中正确的是(
)
A.含有碳元素的化合物都是有机化合物
B.所有的有机化合物均难溶解于水,易溶于有机溶剂
C.易溶解于汽油、苯、四氯化碳的物质就是有机化合物
D.有机物组成元素较少,而有机物的种类繁多
3.某有机物在空气中完全燃烧只生成二氧化碳和水,则此有机物
(
)
A.一定含有氧元素
B.一定含有碳、氢、氧三种元素
C.一定不含有氧元素
D.一定含有碳、氢两种元素,不能确定是否含有氧元素
4.下列混和气中主要成分不是甲烷的是(
A.液化石油气
B.沼气
C.天然气
D.瓦斯气
5.下列叙述中错误的是(
A.煤矿的矿井要注意通风和严禁烟火,以防爆炸事故的发生
B.甲烷燃烧能放出大量的热,所以是一种很好的气体燃料
C.点燃甲烷不必像点燃氢气那样事先验纯
D.如果隔绝空气,将甲烷加热到1000℃以上,甲烷分解生成炭黑和氢气
6.下列可证明甲烷分子是正四面体结构的是()
A.一氯甲烷没有同分异构体
B.二氯甲烷没有同分异构体
C.甲烷分子的四个键完全相同
D.甲烷分子的四个键完全不相同
7.某烷烃含有200个氢原子,那么该烃的分子式是(
)
A.C97H200
B.C98H200
C.C99H200
D.C100H200
8.工业上大量获得乙烯的方法是()
A.煤的干馏
B.石油分馏
C.石油裂化
D.石油裂解
9.通常用来衡量一个国家石油化工发展水平标志的是(
A.甲烷的产量
B.乙烯的产量
C.乙醇的产量
D.石油的产量
10.把煤隔绝空气加强热,不能得到下列物质中的()
A.焦炭
B.水煤气C.煤焦油
D.焦炉气
11.能证明乙烯分子里含有一个碳碳双键的事实是
(
A.乙烯分子里碳氢原子个数比为1:
2
B.乙烯完全燃烧生成的CO2和H2O的物质的量相等
C.乙烯容易与溴水发生加成反应,且1mol乙烯完全加成消耗1mol溴单质
D.乙烯能使酸性KMnO4溶液褪色
12.甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,最好依次通过盛下列哪组试剂的洗气瓶( )
A.澄清石灰水、浓硫酸B.酸性高锰酸钾溶液、浓硫酸
C.浓溴水、浓硫酸D.浓硫酸、酸性高锰酸钾
13.将苯加入溴水中,充分振荡、静置后溴水层颜色变浅,是因为发生了()
A.加成反应B.萃取过程C.取代反应D.氧化反应
14.加成反应是有机化学中的一类重要的反应,下列属于加成反应的是(
)
A.甲烷与氯气混和后光照反应
B.乙炔与溴的四氯化碳溶液反应
C.乙烯使酸性高锰酸钾溶液的褪色
D.乙烯在空气中燃烧
15.下列物质中,能使酸性高锰酸钾溶液褪色的是()
①溴苯②二氧化硫③C6H14④电石气⑤异丁烷⑥CH2=CH-CH3
A.①②④B.②④⑤C.②④⑥D.①③⑤
16.下列关于苯的性质的叙述中,不正确的是()
A.苯是无色带有特殊气味的液
体
B.常温下苯是一种不溶于水且密度小于水的液体
C.苯在一定条件下能与溴发生取代反应
D.苯不具有典型的双键所应具有的加成反应,故不可能发生加成反应
17.有a升乙烯和乙炔的混合气,与氢气充分反应,消耗氢气1.25a升,则混合气体中乙烯、乙炔的体积比为()
A.1∶1B.4∶1C.2∶1D.3∶1
18.两种气态烃组成的混合气体0.1mol,完全燃烧得0.16molCO2和3.6g水,下列说法中正确的是()
A.一定有乙烯B.一定有甲烷C.可能有乙烯D.可能有甲烷
第三课时:
三、烃的含氧衍生物
乙醇
乙醇的分子结构
羟基及其性质
乙醇的物理性质
乙醇的化学性质
乙醇的工业制法及用途
粮食发酵法和乙烯水化法
乙醛
乙醛的分子结构
醛基及其性质
乙醛的物理性质
乙醛的化学性质
乙酸
乙酸的分子结构
羧基及其性质
乙酸的物理性质
乙酸的化学性质
乙酸的酯化反应
物质名称
官能团符号和名称
甲醛
(一)乙醇
1.乙烷分子中的一个氢原子被___________取代后的产物即为乙醇,俗称__________。
我们把这种____________________________________成为烃的衍生物。
2.乙醇是________色、有______________味的液体,密度于水。
乙醇的水溶性是________________,为得到高浓度乙醇可采用的方法。
3.工业上制取乙醇的方法有和两种,其中具有成本低、产量大、节约大量粮食的生产方法的化学反应方程式为,制饮料酒应用__________法,而不可用工业酒精为原料,这是因为工业酒精中含有有毒的。
4.实验室中,点燃酒精灯发生的反应是_____________________________,酒精灯不使用时,必须盖好灯帽的原因是_______________。
乙醇是一种_______(“一次”或“二次”)能源,用乙醇作燃料的优点是_______________________,_________________________
5.写出以下方程式:
(1)乙醇和浓硫酸共热,可以生成乙烯___________________________________________
(2)
乙醇催化氧化的方程式:
6.羟基的符号是()
A.OHB.OH―C.-OHD.
7.将铜丝放在酒精灯火焰上加热后,分别再将其放入下列溶液中,取出洗涤、干燥后,质量没有变化的是(
)
A.水
B.乙醇
C.醋酸
D.硫酸
8.能证明乙醇分子中含有一个羟基的事实是(
A.乙醇完全燃烧生成水
B.0.1mol乙醇与足量金属钠反应生成0.05molH2
C.乙醇能与水以任意比例互溶
D.乙醇容易挥发
9.乙醇分子中不同的化学键,如右图:
关于乙醇在各种反应中断裂键的说法不正确的是(
A.乙醇和钠反应,键①断裂
B.乙醇制乙烯时键②③断裂
C.乙醇发生酯化反应时键①断裂
D.在铜催化下和O2反应,键①③断裂
(二)甲醛和乙醛
1.甲醛又叫,是一种色气味的体,密度,
溶于水。
福尔马林指的是。
2.甲醛的水溶液是一种良好的杀菌剂,下列关于甲醛用途的叙述中不正确的是()
A.用35%~40%的甲醛溶液浸制生物标本
B.用甲醛的稀溶液来给种子消毒
C.用含有甲醛的化学物质做漂白剂,加工快餐面、牛百叶等食品
D.用甲醛生成的甲醛树脂作胶合板黏合剂
3.乙醛是色气味的体,沸点较,密度比水,挥发,燃烧,能跟水、乙醇、氯仿等。
4.下列有机物,常温下为气态的是()
A.CH3CHOB.CH3CH2OHC.HCHOD.C6H6
5.下列试剂中可用于检验有机物中是否含有醛基的是()
A.银氨溶液B.新制的氢氧化钠溶液C.酚酞溶液D.石蕊试液
6.乙醛的化学性质与甲醛相似,试写出有关乙醛的化学反应方程式,并注明反应类型。
(1)乙醛与氢气的反应 _______________________________________,____________
(2)乙醛与新制氢氧化铜悬浊液的反应______________________________,__________;
(3)乙醛在氧气中燃烧_____________________________________,_________________。
(三)乙酸
1.乙酸是一种色有气味的体,熔点16.6℃,易,低于16.6℃就凝结成冰状晶体,所以无水乙酸称为。
乙酸溶于水和酒精。
2.乙醇和乙酸发生反应生成乙酸乙酯,乙酸乙酯是一种具有味,密度比水,溶于水,溶于有机溶剂。
可做也可做溶剂。
3.下列物质中,属于纯净物的是()
A.食醋
B.固体酒精
C.福尔马林
D.冰醋酸
4.下列各组混合液,静置后不能用分液漏斗分离的是()
A.乙醇和苯B.苯和水C.硝基苯和水D.四氯化碳和水
5.用一种试剂可以区分乙醇和乙酸的是(
A.氢氧化钠溶液
B.氨水C.碳酸钠溶液
D.银氨溶液
6.下列关于乙酸的叙述中,不正确的是
)
A.乙酸是具有强烈的刺激性气味的的液体B.冰醋酸是混合物
C.乙酸和水、乙醇能互相混溶D.乙酸和乙醇的酯化反应也是取代反应
7.除去乙酸乙酯中含有的乙酸,最好的处理操作是(
A.蒸馏
B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液
D.用过量氢氧化钠溶液洗涤后分液
8.可以用分液漏斗分离的一组混合物是(
A.溴苯与苯
B.乙酸乙酯与乙醇
C.乙酸与水
D.乙酸乙酯与水
9.下列是有关生活中对醋酸的应用,其中主要利用了醋酸酸性的是(
A.醋酸溶液可一定程度上治疗手足癣
B.熏醋可一定程度上防止流行性感冒
C.醋可以除去水壶上的水垢
D.用醋烹饪鱼,除去鱼的腥味
10.酯化反应是有机化学中的一类重要反应,下列对酯化反应理解不正确的是
A.酯化反应中醇脱去了羟基
B.酯化反应也可能会有副反应
C.酯化反应是有限度的
D.酯化反应一般需要催化剂
第四课时:
四、烃与烃的含氧衍生物的相互转化
写出各转化的化学方程式。
①反应类型
②反应类型
③反应类型
④反应类型
⑤反应类型
⑥反应类型
⑦反应类型
⑧反应类型
⑨反应类型
⑩反应类型
五、有机物的计算
1、某气态烃含C85.7%,含H14.3%,在标准状况下的密度是2.5g/L。
该烃能使酸性高锰酸钾溶液或溴水褪色。
求该烃的分子式,并写出它的能使酸性高锰酸钾溶液褪色的各种同分异构体的结构简式。
2、在标准状况下体积为112毫升的某烃完全燃烧后生成CO2,和水蒸汽的物质的量之比为3︰4,把燃烧产物通过碱石灰,碱石灰质量增加1.02克,求该烃的分子式。
3、某气态有机物A,其密度是相同状况下H2密度的22倍,燃烧0.05molA能生成3.36L二氧化碳(S.T.P)和3.6g水,写出该有机物的分子式和结构简式。
4、现有0.1mol有机物A,其质量为4.6g,将4.6gA完全燃烧需要标准状况下氧气1.12L,产生的二氧化碳和水的物质的量相等。
试根据计算推断有机物A的分子式,并写出其可能的结构简式。
5、在标准状况下,把5L甲烷和乙烯的混合气体通入足量的溴水里,反应后,溴水质量增加2.8g,求剩余的气体有多少升?
混合气体中乙烯所占的质量百分比是多少?
将5L混合气体加入足量氧气使其完全燃烧,需消耗多少升氧气(标准状况)?