山东省日照市岚山区中考三模化学试题 答案和解析Word下载.docx
《山东省日照市岚山区中考三模化学试题 答案和解析Word下载.docx》由会员分享,可在线阅读,更多相关《山东省日照市岚山区中考三模化学试题 答案和解析Word下载.docx(16页珍藏版)》请在冰豆网上搜索。
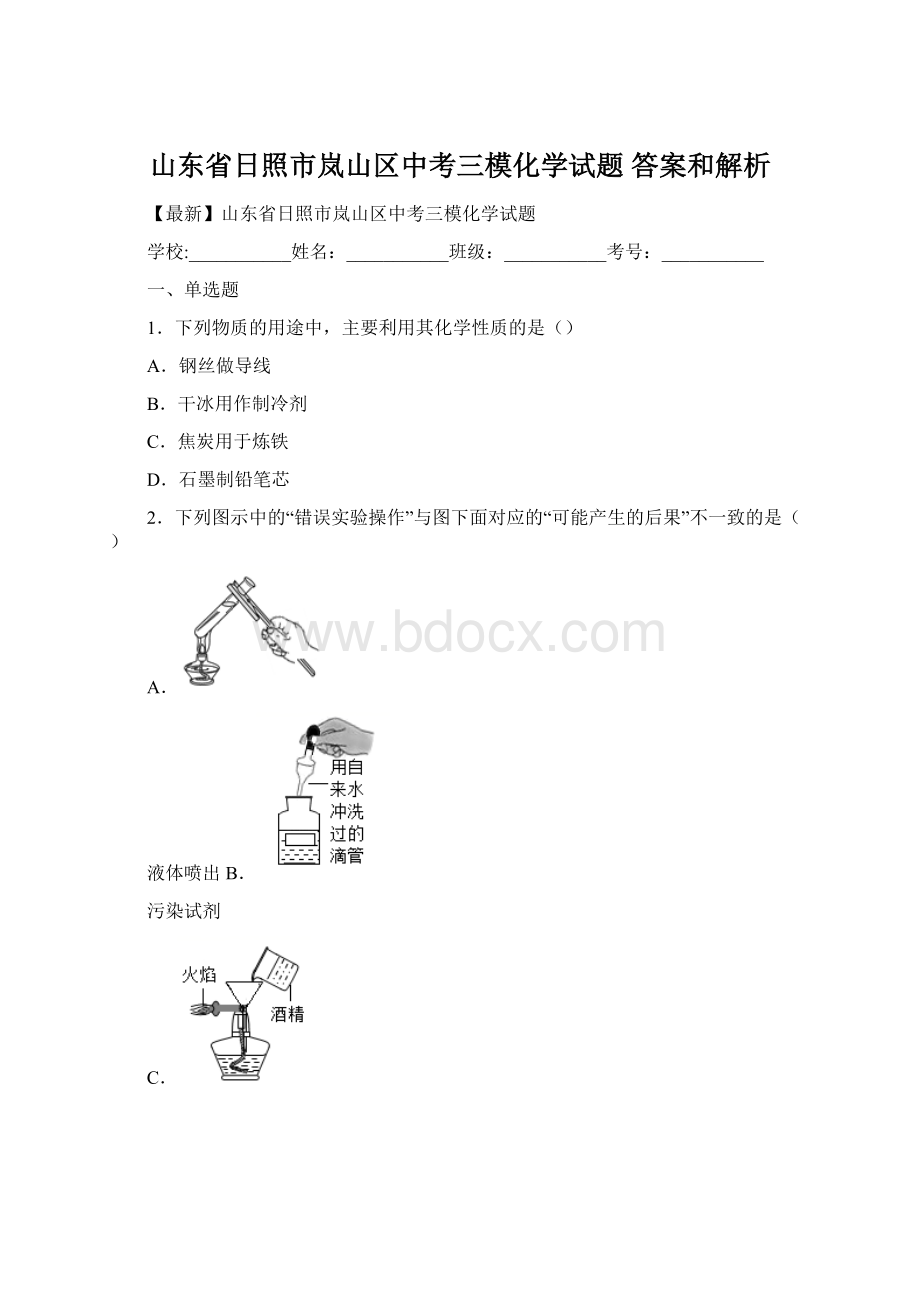
B.原子
C.元素
D.分子
5.以下说法中正确的是( )
A.有机物中都含碳元素,所以含碳元素的化合物都是有机物
B.在氯化钠溶液中有自由移动的钠离子和氯离子,所以氯化钠溶液能导电
C.单质是由同种元素组成的,所以只含一种元素的物质一定是单质
D.在化合物里,正负化合价的代数和为零,所以在同一化合物中金属元素显正价,则非金属元素一定显负价
6.如图是某化学反应的微观示意图,其中不同的圆球代表不同原子,下列说法中正确的是()
A.该反应涉及到四种原子
B.该反应属于置换反应
C.反应后生成三种物质
D.参加反应的两种分子的个数比为1:
1
7.高铁酸钾(K2FeO4)是一种集吸附、凝聚、杀菌等功能为一体的新型高效水处理剂,可将水中的三氯乙烯(C2HCl3)除去85.6%,下列说法正确的是( )
中三种元素的质量比是2:
1:
4
B.
中Fe元素的化合价为
价
中氯元素的质量分数最大
D.
是由2个碳原子、1个氢原子和3个氯原子构成的
8.科学合理地使用燃料,可有效地防治环境污染。
下列关于燃料与燃烧的说法错误的是( )
A.石油分解后可得到汽油、煤油、柴油等一系列产品
B.把煤加工成蜂窝煤可使之燃烧更加充分
C.天然气是比煤、石油更加清洁的化石燃料
D.汽油中加入适量的乙醇可减少汽车尾气的污染
9.下列关于金属材料的说法不正确的是( )
A.用稀盐酸可以鉴别黄金和黄铜(铜锌合金)
B.铁在干燥的空气中容易生锈
C.硬铝(铝合金)的硬度大于纯铝
D.金属资源的回收利用既保护了环境,又节约了金属资源
10.装有50g稀硫酸的小烧杯中,不断慢慢滴加10%的Ba(OH)2溶液至过量。
有关量的变化情况见图(横坐标表示氢氧化钡溶液的质量,纵坐标表示小烧杯中量的变化)。
其中肯定不正确的是( )
B.
D.
11.归纳总结是学习化学的基本方法。
下面是某同学整理的部分化学知识,你认为都正确的选项是()
A.物质的性质决定用途
B.物质的鉴别
①浓硫酸具有吸水性——常用于干燥气体
②CO具有可燃性——常用于炼铁
①可用石蕊试液鉴别CO和CO2
②可用肥皂水区分硬水和软水
C.物质的构成
D.化学符号的意义
①分子、原子、离子都可以直接构成物质
②构成原子的微粒都不带电荷
①O2:
两个氧原子
②O2—:
一个氧离子带两个单位负电荷
A.AB.BC.CD.D
12.有18.6g的NaOH和Na2CO3固体混合物,已知Na元素与C元素的质量比是23:
3,把该固体全部加入到盛有100g的足量稀硫酸的烧杯中,充分反应后,烧杯里残留物质的质量是114.2g。
则原NaOH和Na2CO3固体混合物中钠元素的质量是()
A.9.2gB.6.9gC.4.6gD.2.3g
二、填空题
13.下表为元素周期表中部分元素的相关信息,利用下表回答相关问题。
(1)请画出16号元素原子结构示意图______________,化学反应中该原子比较容易________(选填“得到”或“失去”)电子变成离子;
(2)
表示的是_____________(填化学符号);
(3)仔细观察上表,我们能发现很多规律:
①同周期(同一横行)元素的原子核外__________数相同,_____________数从左到右依次递增;
②同族(同一纵行)元素的原子核外___________数相同,______________数从上到下依次递增。
14.生活中处处有化学,化学与生活密切相关。
(1)成语“釜底抽薪”运用的灭火原理是_____________。
(2)CO2常用于灭火,但镁着火不能用CO2灭火,原因是镁能在CO2中燃烧生成一种黑色固体,请写出该置换反应的化学方程式:
_______________。
(3)某饼干包装袋中用作干燥剂的是生石灰(CaO),这是利用了生石灰能与水反应的性质,请写出该反应的化学方程式:
______________。
(4)甲醛(CH3OH)有毒,误饮可使眼镜失明,甚至死亡,最新研究证明,用氨气(NH3)处理含有甲醛的工业废水,可使其转变成无毒的物质,有关反应的化学方程式为
,则X的化学式为__________。
(5)科学家在1527℃的高温下用激光器合成了一种新型物质(化学式为CO2),该物质与金刚石结构相似,下列有关该新型物质的说法正确的是__________(填序号)。
A它是一种超硬物质
B构成它的基本粒子是原子
C它在常温下为气态
D构成它的基本粒子是分子
15.如图是A,B,C三种固体物质的溶解度曲线,请回答下列问题:
(1)t2℃时,A物质的溶解度为_________
(2)三种物质中___________
(3)t1℃时,将20g物质投C入到50g水中,得到物质C的___________
(4)若B点混有少量A时,可采用______________
(5)将t1℃时A,B,C三种固体物质的饱和溶液升温到t2℃,其溶质的质量分数由大到小的顺序是_____________
三、推断题
16.已知A、B、C、D、E分别是初中化学常见的五种不同类别的物质,其中B的固体和E的浓溶液常用作实验室的干燥剂,F是一种红色物质,它们之间存在如图所示的关系(图中“一”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,部分物质和反应条件未标出)请回答下列问题:
(1)写出B的化学式:
__________
(2)若D→C的转化属于化合反应,请写出该反应的化学方程式:
_____________
(3)请写出B和E的反应的化学方程式_________
四、实验题
17.下图是实验室制取气体的的常用实验装置,请根据所学的知识回答下列问题。
(1)写出编号①所指仪器的名称:
(2)写出利用A装置制取氧气的化学方程式_____________
(3)若用过氧化氢溶液制取一瓶干燥的氧气,需要用到装置F,装置F中应装入_____________
五、流程题
18.氯碱工业以粗盐(主要成分是NaC1,含少量泥沙、CaC12、MgC12)为原料,生产氯气和氢氧化钠,模拟流程如下:
(1)试剂A与试剂B的组合为____________
①KOH②NaOH③K2CO4④Na2CO3
(2)操作A是_____________;
该操作需使用玻璃棒,其作用是______;
(3)流程中Mg元素必须转化成_____________
(4)写出电解NaCl溶液的化学方程式__________
(5)该工业副产品H2目前还不能作为燃料被广泛应用,其理由_____________
六、计算题
19.某课外兴趣小组对一批大理石样品(含有杂质,杂质不溶于水,也不与稀盐酸反应)进行分析,甲、乙、丙三位同学分别进行实验,烧杯的质量为75.4g,其中只有一位同学所取用盐酸与大理石恰好完全反应,实验数据如下:
甲
乙
丙
烧杯+稀盐酸
230.8g
180.8g
加入的大理石样品
20g
25g
充分反应后,烧杯+剩余物
246.4g
196.4g
201.4g
请你认真分析数据,回答下列问题:
(1)同学所取用的稀盐酸与大理石样品恰好完全反应;
(2)计算恰好完全反应后所的溶液中溶质的质量分数。
(写出具体计算过程)
参考答案
1.C
【详解】
A、铜作电线,是利用了铜的导电性,不需要通过化学变化就能表现出来,属于物理性质,故A错误;
B、干冰用作人工降雨,是利用了干冰升华时吸热的性质,不需要发生化学变化就能表现出来,是利用了其物理性质,故B错误;
C、碳用来冶炼金属,是利用了碳的还原性,需要通过化学变化才表现出来,是利用了其化学性质,故C正确;
D、用石墨做铅笔芯写字利用了石墨的硬度小,属于物理性质,故D错误。
故选C。
2.C
A、给试管里的液体加热时,试管内液体超过试管容积的1/3,会导致液体沸腾喷出伤人,故A正确;
B、使用胶头滴管时,用自来水冲洗,会使滴管沾有自来水,自来水中含有一些可溶性杂质,所以能污染试剂,故B正确;
C、使用酒精灯时,绝对禁止向燃着的酒精灯内添加酒精,防止发生火灾,故C错误;
D、用量筒量液读数时,视线偏高(俯视)会导致读数偏大;
故D正确;
3.D
A、二氧化碳不具有可燃性,不能做燃料,故选项不符合题意;
B、一氧化碳不能与水化合,故选项不符合题意;
C、一氧化碳和二氧化碳的分子构成不同,故选项不符合题意;
D、一氧化碳和二氧化碳在一定条件下能相互转化,故选项符合题意
4.C
物质是由元素组成的,“铁”和“钙”是指元素;
5.B
A、有机物中都含有碳元素,但含碳元素的化合物不一定都是有机物。
例如,一氧化碳、二氧化碳、碳酸钙等虽含有碳元素,由于其性质与无机物相似,故把它们归到无机物,此选项错误;
B、氯化钠溶于水时,在水分子作用下,解离出能自由移动的钠离子和氯离子,所以氯化钠溶液能导电,此选项正确;
C、单质是由同种元素组成的,但是由同种元素组成的物质不一定是单质,如氧气和臭氧组成的混合物中只含有一种元素,此选项错误;
D、在同一化合物中金属元素显正价,则非金属元素不一定显负价,如氢氧化钠中氢元素呈+1价,此选项错误。
故选B。
6.D
【分析】
根据反应的微观示意图,该反应为一种化合物的2个分子与另一种化合物的2个分子发生反应,生成一种单质的1个分子和一种化合物的2个分子,其中有一个化合物的分子没有参加反应。
A、根据反应微观示意图中分子结构图,该反应中只涉及到三种原子而非四种原子,故不正确;
B、该反应的反应物中没有出现同种原子构成的单质分子,因此,该反应一定不属于置换反应,故不正确;
C、根据反应微观示意图中分子结构图,该反应生成两种物质,故不正确;
D、由于微观示意图中有一个分子未参加反应,因此可判断参加反应的两种分子的个数比为2:
2=1:
1,故正确。
故选D。
7.C
A、K2FeO4中钾、铁、氧三种元素的质量比=(39×
2):
56:
(16×
4)≠2:
4,故A错误;
B、根据化合物中各元素正负化合价的代数和为零,设:
铁元素的化合价为x,则有:
(+1)×
2+x+(-2)×
4=0,解得x=+6,故B错误;
C、C2HCl3中碳、氢、氯三种元素质量比=(12×
(35.5×
3)=24:
106.5,可见其中氯元素的质量分数最大,故C正确;
D、C2HCl3是由分子构成的,不是由原子直接构成的,1个C2HCl3分子是由2个碳原子、1个氢原子和3个氯原子构成的,故D错误。
【点睛】
在比较物质中元素质量分数大小时,不一定将每种元素的质量分数都计算出来,可通过元素的质量比的大小进行比较。
8.A
A、石油分馏后可得到汽油。
煤油。
柴油等一系列产品;
从石油里提炼柴油、汽油、煤油的过程叫石油分馏,属于物理变化。
因为它是根据不同的烯烃的沸点不同,然后蒸馏让它们分离开来。
而不是分解,分解属于化学变化;
B、把煤加工成蜂窝煤,增大了煤与氧气的接触面积,故可使之燃烧更加充分;
C、由于天然气主要成分是甲烷,燃烧产物是二氧化碳和水,而煤、石油中含有硫、磷等物质,故天然气是比煤、石油更加清洁的化石燃料;
D、汽油中加入适量的乙醇,因为乙醇燃烧后的产物是二氧化碳和水,故可减少汽车尾气的污染。
故选A。
解答时需要综合考虑试题所涉及的信息,借助排除法即可选出正确的答案.
9.B
【解析】
A、金的活动性比氢弱,故黄金不与酸反应,黄铜中的锌可以与酸反应冒出气泡,故可以用酸鉴别,故正确;
B、铁生锈的条件是与空气和水同时接触,故干燥的空气中铁不易生锈,故错误;
C、合金的硬度比组成金属的硬度大,故硬铝(铝合金)的硬度大于纯铝,故正确;
D、金属资源的回收利用既保护了环境,又节约了金属资源,正确。
10.B
A、沉淀随Ba(OH)2溶液的加入逐渐变大,稀硫酸反应完后不再增加,选项A正确;
B、稀硫酸和氢氧化钡反应生成水,氢氧化钡溶液中也含水,随着氢氧化钡溶液的加入,即使反应结束水的质量也应该不断增加,选项B不正确;
C、溶液的pH随Ba(OH)2溶液的加入逐渐变大,选项C正确;
D、硫酸与Ba(OH)2溶液反应生成沉淀,溶质质量分数变小,恰好反应时为零,Ba(OH)2溶液过量后溶质质量分数变大,选项D正确。
11.B
试题分析:
A中一氧化碳具有可燃性,故可做燃料,A错误;
B中二氧化碳与水反应生成碳酸能使紫色的石蕊试液变成红色,一氧化碳不能,B正确;
C中构成原子的原子核带正电,核外电子带负电,C错误;
D中O2:
表示的是一个氧分子中含有两个氧原子,D错误。
考点:
物质的性质与用途,物质的鉴别,物质的构成,化学符号的意义
12.A
根据已知,生成二氧化碳的质量为:
18.6g+100g﹣114.2g=4.4g,二氧化碳中碳元素的质量为:
4.4g×
(
×
100%)=1.2g,已知钠元素与碳元素的质量比为23:
3,则钠元素的质量为:
1.2g×
=9.2g。
质量守恒定律及其应用;
化合物中某元素的质量计算
13.
得到Al3+电子层最外层电子最外层电子电子层
(1)16号元素是硫元素,根据原子结构示意图的画法画出硫原子的结构示意图为
,最外层有6个电子,易得到两个成为8电子稳定结构;
(2)该粒子的核内有13个质子,核外有10个电子,是带有三个单位正电荷的铝离子--Al3+;
(3)根据元素周期表得规律:
①同周期(同一横行)元素的原子核外电子层数相同,最外层电子数从左到右依次递增;
②同族(同一纵行)元素的原子核外最外层电子数相同,电子层数从上到下依次递增。
14.隔离可燃物
N2AD
(1)灭火的原理:
隔离可燃物、隔绝空气(或氧气)、降低温度至可燃物的着火点一下,满足任一条件即可灭火,“釜底抽薪”运用的灭火原理是隔离可燃物;
(2)在点燃的条件下,镁与二氧化碳发生置换反应生成氧化镁和碳,该反应的化学方程式为
;
(3)氧化钙与水反应生成氢氧化钙,化学方程式为CaO+H2O=Ca(OH)2;
(4)由
可知,反应前含有5个C原子,38个H原子,29个O原子,6个N原子,反应后含有5个C原子,38个H原子,29个O原子,3个X,故X中含有2个氮原子,其化学式为N2;
(5)A.该物质与金刚石结构相似,金刚石的硬很大,则它是一种超硬物质,故选项说法正确;
B.该物质(化学式为CO2),则构成它的粒子是分子,故选项说法错误;
C.该物质与金刚石结构相似,金刚石在常温下为固体,则该物质在常温下也为固体,故选项说法错误;
D.该物质(化学式为CO2),构成它的粒子是分子,故选项说法正确;
故选:
AD。
15.30t2℃时A和C的溶解度相等C饱和70g蒸发结晶B>A>C
(1)根据溶解度曲线可知,t2℃时,A物质的溶解度为30g;
P点的含义是t2℃时A和C的溶解度相等;
(2)气体的溶解度随着温度升高而减小,三种物质中C的溶解度随温度变化趋势与气体溶解度的变化相似;
(3)t1℃时C的溶解度是40g,将20g物质投C入到50g水中,C恰好完全溶解,得到物质C的饱和溶液,此时溶液的质量是70g;
(4)A的溶解度受温度变化影响较大,B的溶解度受温度变化影响较小,若B点混有少量A时,可采用蒸发结晶的方法提纯B;
(5)将t1℃时A、B、C三种固体物质的饱和溶液升温到t2℃,A、B都变成不饱和溶液,C仍然是饱和溶液,由于t1℃时B的溶解度大于A,因此B的质量分数大于A,由于C在t2℃时的溶解度大于A在t1℃时的溶解度,因此C的质量分数大于A,其溶质的质量分数由大到小的顺序是B>C>A。
16.NaOH
复分解反应
B的固体和E的浓溶液常用作实验室的干燥剂,所以B是氢氧化钠,E是硫酸,A和氢氧化钠可以相互转化,所以A是碳酸钠,氢氧化钠、硫酸都会转化成C,所以C是水,硫酸会转化成D,D和水可以相互转化,所以D是氢气,F会转化成水,会与氢气反应,F是一种红色物质,所以F可以是氧化铁,经过验证,推断正确。
(1)由分析可知,B是氢氧化钠,化学式是NaOH;
(2)若D→C的转化属于化合反应,该反应是氢气和氧气在点燃的条件下生成水,化学方程式为:
(3)B和E的反应是硫酸和氢氧化钠反应生成硫酸钠和水,化学方程式为:
H2SO4+2NaOH=Na2SO4+2H2O,该反应是两种化合物交换成分生成另外两种化合物的反应,属于复分解反应。
17.长颈漏斗
BD浓硫酸f→g→d
(1)由图可知,仪器①的名称是:
长颈漏斗;
(2)A装置适用于固体加热反应制取氧气,且试管口有一团棉花,故是加热高锰酸钾制取氧气,高锰酸钾受热分解为锰酸钾、二氧化锰和氧气,该反应的化学方程式为:
实验室通常用石灰石和稀盐酸反应制取二氧化碳,该反应属于固液不加热反应,发生装置应选B,二氧化碳溶于水,密度比空气大,应用向上排空气法收集,故收集装置选D,故填:
BD;
(3)浓硫酸具有吸水性,且不与氧气反应,故可用浓硫酸干燥氧气,故装置F中应装入浓硫酸;
若用过氧化氢溶液制取一瓶干燥的氧气,可用盛有浓硫酸的F装置干燥,洗气应“长进短出”,氧气不易溶于水,密度比空气大,可用排水法或向上排空气法收集,要想得到干燥的氧气,可用向上排空气法收集,故收集装置选D,故整个实验中正确的接口顺序为b→f→g→d。
18.②④过滤引流Mg(OH)2
H2不易储存和运输或生产H2的成本高
(1)试剂A与试剂B的组合为氢氧化钠、碳酸钠,分别除去氯化镁、氯化钙;
(2)操作A将固体和液体分开,所以为过滤,过程中需使用玻璃棒,玻璃棒的作用是引流;
(3)流程中Mg元素必须转化为Mg(OH)2才能完全除去;
(4)电解NaCl溶液生成氢氧化钠、氯气和氢气,反应的化学方程式:
(5)该工业副产品H2目前还不能作为燃料被广泛应用,其理由是不易储存、不安全、制取价格较高等。
19.
(1)乙;
(2)设样品中碳酸钙的质量为x,生成的氯化钙的质量为y,
x=10g,
y=11.1g,
恰好完全反应后所的溶液中溶质的质量分数=
100%=10%;
答:
恰好完全反应后所的溶液中溶质的质量分数10%。
(1)由表中数据可知,甲同学实验得到二氧化碳的质量为:
230.8g+20g-246.4g=4.4g;
乙同学实验得到二氧化碳的质量为:
180.8g+20g-196.4g=4.4g;
丙同学实验得到二氧化碳的质量为:
180.8g+25g-201.4g=4.4g,故所用样品最少的同学所取用的稀盐酸与大理石样品恰好完全反应,故填:
乙;
(2)见答案。