高中化学专题五物质结构和元素周期律讲义新人教版Word格式文档下载.docx
《高中化学专题五物质结构和元素周期律讲义新人教版Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《高中化学专题五物质结构和元素周期律讲义新人教版Word格式文档下载.docx(22页珍藏版)》请在冰豆网上搜索。
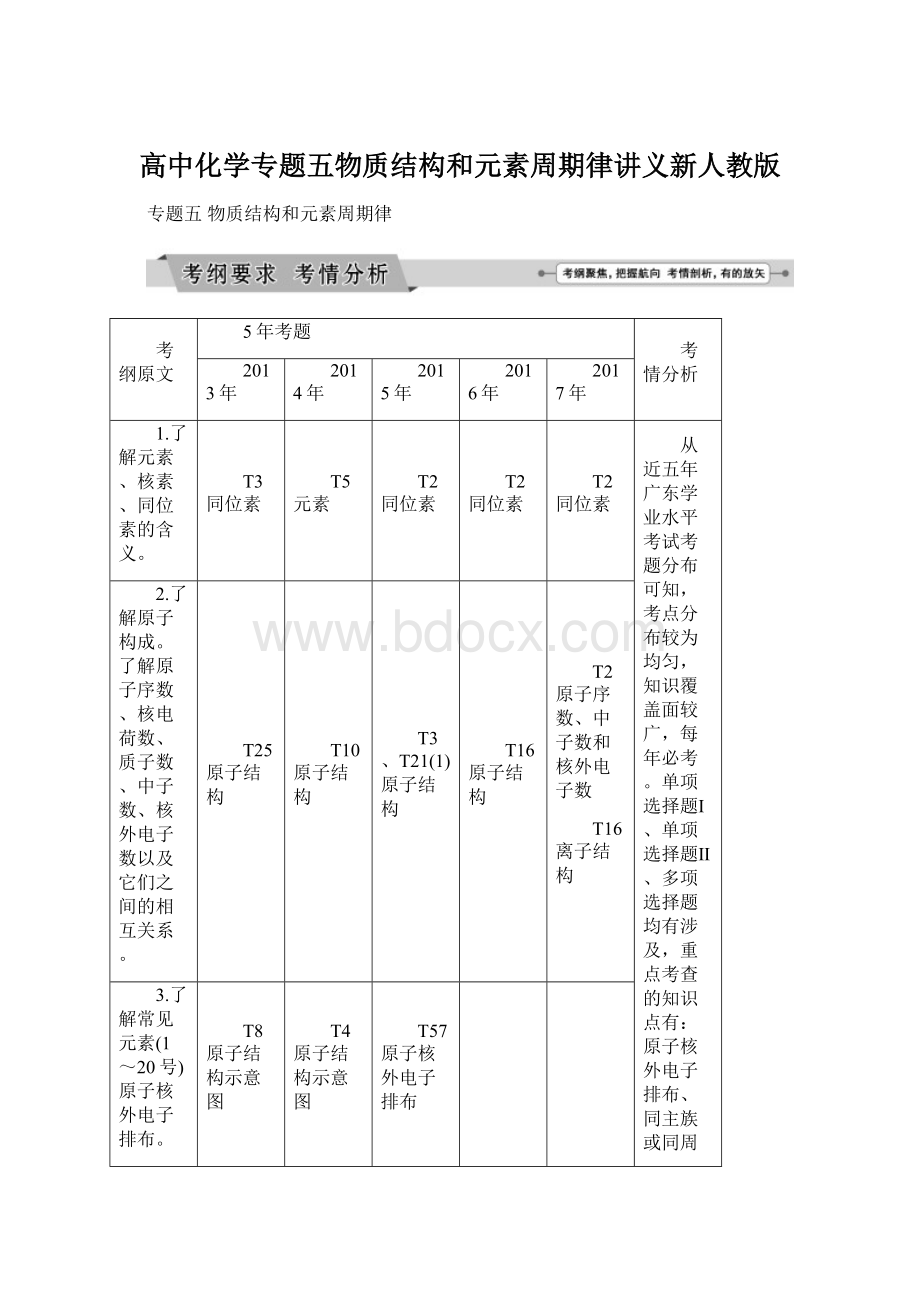
注:
(1)表示1月学业水平考题。
考点1 元素、核素、同位素的含义
1.(2016·
广东学业水平测试T2)碳有三种同位素:
6C、
6C和
6C,它们之间不同的是( )
A.电子数B.中子数
C.质子数D.原子序数
2.(2015·
广东学业水平测试T2)氢有三种同位素:
H、
H和
H,它们之间存在差异的是( )
A.中子数B.电子数
C.原子序数D.质子数
3.(2013·
广东学业水平测试T3)3H在月球上储量丰富,4H主要来源于宇宙射线的初级粒子。
下列关于3H和4H的说法正确的是( )
A.两者互为同位素
B.两者互为同素异形体
C.两者为同一种核素
D.两者具有相同的中子数
1.元素
具有相同核电荷数(质子数)的同一类原子的总称。
2.核素
具有一定数目质子和一定数目中子的一种原子。
绝大多数元素有多种核素,如氢元素有1H、2H、3H3种核素。
3.同位素
质子数相同而中子数不同的同一元素的不同原子互称为同位素,如12C、13C、14C是碳元素的3种核素,互为同位素。
同一种元素的不同同位素原子其质量数不同,核外电子层结构相同,其原子、单质及其构成的化合物化学性质几乎完全相同,只是某些物理性质略有差异。
在天然存在的某种元素中,不论是游离态还是化合态,各种同位素所占的原子个数百分比一般是不变的。
4.元素、核素、同位素之间的关系
[温馨提示]
(1)同位素的概念针对的是核素与核素之间的关系,分子之间就不存在这种关系;
(2)要注意区别同位素、同素异形体和同分异构体三个概念的差异。
C与
C互为同位素,下列说法不正确的是( )
A.
C具有相同的中子数
B.
C具有相同的质子数
C.
C具有相同的最外层电子数
D.
C具有不同的质量数
[解析] 同位素的特点是具有相同的质子数,不同的中子数。
对于原子而言,核外电子数和质子数相同。
[答案] A
[特别提醒] 主要考查同位素概念和质量数、质子数及中子数之间的关系,同位素一定是原子。
下列各组物质中,互为同位素的是( )
A.氧气与臭氧B.金刚石与石墨
C.1H与2HD.正丁烷与异丁烷
[解析] 本题主要考查同位素、同分异构体、同素异形体的有关概念及区别。
氧气与臭氧、金刚石与石墨均互为同素异形体,正丁烷与异丁烷互为同分异构体,1H与2H互为同位素。
[答案] C
[特别提醒] 同位素、同分异构体和同素异形体的对象分别是原子、化合物和单质。
考点2 原子结构
1.(2017·
广东学业水平测试T2)月球上有颇为丰富的核聚变燃料
He。
有关
He的说法正确的是( )
A.原子序数为3B.中子数为3
C.与
He互为同位素D.核外电子数为3
广东学业水平测试T3)具有9个质子和10个电子的微粒是( )
A.Na+B.O2-
C.F-D.Ne
3.(2015·
广东1月学业水平测试T21)基因测试研究中,常用
P作标记物。
下列关于
P的说法正确的是( )
A.质子数为32B.质量数为15
P与
P互为同位素D.中子数为15
4.(2014·
广东学业水平测试T10)陶瓷家族中有“全能冠军”之称的工程陶瓷由氮元素与X元素组成,其化学式为X3N4。
已知X为第三周期元素且原子最外层有4个电子,则X元素为( )
A.CB.Al
C.OD.Si
1.原子的构成
原子(
X)
2.构成原子或离子的各基本粒子间的数量关系
(1)原子的核外电子数=核内质子数=核电荷数=原子序数;
(2)质子数+中子数=质量数≈相对原子质量;
(3)阳离子核外电子数=核内质子数-离子的电荷数;
(4)阴离子核外电子数=核内质子数+离子的电荷数。
3.核外电子的分层排布
(1)核外电子排布规律
第一层不超过2个;
第二层不超过8个;
最外层不超过8个。
(2)原子结构示意图
以Na原子结构示意图为例:
[温馨提示]
(1)元素的化学性质决定于原子的最外层电子数。
(2)原子最外层电子数为8(氦为2)的结构称为稳定结构。
(3)原子、阳离子、阴离子的判断
①原子:
质子数=核外电子数;
②阴离子:
质子数<
核外电子数;
③阳离子:
质子数>
核外电子数。
(2016·
广东学业水平测试)具有11个质子和10个电子的粒子是( )
A.Na+ B.O2-
C.Mg2+D.F-
[解析] O2-有8个质子,Mg2+有12个质子,F-有9个质子。
(多选)右图是某粒子W的结构示意图,下列关于它的说法正确的是( )
A.y=2
B.若x=18,则z=8
C.若x=11,它的氧化物化学式为W2O
D.若x=15,它属于金属元素的原子
[解析] 本题主要考查原子结构示意图及原子核外电子排布。
A项根据原子核外电子排布规律,K层最多可容纳2个电子,y一定等于2;
B、C、D项质子数确定后,则元素及原子的核外电子排布、原子结构示意图均可确定,其中D项若x=15,该元素是磷元素,属于非金属元素。
[答案] ABC
考点3 元素周期表(长式)及元素周期律
广东学业水平测试T59)(多选)短周期非金属元素甲~戊在元素周期表中相对位置如下表所示,下列判断正确的是( )
甲
乙
丙
丁
戊
A.原子半径:
甲>
B.原子核外电子层数:
乙<
C.原子最外层电子数:
丙>
丁>
D.元素的最高价氧化物对应水化物的酸性:
丙<
2.(2014·
广东学业水平测试T65)(多选)甲~辛等元素在周期表中的位置如下表所示。
下列说法正确的是( )
A.甲、丁、戊的单质都是金属
B.乙、丙、辛都是非金属元素
C.乙、庚、辛都能形成氧化物
D.己的氧化物既可溶于KOH溶液又可溶于H2SO4溶液
广东学业水平测试T33)已知某短周期元素原子的第三电子层上排布有5个电子,则该元素在周期表中位于( )
A.第二周期ⅣA族B.第二周期ⅤA族
C.第三周期ⅣA族D.第三周期ⅤA族
1.元素周期表的编排原则
(1)按原子序数(核内质子数)递增的顺序从左到右排列。
(2)将电子层数相同的各元素从左到右排成一横行。
(周期序数=原子的电子层数)
(3)把最外层电子数相同的元素按电子层数递增的顺序从上到下排成一纵行。
(主族序数=原子的最外层电子数)
2.元素周期表与原子结构的关系
(1)原子序数=核电荷数=核内质子数=核外电子数。
(2)周期序数=电子层数。
(3)主族序数=最外层电子数=元素的最高正价数。
(4)|最高正价数|+|最低负价数|=8。
[妙招巧记] 横行叫周期,共有七周期;
三四分长短,第七不完全;
竖行称作族,总共十六族;
Ⅷ族最特殊,三列是一族;
二三分主副,先主后副;
镧锕各十五,均属第ⅢB族;
构位性一体,相互可推断。
据国外资料报道,在一种共生矿——独居石中,查明有尚未命名的116号元素,判断116号元素应位于周期表中的( )
A.第六周期第ⅣA族
B.第七周期第Ⅷ族
C.第七周期第ⅥA族
D.第八周期第ⅥA族
[解析] 第七周期稀有气体原子序数为118,由118-116=2,所以该元素应位于第七周期第ⅥA族。
元素在周期表中的位置,反映了元素的原子结构和性质。
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.短周期元素形成离子后,最外层都达到8电子稳定结构
D.同一主族元素的原子,最外层电子数相同,化学性质完全相同
[解析] Al元素既表现金属性又表现非金属性,故A项错误;
氢元素原子失去1个电子变为H+,H+最外层没有电子,得到1个电子变为H-,H-为2个电子稳定结构,故C项错误;
同一主族元素的原子最外层电子数相同,化学性质不一定完全相同,如第ⅠA族的H和Na,它们的化学性质完全不同,故D项错误。
[答案] B
[特别提醒] 元素在周期表中的位置(位)、元素原子结构(构)、元素的性质(性)之间的关系是元素周期表命题的重点。
另外,在做这方面题目时,可以记住一些特例,用举例法排除一些选项,达到快速、准确答题的目的。
考点4 同周期、同主族内元素性质的递变规律
广东学业水平测试T5)下列元素中,非金属性最强的是( )
A.CB.N
C.SD.O
2.(2016·
广东学业水平测试T3)下列元素中,非金属性最强的是( )
A.SB.Mg
C.PD.Cl
广东学业水平测试T18)下列单质氧化性最强的是( )
A.F2B.Cl2
C.Br2D.I2
4.(2013·
广东学业水平测试T16)元素在周期表中的位置反映了元素的性质。
第三周期元素中,得电子能力最强的是( )
A.NaB.Si
C.SD.Cl
一、元素的金属性与非金属性强弱判断依据
1.金属性
(1)与水(或酸)反应的难易或剧烈程度。
(2)金属与盐溶液之间的置换反应。
(3)金属阳离子的氧化性强弱。
(4)最高价氧化物对应水化物的碱性强弱。
2.非金属性
(1)非金属单质与氢气化合难易程度及氢化物稳定性。
(2)非金属之间的置换反应。
(3)非金属阴离子的还原性强弱。
(4)最高价氧化物对应水化物的酸性强弱(除F外)。
二、微粒半径大小比较的规律
1.同主族:
最外层电子数相同时,先比较电子层数,电子层数多的半径大。
2.同周期:
电子层数相同时,先比较核电荷数,核电荷数多的半径反而小。
3.相同电子层结构:
先比较核电荷数,核电荷数多的半径反而小。
三、碱金属元素与卤族元素
第ⅠA族元素依次是H、Li、Na、K、Rb(Cs、Fr),除了H之外,都称为碱金属元素。
第ⅦA族元素依次是F、Cl、Br、I(At),也称为卤族元素。
[温馨提示]
(1)周期表中,左下方元素,原子半径大,元素金属性最强。
(2)周期表中,右上方元素,原子半径小,元素非金属性最强。
(3)短周期元素中,原子半径最大的是Na,最小的是H;
最活泼的金属是Na,最活泼的非金属是F2,最强的碱是NaOH,最强的含氧酸是HClO4,最稳定的氢化物是HF。
元素的性质随着原子序数的递增呈现周期性变化的根本原因是( )
A.元素相对原子质量的递增而引起的变化
B.元素的化合价呈周期性的变化
C.元素原子核外电子排布呈周期性变化
D.元素的金属性和非金属性呈周期性变化
[解析] 元素的化学性质主要决定于原子的最外层电子数,同一主族元素的化学性质是相似的,原子核外电子排布的周期性变化决定了元素化学性质的周期性变化。
[特别提醒] 物质的结构决定了物质的性质。
(多选)下列各微粒半径依次增大的是( )
A.Ca2+、K+、Mg2+、Al3+
B.F、F-、Cl-、Br-
C.Al3+、Al、Mg、K
D.Ca2+、K+、Cl-、S2-
[解析] 微粒半径大小的比较一般要掌握以下规律:
(1)对原子来说:
①同周期元素的原子,从左到右原子半径逐渐减小;
②同主族元素的原子,从上到下原子半径逐渐增大。
(2)对离子来说:
除符合原子半径递变规律外,经常考查的比较原则是①同种元素的原子和离子相比较,阳离子比相应原子半径小,阴离子比相应原子半径大;
②电子层结构相同的粒子(如O2-、F-、Na+、Mg2+、Al3+),随着核电荷数的增大,离子半径减小。
[答案] BCD
(多选)同周期的三种元素X、Y、Z,已知它们的最高价含氧酸的酸性由强到弱的顺序:
HXO4>
H2YO4>
H3ZO4。
则下列叙述正确的是( )
A.非金属性:
X<
Y<
Z
B.X、Y、Z形成的阴离子的还原性逐渐增强
C.原子半径:
D.X、Y、Z的气态氢化物的稳定性逐渐增强
[解析] 由酸性:
H3ZO4可知X、Y、Z的非金属性强弱顺序为X>
Y>
Z,则三种元素在周期表中从左至右的顺序是Z、Y、X,结合元素周期律的有关知识,可知B、C的叙述正确,其对应气态氢化物稳定性应是X>
Z,D错误。
[答案] BC
考点5 化学键
广东学业水平测试T24)下列化合物中既有共价键又有离子键的是( )
A.Cl2B.NaNO3
C.NaClD.Na2O
广东学业水平测试T12)室温下单质碘为固体,单质氯为气体。
尽管两者存在的状态不同,但两者( )
A.均含离子键
B.都含离子键和共价键
C.均含共价键
D.均可与H2形成离子化合物
广东学业水平测试T12)下列化合物中,既存在离子键又存在共价键的是( )
A.碳酸钠B.乙醇
C.氯化钾D.一氧化碳
4.(2015·
广东1月学业水平测试T34)含有离子键的物质是( )
A.FeB.SiO2
C.HClD.NaCl
5.(2014·
广东学业水平测试T12)NaCl晶体中存在的化学键为( )
A.离子键B.极性键
C.共价键D.非极性键
6.(2013·
广东学业水平测试T43)只含有共价键的物质是( )
A.NeB.K2O
C.Na2SO4D.CH4
1.化学键
定义:
相邻的两个或多个原子之间强烈的相互作用叫做化学键。
化学键
2.离子键
(1)定义:
阴、阳离子间通过静电作用所形成的化学键叫做离子键。
(2)成键元素:
活泼金属(第ⅠA和第ⅡA族元素)和活泼非金属(第ⅥA和第ⅦA族元素)相互结合时形成离子键。
(3)成键原因:
活泼金属原子容易失去电子形成阳离子,活泼非金属原子容易得到电子形成阴离子。
当活泼金属遇到活泼非金属时,电子发生转移,分别形成阳、阴离子,再通过静电作用形成离子键;
离子键构成离子化合物。
(4)存在范围:
金属氧化物、碱、大多数盐等。
3.共价键
原子间通过共用电子对所形成的化学键叫共价键。
通常为非金属元素。
(3)成键原因
①通过共用电子对,各原子最外层电子数目一般能达饱和,由不稳定变稳定;
②两原子核都吸引共用电子对,使之处于平衡状态;
③原子通过共用电子对形成共价键后,体系总能量降低。
(4)分类:
极性键和非极性键
同种元素的原子之间形成的共价键称为非极性共价键,简称非极性键;
不同元素的原子之间形成的共价键称为极性共价键,简称极性键。
[温馨提示]
(1)判断离子键和共价键的方法:
离子键存在于金属离子[或铵根离子(NH
)]与阴离子之间;
共价键存在于非金属元素之间。
(2)离子化合物:
含有离子键的化合物。
例如:
NaCl、CaCl2、NaOH等。
共价化合物:
只含有共价键的化合物。
H2O、CO2、H2SO4等。
下列说法错误的是( )
A.含有共价键的化合物一定是共价化合物
B.在共价化合物中一定含有共价键
C.含有离子键的化合物一定是离子化合物
D.双原子单质分子中的共价键一定是非极性键
[解析] 本题考查离子键和共价键的形成条件。
解答本题时先识别离子化合物和共价化合物,离子化合物中必含离子键,可能含有共价键,如氯化铵和氢氧化钠;
共价化合物只含共价键。
下列各组物质中,化学键类型完全相同的是( )
A.CO2和NaOH
B.SO2和H2O
C.H2和HCl
D.CCl4和NaF
[解析] 根据化学键的类型判断该化合物中存在什么化学键,A项前者为共价键,后者为离子键和共价键;
C项前者为非极性共价键,后者为极性共价键;
D项前者为共价键,后者为离子键。
一、单项选择题Ⅰ
1.(2013·
广东学业水平测试)原子结构示意图为
的元素是( )
A.LiB.Na
C.AlD.K
2.(2013·
广东学业水平测试)在考古中常通过测定14C来鉴定文物年代。
下列有关14C的说法正确的是( )
A.质子数为7B.中子数为8
C.核外电子数为7D.原子序数为14
3.下列元素中金属性最强的是( )
A.MgB.Al
C.NaD.Si
4.下列化合物中存在离子键的是( )
A.CO2B.CH4
C.H2OD.Na2S
5.某元素原子L层电子数是K层电子数的3倍,那么此元素是( )
A.FB.C
C.OD.N
6.下列过程中共价键被破坏的是( )
A.碘升华B.溴蒸气被木炭吸附
C.酒精溶于水D.HCl气体溶于水
7.(2017·
广东学业水平测试)具有12个质子和10个电子的微粒是( )
A.O2-B.Na+
C.Mg2+D.S2-
8.在元素周期表中金属元素和非金属元素的分界线附近的一些元素能用于制( )
A.半导体B.合金
C.催化剂D.农药
9.下列判断正确的是( )
A.核电荷数:
Al<
NaB.金属性:
Na>
Al
C.原子序数:
ClD.原子半径:
Cl>
Na
10.某元素的原子结构示意图为
下列关于该原子的说法正确的是( )
A.质子数为7B.最外层电子数为2
C.核外电子数为7D.核外有3个电子层
11.下列单质中,最容易跟氢气发生反应的是( )
A.O2B.N2
C.F2D.Cl2
12.下列同组微粒间互称同位素的一组是( )
HB.H2O和D2O
C.白磷和红磷D.
K和
Ca
13.与N2分子含有相同电子数的分子是( )
A.O2B.CO
C.NO2D.CO2
14.下列离子中,其核外电子排布与氖原子核外电子排布不同的是( )
A.Mg2+B.O2-
C.K+D.Al3+
15.F、Cl和Br都是第ⅦA族元素,关于这三种元素原子的说法正确的是( )
A.原子半径:
F>
Br
B.最外层电子数都相同
C.核外电子层数相同
D.最外层电子数都不相同
二、单项选择题Ⅱ
16.对Na、Mg有关性质的叙述不正确的是( )
A.碱性:
NaOH>
Mg(OH)2
B.原子半径:
Na<
Mg
D.单质的还原性:
17.下列分子中有3个原子核的是( )
A.HFB.NH3
C.H2OD.CH4
18.(2015·
广东1月学业水平测试)已知S和Cl两种元素均位于第三周期,则( )
S<
Cl
B.元素的非金属性:
S>
C.氢化物的稳定性:
H2S>
HCl
D.最高价氧化物对应水化物的酸性:
H2SO4<
HClO4
19.对于第ⅦA族元素,下列说法不正确的是( )
A.可形成-1价离子
B.从上到下原子半径逐渐减小
C.从上到下原子半径逐渐增大
D.从上到下非金属性逐渐减弱
20.下列说法正确的是( )
A.NaCl固体中含有共价键
B.CO2分子中含有离子键
C.12C、13C、14C是碳的三种核素
D.32S、35S含有相同的中子数
21.下列有关钛原子(
Ti)的说法正确的是( )
A.质子数为48B.中子数为48
C.质量数为22D.原子序数为22
22.M和N都是短周期元素,M的阳离子和N的阴离子具有相同的电子层结构,则下列叙述正确的是( )
A.原子的最外层电子数:
M>
N
B.元素的最高正化合价:
C.离子的微粒半径:
D.元素所在周期数:
23.以下有关原子结构及元素周期律的叙述正确的是( )
A.第ⅠA族元素铯的两种同位素137Cs比133Cs多4个质子
B.同周期元素(除0族元素外)从左到右,原子半径逐渐减小
C.第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强
D.同主族元素从上到下,金属性逐渐减弱
24.某主族元素R原子最外层有6个电子,则其最高价含氧酸钠盐化学式的通式为( )
A.Na2RO3B.Na3RO4
C.NaRO3D.Na2RO4
25.下列关于元素周期表和元素周期律的说法错误的是( )
A.Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多
B.第二周期元素从Li到F,非金属性逐渐增强
C.因为Na比K容易失去电子,所以Na比K的还原性强
D.O与S为同主族元素,且O比S的非金属性强
三、多项选择题
26.(2015·
广东学业水平测试)下列元素中,原子最外层电子数与其电子层数相同的有( )
A.HB.Na
C.AlD.Si
27.下列关于卤化氢的说法中正确的是( )
A.卤素原子半径越大,氢化物越稳定
B.卤素原子半径越大,氢化物越不稳定
C.卤化氢稳定性为HF>
HCl>
HBr>
HI
D.卤素单质与氢气越难反应,生成物越不稳定
28.下列各表分别是元素周期表的一部分,表中的数字表示元素的原子序数,则这些原子序数所代表的元素在周期表中的位置与周期表结构相符的是( )
29.X、Y、Z均为短周期元素,它们在周期表中的相对位置如图所示。
若Y原子的最外层电子数是内层电子数的3倍,下列说法正确的是( )
A.X的气态氢化物比Y的稳定
B.W的最高价氧化物对应水化物的酸性比Z的强
C.Z的非金属性比Y的弱
D.X的氢化物的水溶液显酸