初三升高一化学衔接复习资料docWord下载.docx
《初三升高一化学衔接复习资料docWord下载.docx》由会员分享,可在线阅读,更多相关《初三升高一化学衔接复习资料docWord下载.docx(13页珍藏版)》请在冰豆网上搜索。
1.
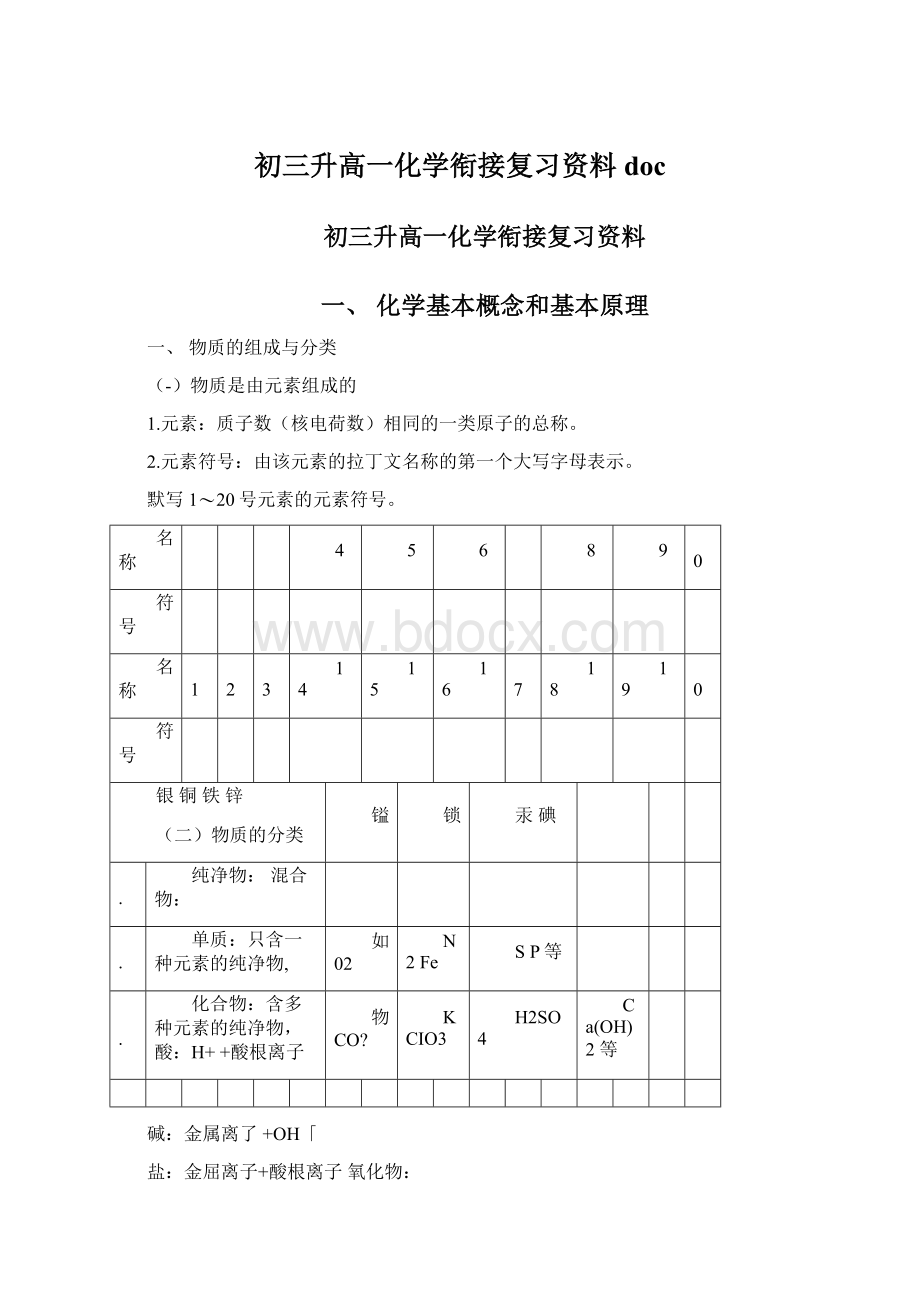
纯净物:
混合物:
2.
单质:
只含一种元素的纯净物,
如02
N2Fe
SP等
3.
化合物:
含多种元素的纯净物,酸:
H++酸根离子
物CO?
KCIO3
H2SO4
Ca(OH)2等
碱:
金属离了+OH「
盐:
金屈离子+酸根离子氧化物:
(三)化学式:
用元素符号表示物质组成的式子。
书写化学式要注意化合价。
化合价:
元素在化合物屮的性质
记住化合价规则:
1.单质中元索化合价为0
2.化合物中,元素化合价代数和为()
3.化合物屮,氧一般为・2价,氢元素为+1价。
金屈只冇正价。
4.记住一些特殊元素在化合物中的化合价
一价钾钠银氯(-1)氢
3铝4硅5价磷
-246硫要记清,
二价氧(・2)钙镁顿锌
铁23碳24
化合物中和为0
练习:
写出下列物质的化学式或化学名称
二、物质的结构
1•构成物质的粒子有:
分子、原子、离子
•分子是保持物质化学性质的粒子。
分子是由原子构成的。
原了是化学变化中的最小粒了
2.原子的结构:
原子由原子核和核外电子构成。
原子中:
原子序数=核电荷数=质子数=核外电子数
3.原子结构示意图
在离子中:
离子所带电荷数=质子数一核外电子数离子所带电荷数与其化合价相同:
(注意加点元素的化合价)
三、物质的变化与性质
1.物理变化:
没冇新物质生成的变化。
如物质状态的转化,形态的变化等。
化学变化:
有新物质生成的变化。
如燃烧等。
2.物理性质:
不需要经过化学变化就表现出来的性质,如颜色、气味、密度、溶解性等。
化学性质:
在化学变化屮表现出的性质。
如可燃性、酸碱性、稳定性等。
3.化学反应的分类:
(1)四种基本反应类型
按照反应物与生成物的类別为种数的多少,化学反应可分为四种基本反应类型:
化合反应、分解反应、
置换反应、复分解反应。
类别
化合反应
分解反应
置换反应
复分解反应
定义
由两种或两种以上物质生成一种物质的反应。
由一种物质生成两种或两种以上物质的反应。
由一种单质跟一种化合物反应生成另一种单质和另一种化合物的反应。
山两种化合物互相交换成分,生成另外两种化合物的反应。
特征
多变一
一变多
1反应物、生成物均为两种物质:
一种单质一种化合物。
2反应完毕后,单质转化为化合物,化合物中的某种元素转化
为单质(化合态一游离态)
1反应物、生成物均为两种化合物。
2反应物小两种化合物相互交换成分能否成功,耍看是否冇沉淀,气体或水生成,满足三者之一反应即可发生,否
则不行。
表达式
A+3->
AB
ABTA+B
A+BC->
3+AC
AB+CD->
AD+BC
此处的氧均既可以指单质形态的氧(游离态)
又可以指化合物屮的氧(化合态)
(2)氧化反应与还原反应
氧化反应:
物质与氧的反应
还原反应:
物质屮的氧被夺去的反应
得氧必然冇物质失氧,因此氧化、还原反应总是同时发生的。
(初中阶段我们将一个反应从两个方面来看,实质为一,高中将就此深入展开讨论)称为氧化述原反应。
其中得氧的物质叫做还原剂,得氧后被氧化,其中所含的某种元素化合价必定升高;
失氧的物质(也就是提供氧的物质)叫做氧化剂,失氧后被还原,具所含的某种元索化合价必定降低。
氧化还原反应屮氧化剂化合价降低的总数与还原剂屮元索化合价
升高的总数必然相等。
以比+CuO=Cu+H2O反应为例:
丹2:
还原剂,有还原性,反应小得氧,被氧化,发牛氧化反应,H元素化合价升高,得到氧化产物片?
。
CuO:
氧化剂,有氧化性,反应屮失氧,被还原,发牛还原反应,Cu元索化合价降低,得到还原产物Cuo
0+1+20
H2tHQ共升高2x(+1—0)=2价,CuOtCm共降低2价。
事实上,即使没有氧元素参加,同样可以发生氧化还原反应,
有化合价升降的反应就是氧化还原反应。
(3)四种基木反应类型与氧化、还原反应的关系。
1化合反应可能冇元索化合价的升降。
如:
点燃
2比+。
2=2H2O
化合反应也可能没有元索化合价的升降。
CO7+HrO=H°
CO\
所以化合反应nJ能是氧化还原反应,也nJ能不是。
一般有单质参加的化合反应,必定有元素化合价的升降,因此是氧化还原反应。
2分解反应与化合反应相似:
可能有元索化合价的升降。
诵由
2H2O=2H2T+O2T也可能没有元素化合价的升降。
CaCO.=CaO+C02T
所以分解反应可能是氧化还原反应,也可能不是,-•般有单质牛成的分解反应,必定有元索化合价的升降,因此是氧化还原反应。
3置换反应,既冇单质参加(单质一化合物),又冇单质生成(化合物中某一元索一单质)其间必冇元素化合价的升降,所以置换反应均为氧化还原反应。
4复分解反应是两种化合物互相交换成分而生成两种新的化合物,其间没有元素化合价的升降,所以复分解反应均不是氧化还原反应。
总之,四种基木反应类型与氧化还原反应的关系可用图示表示为:
可见,化合反应,分解反应与氧化还原反应是交义关系;
置换反应与氧化还原反应是包含关系;
复分解反应与氧化还原反应是排斥关系。
【典型例题分析】
[例1]2000年3月美国钺星公司宣布破产,铁星公司原计划发射77颗卫星以实现全球卫星通讯,发射卫星的数目与铁元素(lr)的原子核外电子数目恰好相等。
卞列关于铁元素的各种说法正确的是()
A.钱原子的质子数为70B.钺原子的相对原子质量为77
C.錶原了的核电荷数为77D.钺元素是金属元素
[例2]计算机产业以惊人的速度发展,计算机芯片生产技术不断改进,生产中所用高纯度的单晶硅其质量分数达到99.999999999%o这种工业产品可认为是()
A.纯净物B.既不是纯净物,也不是混合物C.混合物D.既是纯净物,乂是混合物
[例3]根据物质的纽成或结构不同,具休填写
(1)〜(6)纽物质性质不同的原因。
并以此为例,再写另外两组实例。
(1)金刚石、石墨:
碳原子不同。
(2)钠原子和氯原子:
原子的不同。
(3)CO与CO2:
分子的不同。
(4)酸溶液、碱溶液:
所含的不同。
(5)生铁和钢:
不同。
(6)浓硫酸和稀硫酸:
不同。
(7)o
(8)o
[例4]由H十、Ca"
、CO3A、OFF组成的化合物一共有()
A.2种B.3种C.4种D.5种
[例6]经实验测得某一中性溶液由Mg2\Al3\NO3一、SO产四种离了组成,英中Mg2\AltSO产离了的个数比可能是()
A.3:
1:
10B.3:
5:
1C.3:
10:
1D.3:
[例5]下列反应属于氧化还原反应的是()
A.屁2°
3+3CO=2Fe+3CO2
B.Fe+CuSO4=FeSO4+Cu
C.Na2CO,+2HCI=INaCl+H2O+CO2f
D.Cu2(OH)2CO3=2CuO+CO.?
+W20
课后练习
一.选择题(每题有一个或二个选项符合题意)
1.下列变化中,属于化学变化的是()
A.酒精挥发B.工业上用空气制取氧气
C.冰受热熔化成水D.蓝色硫酸铜品体受热变成白色粉末
2.下列物质属于纯净物的是()
A.碘酒B.液氧C.干冰D.清新的空气
3.阿斯匹林化宁名叫乙酰水杨酸,是一种常用的解热镇痛药,其分了的化学式为c7H6O3oK列说法不疋
确的是()A.它每个分子含16个原子B.它由三种元素组成
■
C.各元索的质量比为C:
H:
O=7:
6:
3D.具相对分子质量为138
4.化学反应2H2O2(过氧化氢)='
J2H2O+O2T的反应事实,说明了()
A.过氧化氢分子在化学反应中可以再分B.化学反应前后分子的总数不变
C.过氧化氢分子是运动的,氢原子是静止的D.在化学反应屮原子可以再分
5.下列符号能代表二个分子的是()
A.MgCl2B.2O2C.屉2°
3D.2AI
6.
下列微粒在化学反应中容易得到电了的是()
Xo根据质量守恒定律,您认为X是()
A.Na.OB.COC.OD.O2
8•卜•列反应中,既属于化合反应,乂属于氧化反应的是()
10.在化合、分解、置换、复分解四种基木反应中,可能生成氧化物的反应有()
A.1种
B.2种
C.3种
D.4种
+i
-2+6
+1
11.有H、
0、S、
Na四种元素,
按指定化合价最多可以组成的化合物种类冇(
)
A.5种
B.6种
C.7种
D.8种
12.下列关于酸、碱、
盐的说法屮,
正确的是(
A.酸、碱一定含氢,盐一定不含氢B.酸、碱、盐都可能含氧
C.碱与盐、酸与盐Z间一定会发生反应D.酸与碱发生中和反应,一定会得到澄清溶液
13.有X、Y、Z三种金属,能发生以下置换反应:
①x+h2so4=xso4+w2T
②Y+HCIT不能反应
③Z+XSQ=X+ZSO4
则X、Y、Z三种金属的活动性由强到弱的顺序可排列为()
A.X、Y、ZB.X、Z、YC.Y、Z、XD.Z、X、Y
14.对于化学反应A+B=C+D的下列说法中,正确的是()
A.若C、D分别为单质和化合物,则该反应一定是置换反应
B.若C、D分別为盐和水,贝U该反应一定是中和反应
C.若A、B、C、D都是化合物,该反应一定是复分解反应
D.若A为碱溶液,B为盐溶液,则C和D可能是两种沉淀
15.5OC时氯化馁的溶解度是5()g,5()°
C时氯化彼的饱和溶液中溶质、溶剂、溶液之间的质量比为()
A.1:
2:
3B.2:
3:
1D.1:
二•填空题
16.用化学符号表示
(1)两个氢原子;
(2)两个氮分了o
17.预计到2000年底,全球拥冇的化合物总数将超过2000万种,其中部分物质是由碳、氢、氧、钠中的某些元素组成的。
(1)请用上述元素按以下分类各写出一种物质的化学式:
常用作还原剂的气态化合物,酸性氧化物,碱性氧化物,碱,
正盐,酸式盐o
(2)写出
(1)中正盐的电离方程式o
18.某些矿物燃料燃烧后,可产生一-种污染空气的有害气体二氧化氮(NO?
)。
二氧化氮溶于水可生成HNO3和NO。
则NO2、HNCh、NO三种物质,按氮元索化合价由低到高的顺序排列为(写化学
••••
式)。
19有A、B、C、D、E五种元素,A的单质是密度最小的气体;
B的次外层电子数占电子总数的丄;
C
的阳离子C+比B原子多2个电子;
D和C具有相同的电子层数,ZT的离子结构与氮原子结构相同;
E和
B具有相同的最外层电子数,但比B多一层,试回答:
(1)写出五种元素符号:
A.B.C.D.E.
(2)写出ZT的离了结构示意图:
o
20.请B选反应物,按以下要求各写出一个化学方程式:
(1)属于氧化反应的化合反应:
;
(2)冇气体生成的分解反应:
:
(3)有盐生成的置换反应:
:
(4)有水牛成的复分解反应:
;
21.哥伦比亚号航天飞机曾用金属铝粉和高氯酸钱(NH4C1O4)混合物作为固体燃料。
加热铝粉使其被氧气氧化,放岀大量的热,促使混合物中高氯酸鞍叉热分解,同时生成四种气体,二种气体是空气中的主要成分,一种气体是氯气(CR),还有一种气体是化合物(常温下是液态),因而产生巨大的推动力。
试写出其屮涉及反应的化学方程式:
(1)铝粉被氧气氧化成三氧化二铝:
(2)髙氯酸钱受热分解:
o
二物质的转化
以上图示表示了各类物质之间的转化。
(一般规律)
1、单质」氧化物
2Cu+O2二2CuOMg+O2=Fe+O2=
C+O2=S+O2=P+O2=H2+。
2=_
2、金属单质+非金属单质f盐
(不稳定性)酸一酸性氧化物+出0
H2CO3=co2+h2o
4、碱性氧化物+H2O-(可溶)碱
BaO+也0=
CaO+H20=Ca(OH)2Na20+H20=
不溶性碱一碱性氧化物+H2O(需要加热)Fe(OH)3=FqzC”+H2OCu(OH)2=
A1(OH)3=
MgO+HNO:
}二
(反应物需可溶)
CuCl2+NaOH=
9、盐+碱一新盐+新碱
FeCL+NaOH=
10、酸+盐一新酸+新盐
CaC03+HC1二
H2S04+BaCl2=
11、盐+盐一新盐+新盐(反应物需可溶)
Na2CO3+CaCl2=
CuSO4+Ba(OH)2=
+H2SO4二
+1IC1二
金属+盐f新金属+新盐(需可溶盐)
+CuSOi=
+AgNO3二
12、金属+酸一盐+也
Zn
Fe
13、
Cu
以上6、7、8、9、10、11属于复分解反应,复分解反应的特征是:
双交换,价不变。
复分解反应发生的条件是:
生成物有水、沉淀、气体。
以上12、13属于在溶液中詈换反应,依据金属活动性顺序判断。
KCaNaMgAlZnFeSnPbHCuHgAgPtAu
在溶液中排在前面的能置换后面的,在溶液中,K、Ca、Na、Ba不能置换后面的金属。