中考化学化学溶解度大题培优含答案文档格式.docx
《中考化学化学溶解度大题培优含答案文档格式.docx》由会员分享,可在线阅读,更多相关《中考化学化学溶解度大题培优含答案文档格式.docx(22页珍藏版)》请在冰豆网上搜索。
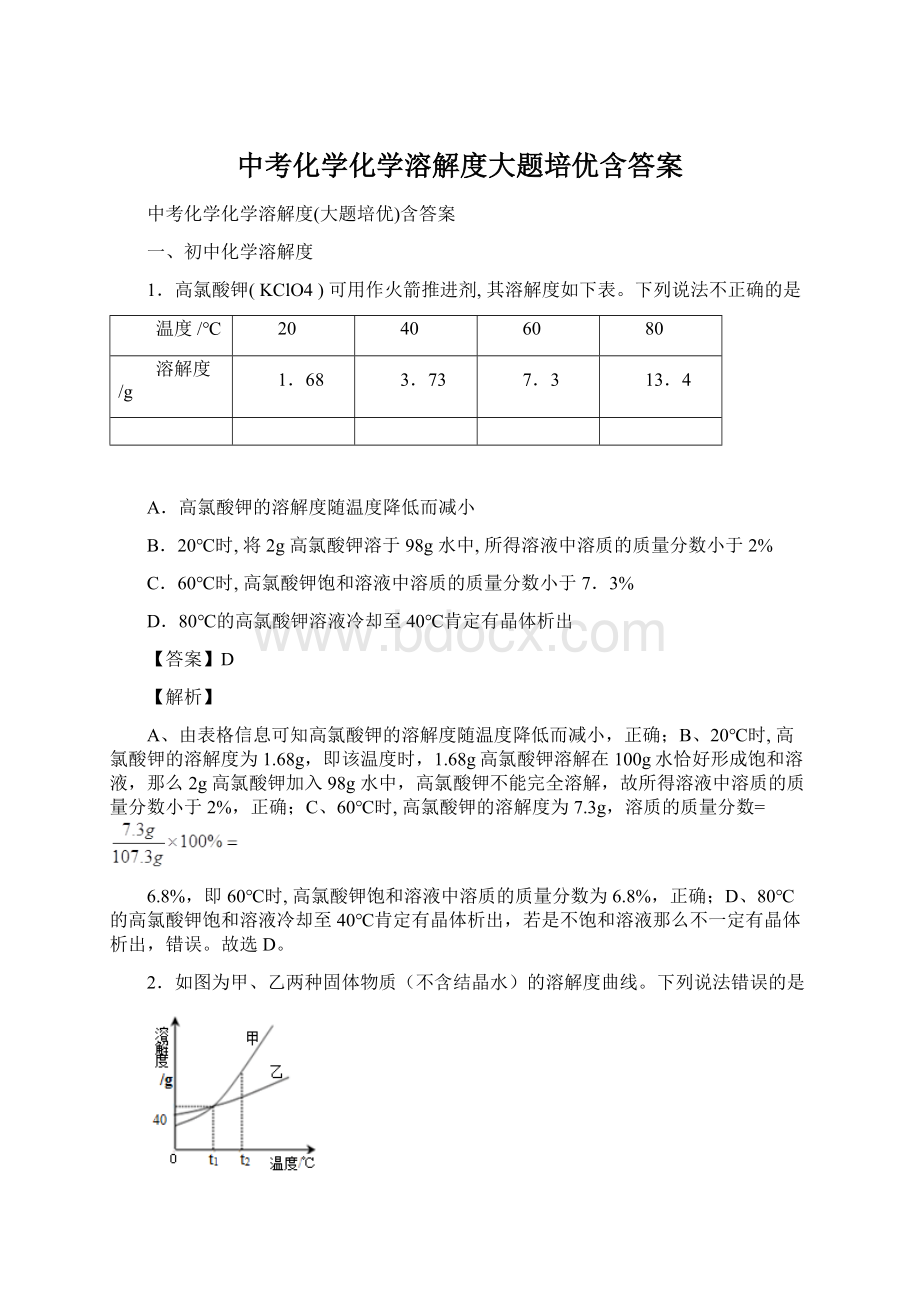
下列说法错误的是
A.t2℃时,甲的溶解度大于乙
B.t1℃时,甲、乙各25g加到50g水中,均得70g溶液
C.t1℃时,甲、乙两种物质的溶液中溶质质量分数相等
D.t2℃时,将溶剂均为100g的甲、乙的饱和溶液分别降温到t1℃时,析出晶体的质量甲>
乙
【答案】C
【分析】
【详解】
A.由图像可知,t2℃时,甲的溶解度大于乙,正确;
B、t1℃时,甲、乙两种物质的溶解度是40g,所以各25g分别加入到50g水中,充分溶解,得到的溶液质量都是70g,故B正确;
C、t1℃时,溶液的饱和状态不确定,所以甲溶液的溶质质量分数不一定等于乙溶液的溶质质量分数,故C错误;
D.t2℃时,甲的溶解度大于乙,将溶剂均为100g的甲、乙的饱和溶液分别降温到t1℃时,析出晶体的质量甲>
乙,正确;
故选C。
3.下图是M、N两种物质的溶解度曲线,由溶解度曲线得出以下几条信息,你认为错误的是( )
A.t1℃时,M、N两物质溶液的溶质质量分数相等
B.N物质的溶解度随温度的升高而降低
C.t2℃时,M物质的溶解度大于N物质的溶解度
D.由t1℃升温到t2℃时,N物质溶液的溶质质量分数可能改变
【答案】A
试题分析:
有溶解度曲线图可知A.t1℃时,M、N两物质溶液溶质质量分数相等是错误的叙述,没有说明溶液是否饱和;
B选项N物质的溶解度随温度的升高而降低是正确的叙述;
C选项t2℃时,M物质的溶解度大于N物质的溶解度D选项由t1℃升温到t2℃时,N物质溶液溶质质量分数可能改变是正确的叙述,看是否加入溶质;
故选A
考点:
溶解度曲线
4.在一定温度下,将少量生石灰放入一定的饱和石灰水中,搅拌并冷却、到原来的温度,下列说法中正确的是( )
A.溶剂质量不变B.溶质质量增加
C.溶液浓度不变D.溶解度增加
由于生石灰会与水反应生成氢氧化钙,同时还会放出大量的热,A、溶剂质量应变小,而不是不变,错误,B、由于饱和溶液水分减少,故溶质会结晶析出,故溶质质量也减少,而不是增加,错误,C、因为最后冷却到原来的温度,成为同温下的饱和溶液,故溶液浓度不变,正确,D、温度没变,溶解度也不变,错误,故选C
溶液的成分,氧化钙的化学性质,溶解度的影响因素,溶质质量分数的计算
5.下列有关溶解度的说法错误的是( )
A.20℃时,甲和乙的溶解度相等
B.40℃时,若将40g乙放入160g水中充分溶解,所得溶液的溶质质量分数为20%
C.40℃时,将甲、乙两物质的饱和溶液各100g,降温至20℃,析出晶体(均不含结晶水)的质量关系是:
m(甲)=m(乙)
D.20℃时,将甲物质的饱和溶液升温到40℃,溶液变为不饱和溶液
A、通过分析溶解度曲线可知,20℃时,甲和乙的溶解度相等,故A正确,不符合题意;
B、40℃时,乙物质的溶解度是40g,所以若将40g乙放入160g水中充分溶解将完全溶解,故所得溶液的溶质质量分数为
100%=20%,故B正确,不符合题意;
C、40℃时,甲物质的溶解度大于乙物质的溶解度,将甲、乙两物质的饱和溶液各100g,降温至20℃,甲、乙物质的溶解度相等,所以析出晶体(均不含结晶水)的质量关系是:
m(甲)>m(乙),故C错误,符合题意;
D、20℃时,将甲物质的饱和溶液升温到40℃,溶解度增大,所以溶液变为不饱和溶液,故D正确,不符合题意。
6.物质甲与乙的溶解度曲线如图所示,下列说法错误的是
A.常温下,乙易溶于水
B.t2℃甲的饱和溶液中溶质的质量分数比乙的饱和溶液大
C.从t2℃降至t1℃,甲溶液中有晶体析出
D.甲的溶解度受温度的影响程度比乙的大
由物质甲与乙的溶解度曲线可知,甲的溶解度随温度的升高而增大,乙的溶解度随温度的变化基本不变,t1℃时,甲乙两种物质的溶解度相同。
A、乙的溶解度为35.7℃,则常温下,乙易溶于水,故A正确;
B、t2℃,甲的溶解度大于乙的溶解度,根据饱和溶液溶质质量分数计算公式为
,则甲的饱和溶液中溶质的质量分数比乙的饱和溶液大,故B正确;
C、从t2℃降至t1℃,甲的饱和溶液中有晶体析出,故C不正确;
D、甲的溶解度随温度的升高而增大,则甲的溶解度受温度的影响程度比乙的大,故D正确。
故选A。
【点睛】
7.如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是()
A.甲和乙的溶解度相等
B.乙的溶解度受温度影响比甲大
C.降低温度可使接近饱和的甲或乙溶液变为饱和
D.10℃时,甲、乙的饱和溶液中所含溶质质量一定相等
A、没有温度限制不能比较溶解度的大小,故A错;
B、由图示可知甲的溶解度曲线较陡,所以乙的溶解度受温度影响比甲小,故B错;
C、降温后甲和乙的溶解度都变小,所以由不饱和变为饱和溶液,故C正确;
D、不知道溶液的质量,没法比较含溶质质量的大小.故D错.
故选C.
固体溶解度曲线及其作用;
饱和溶液和不饱和溶液相互转变的方法.
点评:
溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:
同一溶质在不同温度下的溶解度;
同一温度下,不同溶质的溶解度;
温度对不同物质的溶解度影响不同.
8.三种不含结晶水的固体物质甲、乙、丙的溶解度曲线如下图,下列说法正确的是()
A.将t1℃时的三种物质的饱和溶液升温至t2℃时,所得溶液的的溶质质量分数大小顺序是乙>
甲>
丙
B.在t2℃时,甲、乙两饱和溶液中含的溶质质量一定相等
C.甲、乙、丙三种物质的饱和溶液升温都会转化为不饱和溶液
D.要从含有少量甲的乙溶液中得到较多的乙晶体,通常可采用降温结晶的方法
从溶解度曲线图看,t1℃时,甲、乙、丙的溶解度大小关系为乙>
丙,物质甲、乙的溶解度都随温度的升高而增大,丙的溶解度随温度的升高而减少,乙的溶解度随温度的升高变化不大。
A、从溶解度曲线图看,t1℃时,甲、乙、丙的溶解度大小关系:
乙>
丙,物质甲、乙的溶解度都随温度的升高而增大,所以升温,它们由饱和溶液变为不饱和溶液,但溶液中的溶质和溶剂质量不变,而丙的溶解度随温度的升高而减少,这样溶质析出,所以所得溶液的溶质质量分数大小顺序是乙>
丙,故A正确;
B、在t2℃时,甲、乙的溶解度相等,等质量甲、乙两饱和溶液中含的溶质质量一定相等,故B不正确;
C、丙的溶解度随温度的升高而减少,故丙物质的饱和溶液升温,会有晶体析出,溶液仍然饱和,故C不正确;
D、乙的溶解度随温度的升高变化不大,所以要从含有少量甲的乙溶液中得到较多的乙晶体,应采用蒸发结晶的方法,故D不正确。
乙的溶解度随温度的升高变化不大,从含有少量甲的乙溶液中得到较多的乙晶体,采用蒸发结晶的方法。
9.如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述正确的是( )
A.t2℃时,甲、乙两种溶液降温至tl℃均有固体析出时,所得甲、乙溶液溶质质量分数相等
B.甲中混有少量乙,可用加热蒸发的方法提纯乙
C.tl℃时,甲、乙两种饱和溶液的溶质质量相等
D.t2℃时,用210g甲的饱和溶液加水可以配制成500g20%的甲溶液
A、t2℃时,甲、乙两种溶液降温至tl℃均有固体析出时,都属于饱和溶液,tl℃时甲、乙两物质的溶解度相等,故所得甲、乙溶液溶质质量分数相等,正确;
B、甲物质溶解度受温度影响变化较大,所以甲中混有少量乙,可用降温结晶的方法提纯乙,错误;
C、tl℃时,甲、乙两种饱和溶液的质量不能确定,所以饱和溶液的溶质质量不能确定,错误;
D、t2℃时,甲的溶解度为110g,用210g甲的饱和溶液加水可以配制成500g溶质质量分数为:
×
100%=22%的甲溶液,错误。
10.如图是a、b、c三种物质的溶解度曲线,下列说法错误的是
A.t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c
B.P点表示t1℃时,a、c两种物质的溶解度相等
C.将c的饱和溶液变为不饱和溶液,可采用降温的方法
D.t2℃时,将30ga物质加入到50g水中充分搅拌,得到80ga的饱和溶液
依据图形,A、B、C正确;
t2℃时,a的溶解度为50g,则t2℃时,将30ga物质加入到50g水中充分搅拌时只能溶解25ga物质,则75ga的饱和溶液,D错误。
溶解度曲线。
11.下列说法正确的是
A.均一稳定的液体一定是溶液B.饱和济液一定是浓溶液
C.汽油洗涤油污属于乳化现象D.将氢氧化钠溶于水,所得溶液温度升高
A.均一稳定的混合物一定是溶液;
B、饱和溶液是在一定温度下、一定量的溶剂里不能再溶解某物质的溶液叫该物质的饱和溶液,反之为不饱和溶液。
溶质、溶剂、温度不相同时,饱和溶液不一定是浓溶液;
C汽油洗涤油污形成的是溶液,属于溶解现象;
D氢氧化钠固体溶于水放出大量热,所得溶液温度升高。
选A。
12.M是硝酸钾或氯化铵中的一种。
硝酸钾和氯化铵的溶解度曲线如图1所示。
某化学兴趣小组用物质M进行了如图2所示实验。
下列说法不正确的是()
A.物质M是硝酸钾
B.溶液②中溶质质量分数为37.5%
C.溶液①②③中,溶质质量分数的关系是②>③>①
D.溶液①为不饱和溶液,溶液②和③为饱和溶液
A、由图2可知,t2
时,烧杯
中100g的水将60g的M物质完全溶解,而t2
时氯化铵的溶解度小于60g,故可以确定M物质是硝酸铵,故A正确;
B、溶液
是100g的水中溶解了60g的硝酸钾,故溶质的质量分数为
=37.5%,故B正确;
C、溶液①②④中,②的溶质质量分数为37.5%,①的溶质质量分数为
,③的溶质质量分数要比②小,不一定比①大,故C错误;
D、溶液①经升温蒸发后变为溶液②,t2
时硝酸钾的溶解度是60g,溶液②中刚好是100g的水和60g的硝酸钾,故溶液②刚好是饱和溶液,溶液③中有固体析出,故溶液③也是饱和溶液,故D正确。
13.在一定温度下的饱和食盐水里加入少量的硝酸钾晶体,则( )
①硝酸钾晶体不溶,②硝酸钾晶体溶解,③溶液中食盐的质量分数不变,④溶液中食盐的质量分数减小,⑤溶液中食盐的质量分数增大.
A.①③B.②③C.②④D.②⑤
根据饱和溶液的定义可以知道,饱和溶液是指在一定的稳定下对一种溶质来说的,若该加入其他的溶质仍能够继续溶解,即加入少量的硝酸钾晶体后,硝酸钾能够继续溶解,由于硝酸钾的溶解,而使溶液的质量增加,所以食盐的质量分数要减小,②④是正确的,故选C。
根据饱和溶液的定义可知:
在一定温度下,向一定量溶剂中加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫这种溶质的饱和溶液,也就是说对这种溶质是饱和的,但是其他的溶质仍可以继续溶解直至饱和。
14.如图是X、Y、Z三种固体的溶解度曲线,下列有关说法中不正确的是()
A.Z的溶解度随温度的升高而降低
B.t1℃时,Y的溶解度大于Z的溶解度
C.t3℃时,X的饱和溶液中溶质的质量分数为40%
D.t2℃时,X的溶解度和Y的溶解度相等
根据溶解度曲线,可以看出物质的溶解度随着温度的变化而变化的情况;
还可以判断或比较某一物质在不同温度下的溶解度大小;
饱和溶液中溶质的质量分数=
100%。
观察溶解度曲线,可以看出Z的溶解度随温度的升高而降低,A正确;
观察溶解度曲线,可以看出t1℃时,Y的溶解度大于Z的溶解度,B正确;
观察溶解度曲线,可以看出t3℃时,X的溶解度是100g,所以其饱和溶液溶质的质量分数是:
100%=50%,故C错误;
观察溶解度曲线,可以看出t2℃时,X的溶解度和Y的溶解度相交于一点,说明二者的溶解度在此温度下相等,D正确。
15.如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是()
A.甲物质的溶解度随温度的升高而增大
B.在t1℃时,甲、乙两物质的溶解度相等
C.在t2℃时,N点表示甲物质的不饱和溶液
D.在t1℃时,100g乙物质的饱和溶液中溶质的质量是25g
A、从甲的溶解度曲线不难看出,甲的溶解度随温度的升高而增大,且受温度的影响很大,故A正确;
B、在t1℃时,这两种物质的溶解度相等,故B正确;
C、由于在t2℃时,N点在甲的溶解度曲线的下方,因此代表的是甲的不饱和溶液,故C正确;
D、由于在t1℃时,乙的溶解度是25克,即在100克水中最多溶解25克乙,故D错误;
故选D.
【点评】本题难度不大,主要考查了对固体的溶解度的概念的应用和固体溶解度曲线的意义,培养学生对知识的分析能力和应用能力.
16.一定温度下,向盛有100g蔗糖溶液的烧杯中再加入5克蔗糖,充分搅拌后一定不变的是
A.溶质的质量B.溶液的质量C.溶质的质量分数D.蔗糖的溶解度
溶液由溶质和溶剂组成,溶液的质量等于溶质和溶剂的质量和,被溶解的物质叫溶质。
在一定温度下,向盛有100克蔗糖溶液的烧杯中再加入5克蔗糖,不确定蔗糖是否溶解,溶质、溶液、溶质的质量分数不能确定是否改变,影响固体物质溶解度的因素是温度,温度没有改变,溶解度一定不改变,故选D。
17.甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法正确的是( )
A.降温可使丙物质的不饱和溶液变成饱和溶液
B.t2℃时,等质量甲、乙、丙的饱和溶液中溶剂的质量:
甲>乙>丙
C.t2℃时,将15g甲物质加入到50g水中,再降温到t1℃,所得溶液溶质的质量分数不变
D.分别将甲、乙、丙三种物质t2℃的饱和溶液降温到t1℃,所得溶液溶质的质量分数乙>甲=丙
A、丙物质随着温度升高溶解度降低,故降温不可使丙物质的不饱和溶液变成饱和溶液,错误;
B、t2℃时,甲、乙、丙的饱和溶液,溶质质量分数根据图可知,甲>乙>丙,故等质量甲、乙、丙的饱和溶液中溶质的质量:
甲>乙>丙,溶剂=溶液-溶质,故答案顺序正好反了,错误;
C、t2℃时,将15g甲物质加入到50g水中,再降温到t1℃,溶解度为30g,即100g水中溶解30g,得50g水最多溶解正好为15g,所以所得溶液溶质的质量分数不变,正确;
D、分别将甲、乙、丙三种物质t2℃的饱和溶液降温到t1℃,应该是图像的平移,丙不变,甲、乙分别减小到t1℃和两溶解度曲线的交点,故所得溶液溶质的质量分数乙>甲>丙,错误。
18.下图是a、b两种固体物质的溶解度曲线,下列说法中正确的是()
A.a中含有少量b时,一般用蒸发溶剂的方法提纯a
B.t℃时,a、b饱和溶液中含有的溶质质量a大于b
C.当温度大于t℃时,a溶液一定比b溶液浓
D.a物质的溶解度受温度变化的影响较大
A、从溶解度曲线可看出,a的溶解度随温度的升高变化较大,而b的溶解度随温度的升高而变化较小,故a中含有少量b时,可以用冷却热饱和溶液的方法提纯a,选项A错误;
B、t℃时,a物质的溶解度大于b物质的溶解度,故等质量a、b饱和溶液中含有的溶质质量a大于b,但没有指明是等质量,选项B错误;
C、当温度大于t℃时,a物质的溶解度大于b物质的溶解度,但a溶液不一定比b溶液浓,因为没有讲清楚是否是饱和溶液,选项C错误;
D、从溶解度曲线可看出,a物质的溶解度受温度变化的影响较大,选项D正确。
19.盐场晒盐后得到的卤水中含有MgCl2、KCl和MgSO4等物质,它们的溶解度曲线如图所示。
下列说法正确的是
A.MgSO4的溶解度始终随温度的升高而减小
B.t1℃时,KCl和MgSO4两溶液所含溶质的质量一定相等
C.t2℃时,100gMgCl2的饱和溶液中含有agMgCl2
D.将t2℃时的MgSO4饱和溶液降温到t1℃,溶液的变化是:
饱和→不饱和→饱和
A、由溶解度曲线可知,MgSO4的溶解度随温度的升高先增大后减小,错误;
B、t1℃时,KCl和MgSO4的溶解度相等,即等质量的KCl和MgSO4的饱和溶液所含溶质的质量一定相等,错误;
C、t2℃时,MgCl2的为ag,即该温度时ag氯化镁溶解在100g水中恰好形成饱和溶液,那么100gMgCl2的饱和溶液中含有的溶质氯化镁小于ag,错误;
D、由溶解度曲线可知,MgSO4的溶解度随温度的升高先增大后减小,且t2℃时的溶解度大于t1℃时的溶解度,那么将t2℃时的MgSO4饱和溶液降温到t1℃,溶液的变化是:
饱和→不饱和→饱和,正确。
点睛:
比较溶质质量的大小要指明溶液的质量和状态。
20.地球深处的水处于超临界状态,称为超临界水。
下图为某压强下CaCl2和NaCl在超临界水中的溶解度曲线,该压强下,下列说法正确是()
A.在超临界水中,NaCl的溶解度大于CaCl2的溶解度
B.在超临界水中,2种物质的溶解度都随温升高而增大
C.450℃时,NaCl在超临界水的溶解度为0.04g
D.450℃时,可得到0.04%的CaCl2的超临界水溶液
A、比较物质的溶解度要指明温度,错误;
B、由溶解度曲线可知,在超临界水中,2种物质的溶解度都随温升高而减小,错误;
C、由溶解度曲线可知,450℃时,NaCl在超临界水的溶解度为0.04g,正确;
D、450℃时,CaCl2的溶解度小于0.02g,不可能得打0.04%的溶液,错误。
21.如图是甲、乙两种固体物质的溶解度曲线,下列说法错误的是( )
A.甲中含有少量的乙可以采用降温结晶的方法提纯甲
B.将t1℃甲、乙的饱和溶液升温至t2℃时,乙溶质质量分数变小
C.t2℃时,甲饱和溶液中溶质的质量分数比乙饱和溶液大
D.t2℃时,等质量的甲、乙两种物质配饱和溶液,甲溶液质量大
A、甲中含有少量的乙可以采用降温结晶的方法提纯甲正确,因为甲固体物质的溶解度是随温度升高而增大,而乙的溶解度随温度的升高而减少,不符合题意;
B、乙的溶解度随温度的升高而减少,将t1℃甲、乙的饱和溶液升温至t2℃时,乙溶质质量分数变小,因为乙有固体析出,不符合题意;
C、t2℃时,甲饱和溶液中溶质的质量分数比乙饱和溶液大,因为该温度下甲的溶解度大于乙,不符合题意;
D、t2℃时,甲的溶解度大于乙,等质量的甲、乙两种物质配饱和溶液,甲所需溶剂质量小于乙,故乙溶液的质量大,符合题意。
22.甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法正确的是
A.甲、乙物质都适用降温结晶法使溶质从溶液中析出
B.60℃时将40g甲物质加入50g水中能得到90g饱和溶液
C.通过降温能使A点甲的不饱和溶液变为饱和溶液
D.分别将甲、乙物质饱和溶液从60℃降至20℃,甲析出晶体较多
A、甲、乙的溶解度都随温度的降低而减小,但乙的溶解度受温度影响较小,乙适用蒸发结晶法使溶质从溶液中析出,故A错误;
B、60℃时,甲的溶解度为60g,将40g的甲加入50g水中只能溶解30g,能得到80g饱和溶液,故B错误;
C、甲的溶解度随温度的降低而减小,通过降温能使A点甲的不饱和溶液变为饱和溶液,故C正确;
D、溶液的质量没有确定,无法确定将甲、乙饱和溶液从60℃降至20℃,溶质的析出质量,故D错误。
23.根据下列溶解度曲线和A物质的部分温度是的溶解度判断下列说法正确的是
温度/℃
溶解度/g
A物质
28
45
A.由上图可知,KNO3和NaCl的溶解度均大于A物质的溶解度
B.10℃时,将40gNaCl放入50g水中,充分溶解,所得溶液是NaCl的不饱和溶液
C.将30℃时NaCl、KNO3、和A物质的饱和溶液各降温至10℃,所得溶液的溶质质量分数大小为:
KNO3>NaCl>A
D.20℃时,将KNO3、NaCl和A物质各30g分别配制成恰好饱和溶液,所得溶液的质量大小为A>KNO3=NaCl
A、0℃时,硝酸钾的溶解度小于A物质的溶解度,故A错误;
B、10℃时,氯化钠的溶解度小于40g,所以将40gNaCl放入50g水中,充分溶解,所得溶液是NaCl的饱和溶液,故B错误;
C、将30℃时NaCl、KNO3、和A物质的饱和溶液各降温至10℃,氯化钠的溶解度最大,硝酸钾的溶解度最小,所以所得溶液的溶质质量分数大小为:
NaCl>A>KNO3,故C错误;
D、20℃时,A物质的溶解度最小,氯化钠和硝酸钾的溶解度相等,所以将KNO3、NaCl和A物质各30g分别配制成恰好饱和溶液,所得溶液的质量大小为A>KNO3=NaCl,故D正确。
24.下面关于饱和溶液的说法中,正确的是()
A.含有溶质很多的溶液
B.还能继续溶解某种溶质的溶液
C.不能继续溶解某种溶质的溶液
D.在一定温度下,一定量的溶剂里,不能再溶解某种溶质的溶液
A、含有溶质很多的溶液不一定是饱和溶液,选项错误;
B、还能继续溶解某种溶质的溶液是不饱和溶液,选项错误;
C、不能继续溶解某种溶质的溶液,没有指明温度和溶剂的量,选项错误;
D、在一定温度下,一定量的溶剂里,不能再溶解某种溶质的溶液,选项正确;
25.下图是甲、乙、丙三种物质在水中的溶解度曲线。
以下说法正确的是()
A.t2℃时溶解度由大到小的顺序是乙>
丙>
甲
B.由t2℃降到t1℃析出晶体最多的是甲溶液
C.由t2℃降到t1℃丙溶液浓度一定不发生变化
D.甲乙丙三种物质溶解度都随温度升高而增大
A、根据溶解度曲线可知,在t2℃时,三种物质的溶解度大小关系是甲>