无机二氧化钛文档格式.docx
《无机二氧化钛文档格式.docx》由会员分享,可在线阅读,更多相关《无机二氧化钛文档格式.docx(11页珍藏版)》请在冰豆网上搜索。
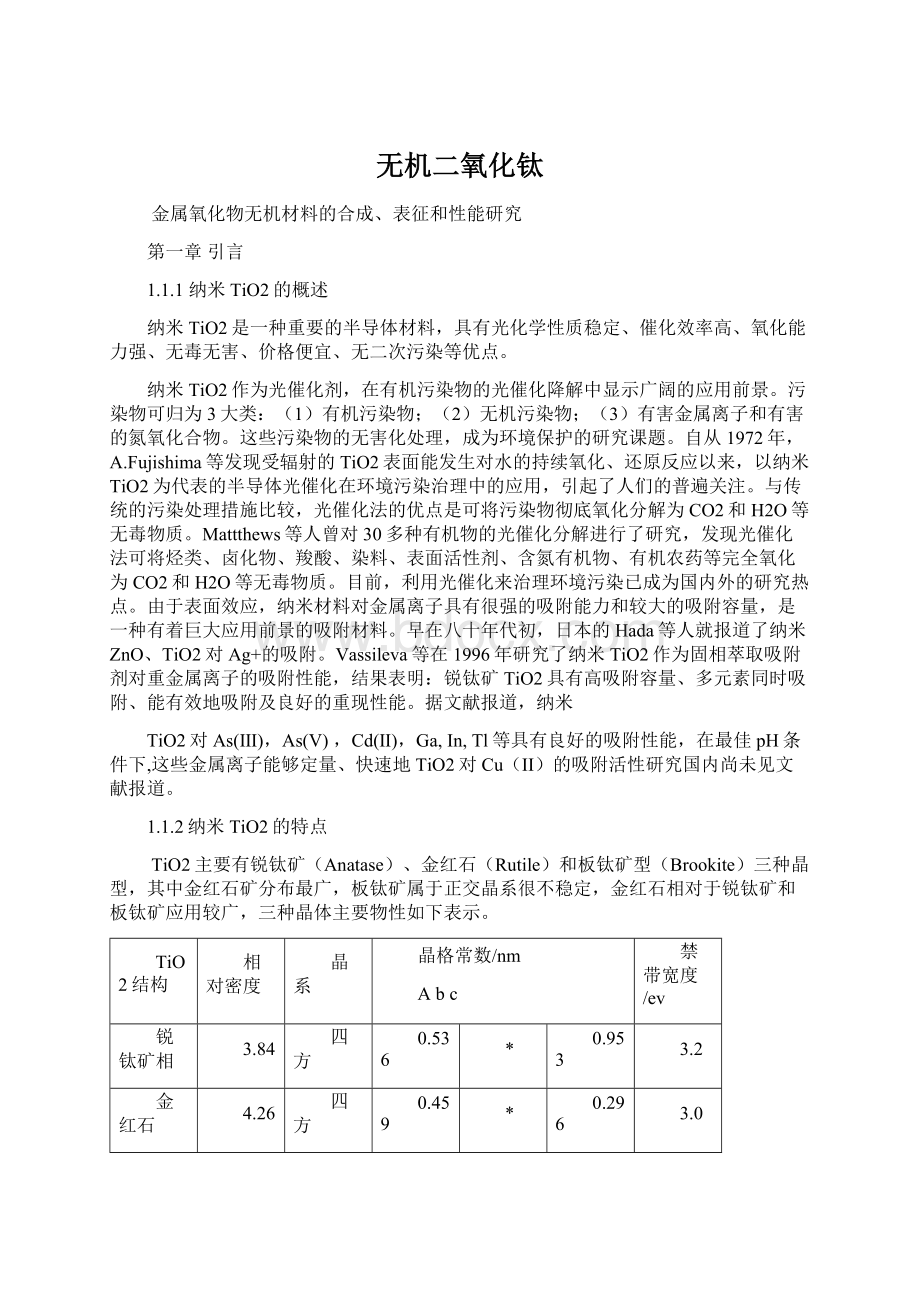
晶格常数/nm
Abc
禁带宽度/ev
锐钛矿相
3.84
四方
0.536
*
0.953
3.2
金红石
4.26
0.459
0.296
3.0
板钛矿
4.17
斜方
0.915
0.544
0.514
*
其中锐钛矿和金红石的晶体结构中,Ti4+离子位于相邻的六个O32+。
离子形成的八面体中,两者的差别主要在于八面体结构之间的结合方式不同,图1.1是两种结构的结构示意图。
,钛矿在常温下较为稳定,高温时向金红石相转变,这属于不可逆转变。
第二章实验部分
2.1纳米TiO2材料的制备
2.1.1低温水热合成法
1)准备两个干燥的250ml烧杯。
在一个烧杯中加入100ml无水乙醇和10ml钛酸四丁脂,搅拌使其混合均匀。
另取250ml烧杯,加入100ml水,HNO3调节PH值=1,加热到70°
C,不断搅拌将两种溶液充分混合。
可观察到钛酸四丁脂分解,产生白色凝胶,在70°
C干燥箱中静置0.5h。
2)将沉淀离心分离。
沉淀用去离子水充分洗涤后,置于干燥箱中干燥。
干燥后的粉末收集于样品袋中,留作下面的实验。
2.1.2结果分析与讨论
水热合成法由于是在相对较高的温度下进行,通常可直接得到晶化产物。
水热温度、水热反应时间和水醇比是影响产物TiO2结构的重要参数。
采用水热合成法易造成局部浓度过高,颗粒大小、形状不均、分散性差,在干燥过程中TiO2易团聚,影响产品的使用效果和应用范围。
2.2纳米TiO2材料的热力学性质的研究
2.2.1热分析方法
物质在加热或冷却过程中可能发生诸如状态变化、晶型转变、异构化、水合物脱水、热分解、氧化还原反应等物理或化学变化。
热分析就是通过测量物质的这些变化达到对物质的定性、定量表征。
2.2.2实验步骤
1)取少量自制TiO2粉置于特制的坩锅内,按照一定升温速度升温(10℃/min.),测定到TiO2粉的DTA曲线。
对热曲线结果进行分析,判断TiO2从无定形到锐钛矿相,从锐钛矿相到金红石相的相转变温度。
2)根据热分析曲线的分析结果,确定TiO2的烧结温度。
3)纳米TiO2的热处理在微波马弗炉中进行,程序升温控制升温速度,禁止从室温一步升至所需烧结温度。
保温时间:
0.5h。
2.2.3结果与讨论
根据上图中重量损失曲线,可知TiO2样品在加热过程中,有机杂质分解,导致样品质量不断减少,根据DTA对温度的曲线,在253°
C和460.1°
C处有峰,可知在253°
C是有机杂质分解出的峰,在460.1°
C矿是无定形TiO2开始转变为锐钛矿,金红石的转变温度在800°
C
。
所以本实验制备锐钛矿设置的温度是500度,制备板钛矿(即锐钛矿和金红石的混合)的温度是650度,在此温度锐钛矿没有完全转化为金红石,制备金红石设置的温度是800度。
2.3纳米TiO2对水中Cu2+的吸附活性研究
2.3.1实验方法
1)Cu2+标准溶液配制
准确量取10mL125μg/mLCu2+标准溶液,配置成50mL溶液。
2)分别准确移取1,2,4,6,8mLCu标准溶液入125mL分液漏斗中,加水至50mL,加入50mLNH3-NH4Cl缓冲溶液,摇匀。
加入5mL铜试剂,摇匀,静置5min.加入10mLCCl4振荡2min.,静置分层,用滤纸吸去下端管口水分,塞入脱脂棉,弃去前1-2mL,以CCl4为参比,在440nm波长测定溶液的吸光度值。
3)纳米TiO2颗粒的预处理
将制的纳米TiO2颗粒浸泡于5mol/LHNO3溶液中30min,然后用二次蒸馏水洗至中性,抽滤后于100°
C下烘干。
4)在25ml比色管中加入25ug/ml的Cu2+溶液20ml,NH3调节PH值为9.0,定容至25ml。
加入20.0mg纳米TiO2,搅拌10min,静置10min后离心分离。
移取上层清液(A)待测,沉积物充分洗涤后,准确移取1mol/LHNO330ml,超声15min,静置后离心分离,移取上层清液(B)。
参比步骤
(2)测定溶液A和B的吸光度,根据工作曲线,确定溶液A和B中Cu2+的浓度。
2.3.2结果与讨论
序号
浓度ug/ml
吸光度A
吸光度△A
0.041
1
2.36
0.063
0.022
2
4.72
0.071
0.03
3
9.17
0.083
0.042
4
13.51
0.095
0.054
5
17.7
0.106
0.065
实验前:
A
4.5
B
14.5
洗脱后
A
0.066
0.025
B
0.086
0.045
洗脱后:
A的浓度(0.025-0.016)/0.002=4.5ug/ml
B的浓度(0.045-0.016)/0.002=14.5ug/ml
Cu2+在纳米TiO2表面的吸附率:
(20-4.5)/20*100%=74.55%
纳米TiO2表面Cu2+的洗脱率:
14.5/(20-4.5)*100%=98.03%
纳米TiO2对Cu2+吸附可能的机理:
二氧化钛的等电点是6.2,当PH值高于等电点时,氧化物表面被羟基覆盖而显负电。
因此,带负电的纳米二氧化钛可以吸附带正电的阳离子。
当PH值较小的酸性溶液洗脱时,较大浓度H离子把吸附在纳米二氧化钛表面的阳离子洗脱下来。
Ti-O+OH-OH--Ti-O
OH--Ti-O+Mn+(L)x+1OH--Ti-O-Mn+(L)x+L
2.4TiO2纳米晶体(锐钛矿)对甲基橙的吸附
2.4.1实验方法
1)绘制甲基橙的工作曲线
首先测定甲基橙溶液在200-800nm的紫外-可见吸收光谱,确定可见光区的最大吸收波长490nm。
配制一系列0-15mg/L不同浓度的甲基橙标准溶液,测定其吸光度,绘制工作曲线。
2)纳米TiO2(锐钛矿)对甲基橙的吸附实验
量取100mL15mg/L的甲基橙溶液于100mL带塞子的锥形瓶中,称取TiO2晶体0.01g,加入锥形瓶中,磁力搅拌10min,使混合均匀。
每隔20min,取上层清液,离心分离后测定其吸光度值,直至吸光度不再发生变化,达到吸附平衡。
3)TiO2的吸附量由Q=△C*V/m计算,△C是初始浓度与平衡浓度之差,V是溶液的体积,m是催化剂的质量。
2.4.2结果与讨论
甲基橙标准曲线
浓度C(mg/L)
0.202
6
0.433
9
0.657
12
0.877
15
1.104
起始A0
20minA1
40minA2
60minA3
80minA4
100minA5
1.068
1.028
0.994
0.986
吸光度随时间变化曲线
称取:
锐钛矿
质量/g
0.0101
平衡浓度:
C1=(0.986+0.019)/0.074=13.581mg/L
Q=△C*V/m=(15.00-13.581)/1000*0.1/0.0101=0.014
即:
1g锐钛矿能吸附0.014g甲基橙。
2.5TiO2纳米晶体(金红石)对甲基橙的吸附(自主设计)
2.5.1实验方法
1)同上,绘制甲基橙标准曲线。
2)纳米TiO2(金红石)对甲基橙的吸附实验
量取100mL15mg/L的甲基橙溶液于100mL带塞子的锥形瓶中,称取TiO2晶体0.01g,加入锥形瓶中,磁力搅拌10min,使混合均匀。
3)计算吸附量
TiO2的吸附量由Q=△C*V/m计算,△C是初始浓度与平衡浓度之差,V是溶液的体积,m是催化剂的质量
2.5.2结果与讨论
1.078
1.044
1.023
质量g
0.0108
平衡浓度:
C2=(1.023+0.019)/0.074=14.081mg/L
Q=△C*V/m=(15.00-14.081)/1000*0.1/0.0101=0.009
1g金红石能吸附0.009g甲基橙。
锐钛矿和金红石都是纳米TiO2,具有很大的表面积和复杂的空隙结构,而吸附过程正是在这些孔隙中和表面上进行的,从而使其能够吸附杂质。
象磁力一样,所有的分子之间都具有相互引力。
纳米TiO2孔壁上的大量的分子可以产生强大的引力,从而达到将介质中的杂质吸引到孔径中的目的,这就是物理吸附。
锐钛矿与金红石相比,金红石的晶格较小,致密度高,所以具有更大的稳定性和较高的密度,比表面积比锐钛矿小,所以吸附量比锐钛矿小。
2.6TiO2纳米晶体对甲基橙的光催化降解
2.6.1实验方法
分别称取三种TiO2纳米晶体0.1g,超声分散于100ml甲基橙水溶液中,反应温度为室温,光源为高压汞灯,功率为100W,垂直照射在反应液上,光源与溶液的垂直距离为20cm。
磁力搅拌器保证溶液浓度的均匀性。
每隔20分钟取少量溶液,离心分离后,取清液用紫外可见分光光度计(TU-1900)测定其吸收光谱,扫描范围从400-700nm。
根据最大吸收峰的吸光度值变化确定甲基橙的浓度变化。
以甲基橙降解率(A0-A)/A0(A0起始甲基橙的吸光度,A为t时刻甲基橙的吸光度)为纵坐标,时间为横坐标,比较三种TiO2纳米晶的光催化活性。
2.6.2结果与讨论
1)0.01g锐钛矿
1.031
0.891
0.873
0.871
甲基橙降解率:
(A0-A)/A0=(1.031-0.871)/1.031=0.916
2)0.01g金红石
0.289
0.287
0.285
(A0-A)/A0=(1.031-0.285)/1.031=0.724
3)0.08g锐钛矿+0.02g金红石
混合两种
0.047
0.045
(A0-A)/A0=(1.031-0.045)/1.031=0.956
应用能带模型可以很好的解释TiO2的光催化机理。
锐钛矿TiO2的能带宽度为
3.2eV,在波长<
400nm的紫外光照射下,产生电子-空穴对:
TiO2TiO2(e-+h+)
光生空穴(h+)即可直接与粒子表面吸附的有机分子(RX)反应,电子从有机分子转移给TiO2粒子:
TiO2(h+)+RXTiO2+RX+
h+还可接受表面吸附的溶剂分子提供的电子,发生如下的氧化反应:
TiO2(h+)+H2OTiO2+HO.+H+
由于TiO2粒子表面吸附的H2O分子和OH-的浓度较高,所以第二种氧化过程在有机物的光催化降解过程中起了重要作用。
同时表明,O2分子在TiO2的光催化过程中是一种必不可少的物质,它主要用来接受导带的光电子,产生超氧离子。
超氧离子不稳定,发生歧化反应,生成过氧化氢。
H2O2还可以接受TiO2导带的光生电子产生氢氧自由基(OH):
氢氧自由基可将吸附在TiO2颗粒表面的大多数的有既无氧化分解为CO2和H2O等无机物。
金红石由于对02的吸收能力较差,比表面积较小,所以导致光生电子和空穴容易复合,光催化活性较锐钛矿的低,但研究发现具有高光催化活性的多数为锐钛矿与金红石的混合物,这是由于此时锐钛矿表面形成了金红石薄层,这种包覆型复合结构能有效地提高电子.空穴对的分离效率,这种现象也被称之为“混晶效应”。
第三章总结与展望
本实验采用低温水合法制备纳米TiO2,高温转化为锐钛矿和金红石,研究它们对金属离子、有机物的吸附,和光催化降解能力。
TiO2作为新兴材料,无论是用来降解有机物污染物,还是用着吸附材料,都有着广泛的应用前景。
作为本实验的拓展,研究纳米TiO2对不用金属离子的吸附能力的比较,以及锐钛矿和金红石两种纳米TiO2混合催化降解能力可以再做实验,使自己对纳米TiO2有更深入的了解。
(注:
可编辑下载,若有不当之处,请指正,谢谢!
)