立克次体柯克斯体东方体巴通体Word下载.docx
《立克次体柯克斯体东方体巴通体Word下载.docx》由会员分享,可在线阅读,更多相关《立克次体柯克斯体东方体巴通体Word下载.docx(12页珍藏版)》请在冰豆网上搜索。
东方体属
恙虫病群
恙虫病东方体(O.tsutsugamushi)
恙虫病
恙螨
野鼠等
柯克斯体属
贝纳柯克斯体(C.burnetii)
Q热
野生小动物、牛和羊等
埃立克体属
犬埃立克体群
查非埃立克体(E.chaffeensis)
人单核细胞埃立克体病
啮齿类
腺热埃立克体群
腺热埃立克体(E.sennetsu)
腺热埃立克体病
嗜吞噬细胞埃立克体群
人粒细胞埃立克体(HGE)
人粒细胞埃立克体病
人、马和狗
巴通体属
五日热巴通体(B.quintana)
战壕热、杆菌性血管瘤
汉赛巴通体(B.henselae)
猫抓病
-
猫和狗
立克次体、东方体、柯克斯体、埃立克体和巴通体属的共同特点是:
①大多数是人畜共患病的病原体;
②以节肢动物为宿主和传播媒介,引起人类发热出疹性疾病;
③体积介于细菌与病毒之间,用光学显微镜可见,形态以球杆状或杆状为主,革兰染色阴性;
④专性细胞内寄生,因酶系统不够完善又缺乏细胞器,故不能独立生活;
⑤以二分裂方式繁殖;
⑥含有DNA和RNA两种核酸;
⑦对多种抗生素敏感。
这类病原所致疾病绝大多数为自然疫源性疾病,动物受染后一般不出现症状。
人类因生产劳动、资源开发等偶然遭到嗜血节肢动物的侵袭而受染。
流行性斑疹伤寒、地方性斑疹伤寒和Q热在世界各地均有发生;
斑点热主要流行于北美和西伯利亚等地区;
人粒细胞埃立克体病流行于北美;
恙虫病主要流行于东南亚和西南太平洋等地区。
我国较常见的立克次体病有流行性斑疹伤寒、地方性斑疹伤寒、恙虫病和Q热等。
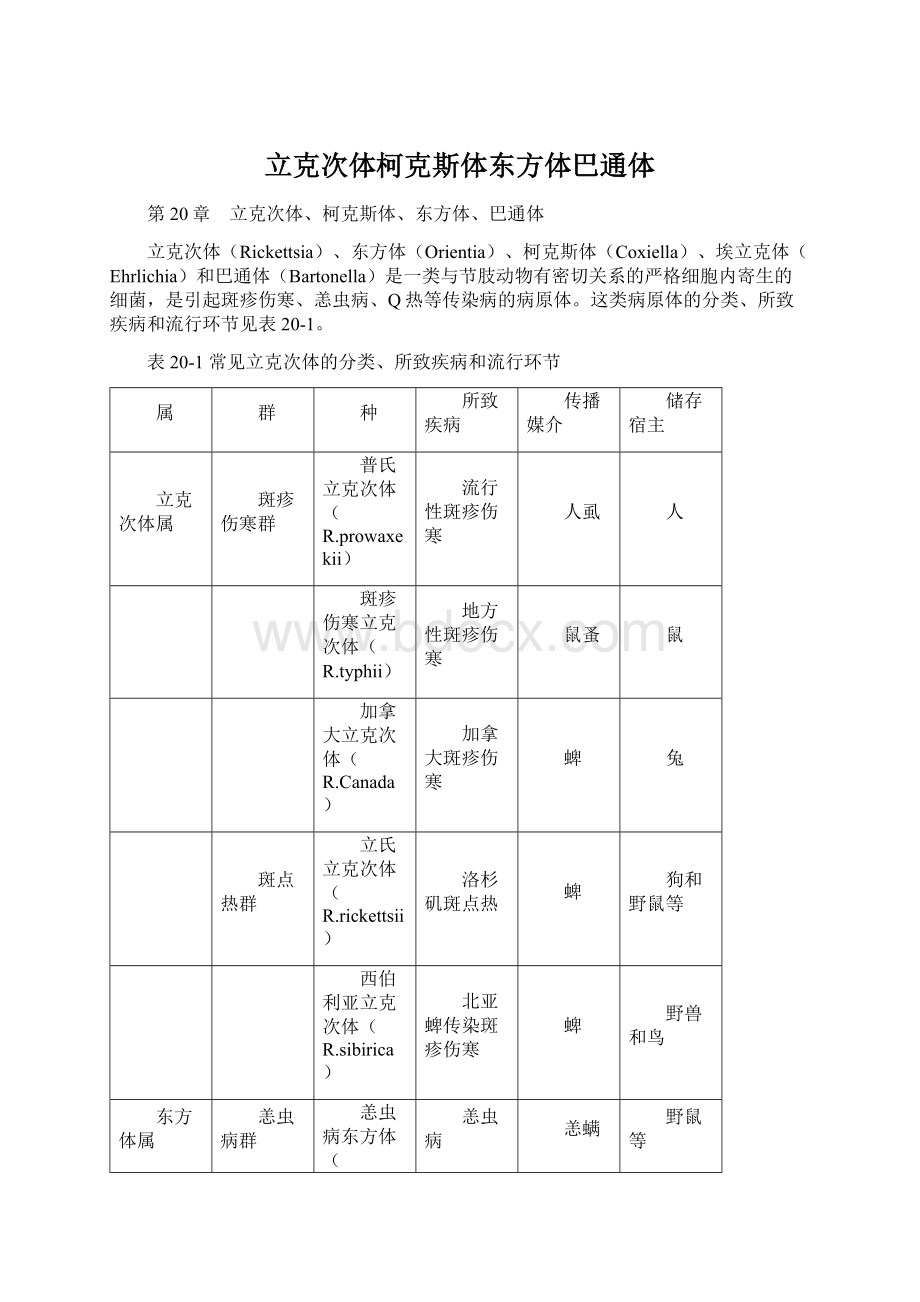
常见立克次体的主要生物学性状见表20-2。
表20-2常见立克次体的主要生物学性状
立克次体种类
培养特性
二分裂
生长分布的位置
灭活温度(℃)
与时间(分钟)
外斐反应
普氏立克次体
活细胞内增殖
+
分散细胞质内
56
30
OX19+++OX2+OXK-
斑疹伤寒立克次体
分散细胞内外
立氏立克次体
细胞质和核质区
恙虫病东方体
近核处成堆
OX19-OX2-OXK+++
贝纳柯克斯体
吞噬溶酶体内
100
10
OX19-OX2-OXK-
第一节普氏立克次体
普氏立克次体(R.prowazekii)是流行性斑疹伤寒(虱传斑疹伤寒或称典型斑疹伤寒)的病原体,用为研究斑疹伤寒而献身的捷克科学家Vonprowazek的姓氏命名。
流行性斑疹伤寒在世界各地均可发生流行。
一、生物学性状
(一)形态结构与染色
普氏立克次体呈多形态性,以短杆形为主,大小为长0.6~2.0m,宽0.3~0.8m,在胞质内呈单个或短链状存在(图20-1)。
革兰染色阴性,着色较淡。
常用Gimé
nez法染色呈鲜红色,效果好;
姬姆萨法染色呈紫色或蓝色;
Macchiavello法染色呈红色。
图20-1普氏立克次体
(二)结构与抗原构造
普氏立克次体与其它立克次体的结构均与革兰阴性菌相似,有细胞壁和细胞膜。
细胞壁由肽聚糖、蛋白脂质多糖和外膜组成,其脂质含量高于一般细菌。
细胞壁外有脂多糖,外表有多糖组成的微荚膜样粘液层,微荚膜样粘液层具有粘附宿主细胞和抗吞噬的作用,与致病性有关。
细胞膜由脂质双层构成,含有大量的磷脂。
细胞质中的核糖体由50S和30S大小两种亚基组成,双链DNA构成的核质区位于中央。
立克次体细胞壁有两类抗原,一类为群特异性的可溶性抗原,可能是细胞壁的脂多糖成分,耐热;
另一类为种特异性抗原,为细胞壁外膜蛋白,不耐热。
立克次体的脂多糖成分与变形杆菌某些X株菌体抗原有共同成分(有相同或相似的抗原决定簇),可引起交叉反应。
根据这一原理,用易于制备的变形杆菌O抗原代替相应立克次体抗原建立一种非特异性直接凝集实验,称外斐反应(Weil-Felixreaction),用于检测患者体内是否有抗立克次体抗体,以辅助诊断斑疹伤寒、斑点热和恙虫病。
(三)培养特性
普氏立克次体和绝大多数立克次体为专性活细胞内寄生,只有在活的细胞内才能生长,以二分裂方式繁殖,繁殖一代需要6~l0小时,生长缓慢。
培养立克次体的方法有动物接种、鸡胚接种和细胞培养。
动物接种是最常用的方法,可采用豚鼠和小鼠,多种病原性立克次体在豚鼠和小鼠体内生长繁殖良好。
鸡胚卵黄囊接种常用于立克次体的传代培养。
目前采用鸡胚成纤维细胞、L929细胞和Vero单层细胞进行分离、鉴定、传代和培养,最适温度为37℃。
(四)抵抗力
普氏立克次体对理化因素的抵抗力较弱,对热敏感,56℃30分钟可杀死(表20-2),在水溶液中4℃24小时失去活性;
耐低温和干燥,在干虱粪中能保持活性两个月左右。
0.5%石碳酸和来苏5分钟可灭活。
对四环素类和氯霉素类抗生素敏感。
磺胺可刺激其增殖。
二、致病性与免疫性
(一)感染途径
普氏立克次体的储存宿主是病人,传播媒介是人虱,病人是惟一的传染源。
感染方式是虱-人-虱-人。
人虱叮咬病人,立克次体进人人虱体内,在肠管上皮细胞内生长繁殖,破坏肠管上皮细胞,并随粪便排出体外,感染7~10天后死亡。
当感染的人虱叮咬健康人时,立克次体随粪便排泄于人的皮肤上,由于瘙痒而抓伤,立克次体便可侵入人体内致病(图20-2)。
由于立克次体的感染性在干燥的虱粪中能保持两个月左右,亦有可能通过呼吸道或球结膜发生感染。
图20-2流行性斑疹伤寒的传播方式
(二)致病物质
普氏立克次体的致病物质主要有内毒素和磷脂酶A两类。
内毒素的化学成分为脂多糖,具有与肠道杆菌内毒素相似的多种生物学活性。
可刺激单核-巨噬细胞产生IL-1和TNF-。
IL-1具有致热性,引起发热;
TNF-引起血管内皮细胞损伤、微循环障碍、中毒性休克和DIC等。
磷脂酶A能溶解宿主细胞膜或吞噬体膜,有利于立克次体穿入宿主细胞内生长繁殖。
此外,微荚膜样粘液层有利于粘附于宿主细胞,并具有抗吞噬作用。
(三)所致疾病
普氏立克次体所致疾病为流行性斑疹伤寒。
当普氏立克次体侵入皮肤后,与局部淋巴组织或小血管内皮细胞表面特异性受体结合而被吞入胞内,依靠磷脂酶A溶解吞噬体膜的甘油磷脂进入细胞质内大量增殖,导致细胞中毒破裂,释放出立克次体,引起第一次立克次体血症。
立克次体经血流扩散至全身组织器官的小血管内皮细胞,在其中大量增殖释放入血,导致第二次立克次体血症。
普氏立克次体通过磷脂酶A和微荚膜样粘液层对抗宿主的免疫作用,大量增殖破坏宿主细胞。
立克次体崩解释放内毒素等毒性物质,形成毒血症。
损害血管内皮细胞,造成肿胀和坏死,通透性增强,血浆渗出,有效循环血量下降。
其主要病理改变为血管内皮细胞增生,血管壁坏死,血栓形成。
造成皮肤、心、肺和脑等血管周围的广泛性病变。
流行性斑疹伤寒的潜伏期为10~14天,发病急、高热、剧烈头痛和周身疼痛,4~7天出现皮疹。
婴幼儿发病率低,多见成年人感染,50岁以上的人发病率高,60岁以上的患者死亡率高。
(四)免疫性
普氏立克次体严格细胞内寄生,抗感染以细胞免疫为主,体液免疫为辅。
CTL细胞溶解杀伤感染立克次体的血管内皮细胞,THl细胞释放细胞因子IFN-增强MΦ的吞噬和杀伤功能;
B细胞产生的群和种抗体有促进吞噬细胞的吞噬作用,中和立克次体的感染性和毒性物质。
同时,免疫作用也增加了对机体的病理性损害。
由于二次立克次体血症,病后获得牢固的免疫力,与斑疹伤寒立克次体的感染有交叉免疫力。
三、微生物学检查法
普氏立克次体的微生物学检查法主要为分离和鉴定,对临床确诊和流行病学调查有意义。
(一)标本采集
一般在发病期或急性期尚未用抗生素之前无菌采血以提高阳性分离率。
流行病学调查则采取野生小动物、家畜脏器或节肢动物的组织悬液。
(二)分离培养
由于标本中立克次体含量较低,直接镜检意义不大。
可将标本尽快接种在雄性豚鼠的腹腔内,接种后若体温>
40℃或阴囊有红肿,表示已发生感染;
若无阴囊红肿而体温超过40℃,可取脾组织接种鸡胚卵黄囊,35℃孵育数日,如卵黄囊膜涂片查见立克次体可能即为普氏立克次体,并根据形态、细胞内部位及免疫荧光法等进行鉴定。
(三)血清学检测
常用外斐反应和补体结合试验。
外斐反应(变形杆菌OXl9抗原)的滴度≥1∶160或恢复期抗体滴度比早期增高≥4倍者可诊断为斑疹伤寒。
但要结合临床症状,以排除外斐反应假阳性。
用普氏立克次体可溶性(群特异)抗原进行的补体结合试验可区别斑疹伤寒和其他群的立克次体感染,而要区别普氏与斑疹伤寒立克次体还需用种特异性抗原。
(四)分子生物学检测
可应用PCR检测或核酸探针检测。
四、防治原则
(一)预防原则
流行性斑疹伤寒的预防主要应改善生活条件,讲究个人卫生,消灭体虱,加强个人防护。
特异性预防采用由γ射线辐射或甲醛处理的灭活鼠肺疫苗和鸡胚疫苗等,可使发病率降低70%~90%,免疫力可持续一年。
(二)治疗原则
氯霉素和四环素类抗生素对普氏立克次体和其它立克次体均有效,可缩短病程,降低死亡率。
但是,抗生素的作用是有限的,增强机体免疫力,提高细胞免疫功能是治疗的关键。
禁用磺胺类药物治疗。
第二节斑疹伤寒立克次体
斑疹伤寒立克次体(R.typhi)或称莫氏立克次体(R.mooseri)是地方性斑疹伤寒(亦称鼠型斑疹伤寒)的病原体。
1931年,Mooser等分别从该疾病流行的墨西哥的鼠脑和美国的鼠虱中分离出来。
地方性斑疹伤寒可在世界各地散发,而主要发生在非洲和南美洲。
斑疹伤寒立克次体大小形态同普氏立克次体,但链状排列少见。
染色性、结构、抗原构造、培养特性、抵抗力以及易感细胞、易感动物方面与普氏立克次体相同,只是斑疹伤寒立克次体所致的豚鼠阴囊反应比普氏立克次体引起的更强。
二、致病性和免疫性
斑疹伤寒立克次体的主要储存宿主是鼠,主要传播媒介是鼠蚤和鼠虱,感染的自然周期是鼠—蚤—鼠。
立克次体长期寄生于隐性感染鼠体,鼠蚤吸疫鼠血后,立克次体进入其消化道并在肠上皮细胞内繁殖,细胞破裂后将立克次体释出,混入蚤粪中,在鼠群间传播。
鼠蚤只在鼠死亡后才离开鼠转向叮吮人血,而使人受感染。
此外,带有立克次体的干燥蚤粪还可经口、鼻及眼结膜进入人体而致病(图20-3)。
鼠
人
鼠蚤
图20-3斑疹伤寒立克次体的传播方式
(二)所致疾病
致病物质同普氏立克次体,所致疾病为地方性斑疹伤寒,其临床症状与流行性斑疹伤寒相似,但发病缓慢,常经过8~12天的潜伏期后出现发热和皮疹,病情较轻,很少累及中枢神经系统和心肌,病死率低于1%。
(三)免疫性
斑疹伤寒立克次体严格细胞内寄生,以细胞免疫为主,体液免疫为辅。
可出现二次立克次体血症,病愈后能获得牢固的免疫力,与普氏立克次体的感染有交叉免疫力。
接种雄性豚鼠腹腔,若有斑疹伤寒立克次体的感染可出现发热,同时伴有明显的阴囊红肿和鞘膜反应(Neill-Mooserreaction)。
余同普氏立克次体。
预防措施主要是要改善居住条件,提高民族素质,讲究个人卫生,灭虱、灭蚤和灭鼠。
接种疫苗。
治疗原则同流行性斑疹伤寒。
第三节恙虫病东方体
恙虫病东方体(O.tsutsugamushi)是恙虫病的病原体。
国外最早系日本人于1810年首先描述本病。
1927年日本学者绪方规雄等用病人血液注射家兔睾丸内,经5~6次传代后,阴囊红肿,取其涂片染色发现。
1948年我国国内(广州)分离出恙虫病东方体。
该病主要流行于东南亚、西南太平洋岛屿、日本和我国的东南与西南地区。
(一)形态、染色与结构
呈双球或短杆状,多成对排列,平均长度为1.2m,很少超过1.5m。
Gimé
nez法染色呈暗红色;
革兰染色法、姬姆萨染色法和Macchiavello染色法其染色特性与普氏立克次体相同。
细胞壁的结构和抗原成分不同于其它立克次体,无粘液层,无微荚膜,无肽聚糖和脂多糖,与变形杆菌OXK有交叉抗原。
故恙虫病立克次体现另立为东方体属。
(二)培养特性
小鼠易感,可在鸡胚卵黄囊和细胞培养中生长。
常用的原代细胞有地鼠肾细胞、睾丸细胞等,传代细胞有HeLa、L929等。
(三)抵抗力
在外环境中的抵抗力较其它立克次体为低,低温可长期保存,-20℃能存活5周,56℃10分钟即被杀灭;
37℃2~3小时后,其活力大为下降;
对一般消毒剂极为敏感。
恙虫病是一种自然疫源性疾病,主要流行于啮齿动物之间。
野鼠和家鼠感染后多无症状,但体内长期保留病原体,故为主要传染源。
此外,兔类、鸟类等也能感染或携带恙螨而成为传染源。
恙螨是恙虫病东方体的寄生宿主、储存宿主和传播媒介,立克次体寄居在恙螨体内,可经卵传代,并借助于恙螨的叮咬在鼠间传播。
所致疾病为恙虫病。
人若被恙螨叮咬后,经7~10天或更长的潜伏期,突然发病,高热,剧烈头痛,可出现耳聋。
于叮咬处出现红斑样皮疹,形成水疱,破裂后发生溃疡,周围红润,上覆黑色痂皮(称为焦痂),是恙虫病的特征之一。
病原体在宿主细胞内繁殖,多在细胞质近核处成堆排列,然后通过出芽方式释放,经淋巴系统入血循环,产生东方体血症。
病原体释出的毒素,可引起发热、皮疹、全身淋巴结肿大及各内脏器官的病变。
以细胞免疫为主,病后获得较持久的免疫力。
(一)病原体分离
取急性期病人血液接于小鼠腹腔,濒死时取腹膜或脾脏作涂片,经姬姆萨染色或荧光抗体染色镜检。
(二)血清学检查
1.外斐反应 病人单份血清对变形杆菌OXk凝集效价在1∶160以上或早晚期双份血清效价呈4倍增长者有诊断意义。
最早第4天出现阳性,3~4周达高峰,5周后下降。
2.补体结合试验 应用当地代表株或多价抗原,特异性高,抗体持续时间长,可达5年左右。
效价1∶10为阳性。
3.间接免疫荧光试验 测定血清抗体,于起病第1周末出现抗体,第2周末达高峰,阳性率高于外斐反应,抗体可持续10年,对流行病学调查意义较大。
在流行区要加强个人防护,防止恙螨幼虫叮咬,灭鼠除草,加快疫苗研制。
治疗同普氏立克次体。
第四节贝纳柯克斯体
贝纳柯克斯体(C.burnetii)亦称Q热柯克斯体,是Q热(queryfever)的病原体。
Q热即疑问热,指原因不明的发热。
1937年,Burnet等证明其病原体是一种立克次体,命名为贝纳柯克斯体。
Q热流行于世界各地。
(一)形态与染色
贝纳柯克斯体呈高度多形性,球杆形或短杆形,甚至球形。
大小为长0.2~1.0m,宽0.2~0.4m,是目前发现的最小的立克次体。
革兰染色多为阴性,其他染色特性同普氏立克次体。
鸡胚卵黄囊中生长旺盛,能在多种细胞中繁殖。
(二)基因组特征
贝纳柯克斯体基因组分子量为1.04×
109,含1.6×
106bp,约为大肠埃希菌的1/3。
近年来已分离其基因达13个之多,分别与编码立克次体代谢酶有关(如PyrB、gitA、sdhCDAB基因),或与编码表面抗原有关(chtpA、tpB、ComI基因),或与编码毒力因子有关(Sod、Mucz、CbbE、Cbmip、dnaJ、qrsA基因)。
此外,还发现贝纳柯克斯体带有4种不同的质粒,分别为36kbQpHI、39kbQpRS、33.5kbQpDV和51kbQPDG,其功能尚未阐明。
(三)抗原结构
贝纳柯克斯体有抗原相的变异,发生变异的主要成分为脂多糖。
新分离的病原体为Ⅰ相,毒力强,含有完整的抗原组份;
经人工传代后失去Ⅰ相中的表面抗原而成为毒力弱的Ⅱ相。
Ⅱ相又可通过动物接种回复至Ⅰ相。
贝纳柯克斯体抵抗力较强。
耐热,牛乳需煮沸10分钟以上才能杀死。
耐干燥,在蜱干粪中可存活一年以上。
1%甲醛需48小时才能将其灭活。
贝纳柯克斯体在蜱体内能长期存活,并可经卵传代。
随粪便排出,粪便中含有大量病原体。
蜱既是寄生宿主和储存宿主,又是动物间的传播媒介。
蜱叮咬野生啮齿动物和家畜使其感染成为中间储存宿主。
受感染家畜多数无症状,却是主要传染原,乳汁、尿、粪中可长期带有病原体,由消化道或呼吸道接触感染人。
Q热的潜伏期一般为14~28天,症状类似流感或原发性非典型肺炎,发病突然,高热寒战,常有剧烈头痛、肌肉疼痛和食欲减退,很少出现皮疹。
轻者可自愈,重症病例如并发肝炎、心内膜炎。
病后可获得一定免疫力,且以细胞免疫为主。
分离病原体可采血进行豚鼠腹腔接种,发热后取脾脏作涂片染色检查。
还可选用鸡胚卵黄囊或细胞培养。
如外斐试验阴性,可用补体结合试验或凝集试验检查血中有无特异性抗体以协助诊断。
一般急性病人只产生Ⅱ相抗体。
若Ⅰ相抗体持续较高水平,说明感染仍然存在,为慢性或隐性感染。
预防重点在于消除家畜的感染,对可疑乳制品严格消毒。
对易感人群可接种用Ⅰ相菌株制成的灭活或减毒疫苗,有一定效果。
对牛、羊也可接种疫苗。
治疗可用四环素和氯霉素。
第五节汉赛巴通体
汉赛巴通体(B.henselae)是猫抓病(catscratchdisease,CSD)的主要病原体。
汉赛巴通体形态多样,主要为杆状,大小为1×
0.5m左右。
革兰染色阴性,姬姆萨染色呈蓝紫色,镀银染色呈棕黄色。
由临床新鲜标本中分离的汉赛巴通体有菌毛,而经实验室传代后可丧失。
其生化反应不活泼,不发酵各种糖类。
传染源主要为猫和狗,尤其是幼猫。
90%以上的患者与猫或狗有接触史,75%的病例有被猫或狗抓伤、咬伤的历史,猫口腔、咽部的病原体经伤口或通过其污染的毛皮、脚爪侵入而传播,多发于学龄前儿童及青少年。
由于近年来国内外养宠物者增多,因此猫抓病病例增加。
病原体从抓伤处进入体内,局部皮肤出现丘疹或脓疱,继而发展为以局部引流淋巴结肿大为特征的临床综合征,出现发热、厌食、肌痛、脾肿大等。
常见的临床并发症是结膜炎伴耳前淋巴结肿大(Parinaud眼淋巴腺综合征),系猫抓病的重要特征之一。
汉赛巴通体尚可引起免疫功能低下的患者杆菌性血管瘤—杆菌性紫癜(bacillaryangiomatosis-bacillarypeliosis,BAP),主要表现为皮肤损害和内脏器官小血管增生。
BAP可见于HIV感染者、肿瘤或器官移植的病人,其杆菌性血管瘤可发生在体内任何实质性器官,而杆菌性紫癜则多见于肝脏、脾脏。
实验室检查可取病灶组织(淋巴结、皮肤、肉芽肿等)作超薄切片,进行组织病理学检查。
此外,还可用羊血琼脂或巧克力色琼脂等培养基,或采用原代细胞或传代细胞,对新鲜组织标本培养和鉴定。
对宠物定期检疫,杀灭感染动物。
与猫、狗接触时避免被抓伤或咬伤,若被抓、咬伤后,可用碘酊局部消毒。
可采用环丙沙星、红霉素、利福平等治疗感染猫或病人。