九年级下学期期中化学试题Word格式.docx
《九年级下学期期中化学试题Word格式.docx》由会员分享,可在线阅读,更多相关《九年级下学期期中化学试题Word格式.docx(10页珍藏版)》请在冰豆网上搜索。
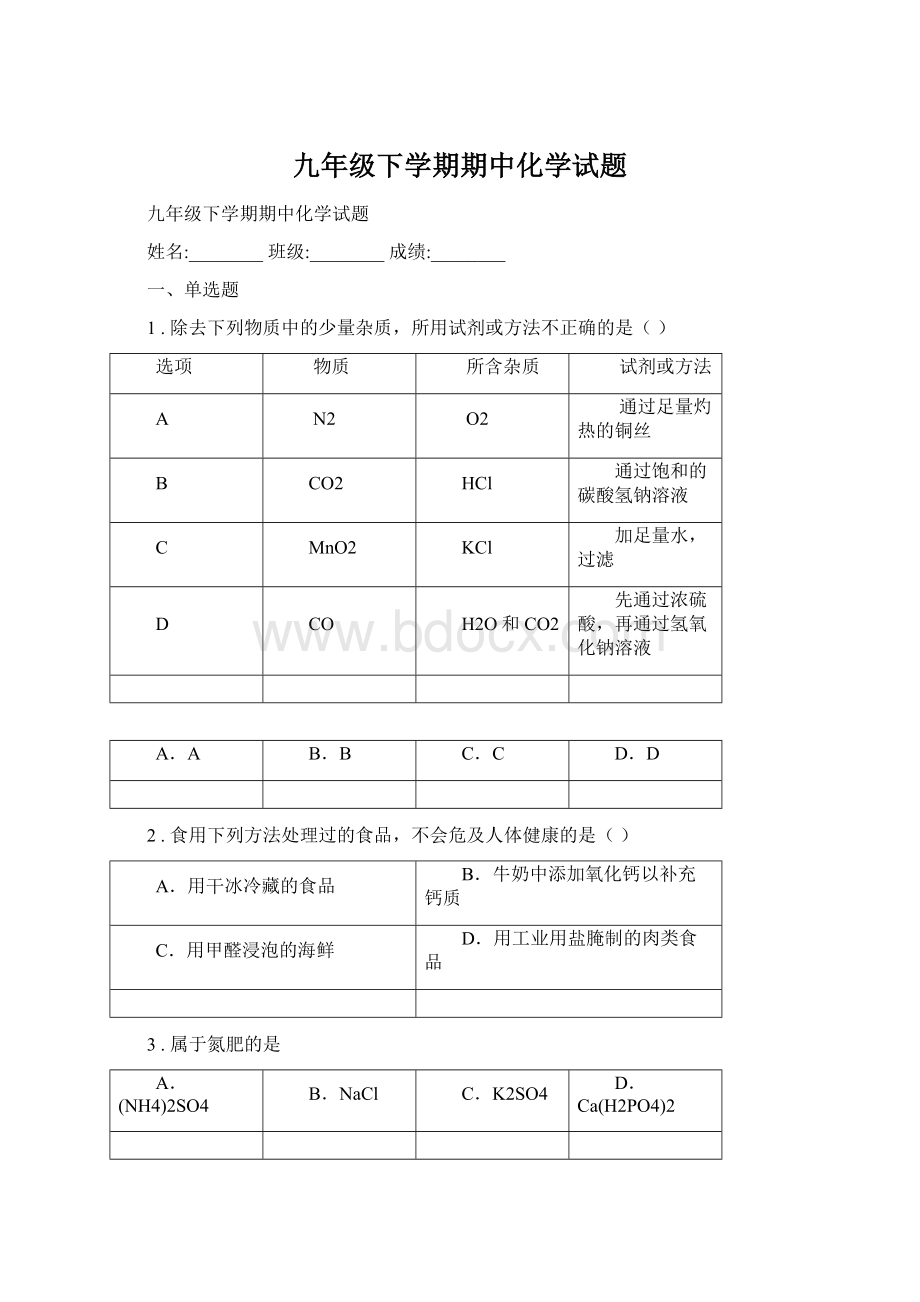
D
CO
H2O和CO2
先通过浓硫酸,再通过氢氧化钠溶液
A.A
B.B
C.C
D.D
2.食用下列方法处理过的食品,不会危及人体健康的是()
A.用干冰冷藏的食品
B.牛奶中添加氧化钙以补充钙质
C.用甲醛浸泡的海鲜
D.用工业用盐腌制的肉类食品
3.属于氮肥的是
A.(NH4)2SO4
B.NaCl
C.K2SO4
D.Ca(H2PO4)2
4.下列各组离子在水中能大量共存的是
A.H+、K+、SO42-、Cl-
B.H、Ba2+、Cl、OH-
C.NH4+、Ag+、Cl-、NO3-
D.Na+、H+、NO3-、CO32-
5.制作蛋糕的人造奶油中含有影响身体发育的反式脂肪酸(C18H34O2),下列关于反式脂肪酸的说法正确的是()
A.该物质由碳、氢、氧三个元素组成
B.该物质在空气中完全燃烧的产物只有CO2和H2O
C.该物质中C、H、O三种元素的质量比为9:
17:
1
D.该物质是由18个碳原子、34个氢原子和2个氧原子构成的
6.下列变化中,属于化学变化的是
A.铁钉生锈
B.冰雪融化
C.香水挥发
D.氮气液化
7.下列关于原子、分子的说法不正确的是()
A.分子可以构成物质,而原子只能构成分子
B.在化学变化中,分子可以分成原子,而原子不能再分
C.在原子中,质子数等于核外电子数
D.分子是保持物质化学性质的一种粒子
8.下列实验操作错误的是
9.青铜是人类最早使用的铜、锡合金,下列说法中正确的是()
A.青铜属于纯净物
B.青铜的熔点介于铜、锡的熔点之间
C.青铜的硬度比铜小
D.青铜耐腐蚀,易铸造成形
二、多选题
10.等质量的X、Y两种金属分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如图所示。
下列说法中不正确的是()(已知X、Y在化合物中均为+2价)
A.两种金属的相对原子质量:
X<Y
B.t1时,消耗盐酸的质量:
X=Y
C.t2时,消耗金属的质量:
X>Y
D.t3时,消耗金属的质量:
三、选择填充题
11.欲除去下列物质中的少量杂质(括号内为杂质),所采取的方法正确的是_____。
加入的试剂或操作
NaCl溶液(CaCl2)
过量的碳酸钠溶液,过滤
CaCO3(CaO)
高温煅烧
C
Cu(NO3)2溶液(AgNO3)
足量铜粉,过滤
NaOH溶液(Ca(OH)2)
_____
12.如图所示,将铁丝插入试管中,一段时间后取出铁丝,洗净、干燥、称量,铁丝的质量增加,则试管中所装的溶液是________
A稀硫酸
B硫酸铜溶液
C硫酸锌溶液
D_____________
13.在伦敦奥运会中,下列体育器材中,使用了合成材料的是_________
A铁饼
B皮划艇
C铅球
D_________.
14.物质的组成和结构决定了物质的性质。
下列解释合理的是______。
A.稀盐酸与稀硫酸的化学性质相似的原因是都含有酸根离子
B.生铁与钢的性能不同的主要原因是含碳量不同
C.二氧化碳与一氧化碳的化学性质不同的原因是原子个数不同
D.金刚石与石墨的物理性质差异大的原因是______。
15.下列含碳元素的物质中,属于有机物的是_____
AK2CO3
BC2H3OH
CH2CO3
D_____
四、填空题
16.生活中处处有化学,结合所学知识回答下列问题。
(1)从分子的角度解释:
墙内开花墙外香的原因是_____。
(2)用硬水洗衣服,既浪费肥皂也洗不干净衣服,生活中可把硬水软化成软水的方法是_____。
(3)雾霾天气,人们常戴PM2.5专用口罩,此口罩中的活性炭具有_____作用。
17.写出符合要求的化学方程式:
(1)电解水_____;
(2)氯酸钾制氧气_____;
(3)一氧化碳还原氧化铁_____;
(4)二氧化碳使澄清的石灰水变浑浊的化学方程式为_____。
18.下列数据是硝酸钾固体在不同温度时的溶解度:
温度/℃
20
40
60
80
溶解度/g
13.3
31.6
63.9
110
169
(1)20℃时,向100g水中加入31.6g硝酸钾,充分溶解后得到_______(填“饱和”或“不饱和”)溶液.
(2)60℃时,l00g水中加入150g硝酸钾,若使硝酸钾完全溶解,可以采用的方法是_______.
(3)如图所示,小烧杯中盛放的是
(1)中所得的硝酸钾溶液.若将少量的下列物质分别加入到大烧杯的水中,一定能够使小烧杯中有固体析出的是_______(填字母).
ANaOH
B浓H2SO4
CNH4NO3
DCaO
19.曾有新闻报道:
南部多地普遍降雪,路政部门在道路、桥梁等处堆放了融雪用的工业盐,做好应急准备。
令人意外的是,工业盐被村民当作食盐搬回家准备腌菜。
工业盐中常含有亚硝酸钠(NaNO2),具有较强毒性,亚硝酸钠外观极像食盐,且具有与食盐一样的咸味。
(1)比较氯化钠和亚硝酸钠的化学式,可推断亚硝酸钠组成成分中的____(用化学符号表示,下同)有剧毒。
(2)15℃时,各取两种固体50g,分别加入100g水中,充分搅拌后,得到饱和溶液的是__。
(3)将两者分别加热到320℃,不分解的是食盐,能分解并放出一种具有刺激性气味气体的是亚硝酸钠,该气体可能是__(填字母序号)。
A.NH3
B.SO2
C.NO2
D.N2
(4)写出亚硝酸钠与盐酸反应的化学方程式:
__。
(5)请你再设计一种鉴别亚硝酸钠与氯化钠的方法,写出实验操作、现象与结论。
实验操作
现象与结论
____________________
__________________________
五、实验题
20.
(1)实验室用高锰酸钾制取氧气的化学方程式为____。
(2)证明收集到的气体为氧气的方法是_____。
(1)用大理石和稀盐酸制取二氧化碳的化学方程式为____。
(2)检验二氧化碳已经收集满的方法是_____。
六、简答题
21.(7分)某化学小组同学为了测定实验室一瓶稀盐酸中溶质的质量分数。
他们用铜锌合金和此稀盐酸完成了如图的实验。
请回答:
(1)生成氢气的质量为
。
(2)合金中铜的质量为多少?
该瓶稀盐酸中溶质的质量分数为多少?
(3)实验完成后,向烧杯中再加入多少克水,能得到10%的氯化锌溶液?
七、流程题
22.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
回答问题:
(1)反应③的化学方程式为____________。
该反应的基本类型属于____________反应。
(2)反应②的化学方程式为____________。
(3)整个生产过程中可循环利用的物质是____________(填化学式)。
八、科学探究题
23.甲、乙、丙三位同学对一瓶实验室久置的NaOH溶液变质程度进行实验探究。
(1)甲同学取少量该溶液于试管中,滴加2~3滴酚酞溶液,观察到_____,他认为该溶液未变质。
(2)乙同学查阅资料获知,Na2CO3溶液遇指示剂变色与NaOH溶液相同,认为甲同学的检验方法不正确。
乙同学取少量该溶液于试管中,加入足量稀盐酸,观察到_____,他认为已完全变质。
写出此现象的化学方程式_____。
(3)丙同学认为乙同学的实验结论不严谨,他的猜想是_____。
他用如下实验方案来证明自己的猜想:
①取少量该溶液于试管中,先加入足量的BaCl2溶液,产生白色沉淀,说明原溶液中存在_____。
(填化学式)
②静置后取上层清液于另一支试管中,加入2~3滴酚酞溶液,观察到溶液变红色,说明原溶液中存在_____。
24.为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1~2.5g进行系列实验。
(查阅资料)①氧化铜(CuO)为黑色固体。
②碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;
氧化亚铜为红色固体,能与稀硫酸反应:
Cu2O+H2SO4=CuSO4+H2O+Cu
(进行实验)
实验1:
取质量比1:
11的木炭粉和氧化铜混合物1.3g,进行实验。
序号
1-1
1-2
装置
反应后物质的颜色、状态
黑色粉末中混有少量红色固体
红色固体有金属光泽,混有极少量,黑色物质
实验2:
取一定量的混合物,用1—2装置进行实验。
木炭粉与氧化铜的质量比
2-1
1:
9
红色固体有金属光泽
混有少量黑色物质
2-2
10
混有很少量黑色物质
2-3
11
混有极少量黑色物质
2-4
12
无黑色物质
2-5
13
混有较多黑色物质
(解释与结论)
(1)配平化学方程式:
___C+___CuO高温___Cu+___CO2↑。
(2)实验1—2中,证明产生CO2的现象是_______________________。
(3)实验1的目的是__________。
(4)实验2的结论是_____________。
(反思与评价)
(5)实验2没有进行质量比为1:
14的实验,理由是________________。
(6)为检验2—4的红色固体中是否含Cu2O,所需试剂是__________。
参考答案
1、
2、
3、
4、
5、
6、
7、
8、
9、