《盐 化肥》全章知识复习与巩固练习Word格式文档下载.docx
《《盐 化肥》全章知识复习与巩固练习Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《《盐 化肥》全章知识复习与巩固练习Word格式文档下载.docx(17页珍藏版)》请在冰豆网上搜索。
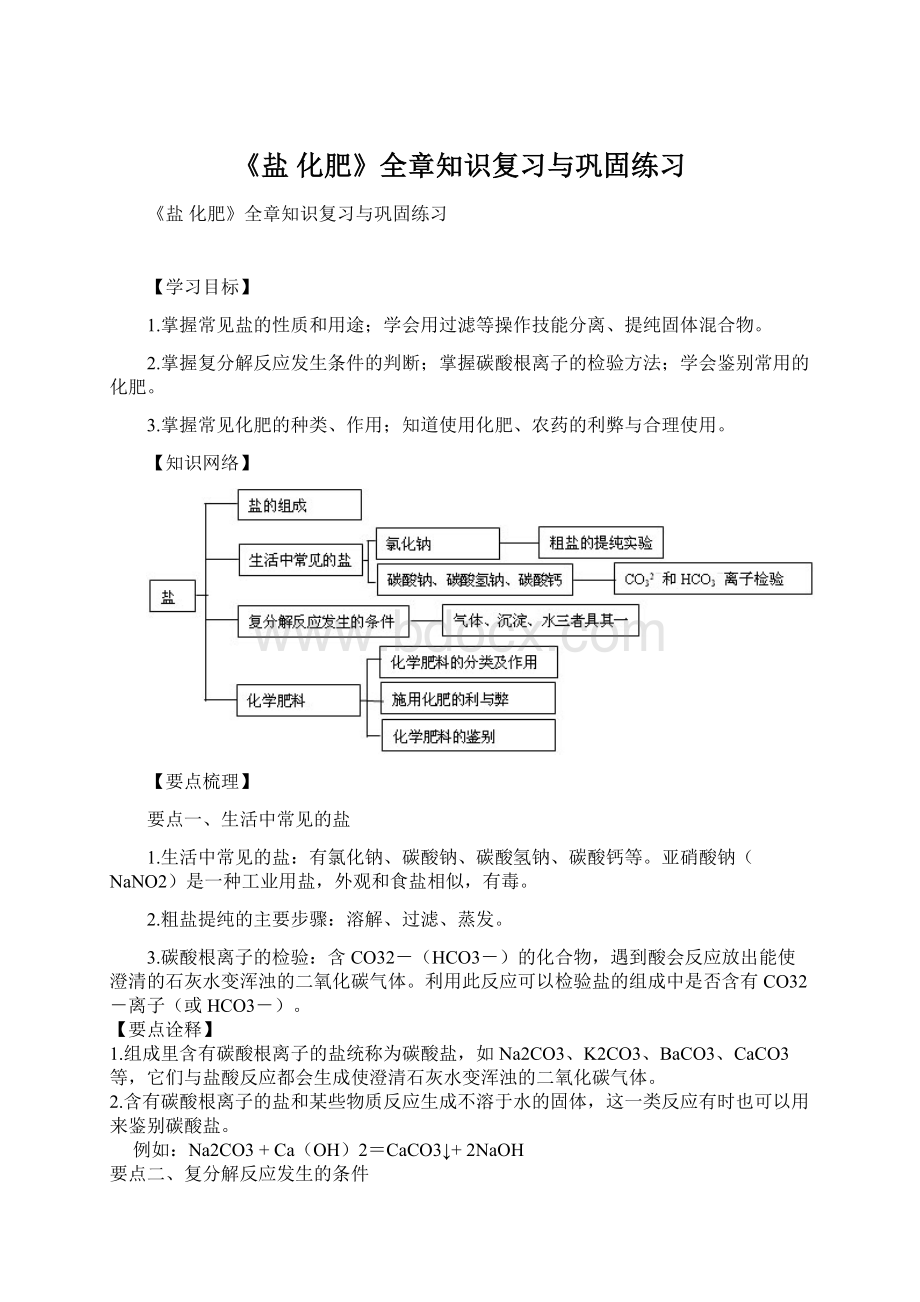
生成物有沉淀或气体或水
CaCO3+2HCl=CaCl2+H2O+CO2↑
HCl+AgNO3=AgCl↓+HNO3
H2SO4+BaCl2=BaSO4↓+2HCl
碱+盐→新碱+新盐
反应物都必须能溶于水。
2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
3NaOH+FeCl3=Fe(OH)3↓+3NaCl
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
盐+盐→新盐+新盐
Na2SO4+BaCl2=BaSO4↓+2NaCl
CaCl2+Na2CO3=CaCO3↓+2NaCl
金属+盐→新金属+新盐
反应物中盐要可溶于水,在金属活动性顺序中,排在前面的金属可以把排在后面的金属从它的盐溶液中置换出来
Fe+CuSO4=FeSO4+Cu
Cu+2AgNO3=2Ag+Cu(NO3)2
Mg+FeSO4=Fe+MgSO4
盐与酸反应、盐与碱反应、盐与盐反应都属于复分解反应,盐与金属反应属于置换反应。
要点四、化学肥料
1.农作物所必需的营养元素:
有多种,其中氮、磷、钾需要量最大;
因此氮肥、磷肥和钾肥是最主要的化学肥料。
2.复合肥料:
是指含有两种或两种以上营养元素的化肥。
如KNO3含有钾元素和氮元素两种营养元素,属于复合肥料。
3.氮肥的简易鉴别:
(1)氮肥中的氨水是液态的,碳酸氢铵有强烈的刺激性气味,据此可直接将它们与其他的氮肥相区别。
(2)铵态氮肥能与碱反应,放出氨气,氨气能使湿润的红色石蕊试纸变为蓝色。
常用此法检验铵态氮肥。
4.化肥和农药:
对提高农作物的产量有重要作用;
但不合理的使用化肥和农药,不仅难以实现增产效益,还会带来环境问题。
如造成对土壤、水源、大气的污染等。
5.使用化肥的注意事项:
种类
性质
使用注意事项
碳酸氢铵
NH4HCO3
易溶于水,受潮时在常温下即能分解,温度越高分解越快,遇碱放出氨气。
在土壤中不残留有害物质
(1)不与碱性物质混用以免降低肥效
(2)贮存和运输时要密封,不要受潮或曝晒;
施用后要盖土或立即灌溉
硝酸铵
NH4NO3
易溶于水,受热易分解,遇碱放出氨气,在高温或受猛烈撞击时易爆炸
(2)不能与易燃物混在一起,结块时,不要用铁锤砸碎
硫酸铵
(NH4)2SO4
易溶于水,吸湿性小,常温稳定,遇碱时放出氨气,长期施用,会使土壤酸化,板结
(2)不能长期使用
硫酸钾
K2SO4
易溶于水,长期使用,会使土壤酸化、板结
不能长期使用
1.氮肥、磷肥、钾肥的简易鉴别方法:
一看、二闻、三溶。
一看:
白色固体是氮肥、钾肥,灰白色固体是磷肥;
二闻:
有刺激性气味气体放出的是氮肥,无刺激性气味气体放出的是钾肥、磷肥;
三溶:
氮肥、钾肥全部溶于水,磷肥大多不溶于水或部分溶于水。
2.铵态氮肥不能与碱性物质混合使用。
【典型例题】
类型一、考查盐和化肥的性质、用途、鉴别及推断
1.下列物质在溶液中,组内两两之间都能互相发生化学反应的是( )
A.
硫酸、碳酸钾、氢氧化钡
B.
硝酸银、氯化钠、氯化钡
C.
氯化钙、碳酸钠、氢氧化钾
D.
盐酸、硝酸钾、氢氧化钠
【思路点拨】根据复分解反应发生的条件,若两种物质相互交换成分有水、气体、或沉淀生成,则能发生化学反应,若没有水、沉淀或气体生成,则反应不能发生。
【答案】A
【解析】硫酸能与碳酸钾反应、能与氢氧化钡反应,碳酸钾和氢氧化钡也能反应,组内两两之间都能互相发生化学反应,正确;
B、硝酸银能与氯化钠反应、能与氯化钡反应,但是氯化钠和氯化钡不能反应,错误;
C、氯化钙能与碳酸钠反应,氯化钙不能与氢氧化钾反应,氢氧化钾能与碳酸钠反应,错误;
D、盐酸与硝酸钾不反应,盐酸与氢氧化钠能反应,硝酸钾与氢氧化钠不能反应,错误;
故选A。
【思路点拨】掌握复分解反应发生的条件(有沉淀、气体或水生成)并能灵活运用是正确解答本题的关键。
2.下列各组溶液中不用其他试剂,仅用组内物质相互反应就能区别开来的是()
A.NaCl、Na2CO3、KNO3、HCl
B.Na2SO4、K2CO3、KNO3、Ba(NO3)2
C.CuSO4、NaOH、NaCl、Ba(NO3)2
D.FeCl3、NaOH、KCl、Na2SO4
【答案】C
【解析】先找组内物质有特殊颜色或气味的物质。
C中的CuSO4溶液为蓝色溶液,将CuSO4分别滴入其他三种物质中,产生蓝色沉淀的是NaOH,产生白色沉淀的是Ba(NO3)2,无现象的是NaCl。
D中的黄色溶液是FeCl3,把FeCl3分别加入其余三种溶液中,产生红褐色沉淀的是NaOH,KCl和Na2SO4都无现象,不能区别开。
【思路点拨】物质的鉴别就是根据物质的特性,根据反应现象对物质进行区分,物质的性质和反应的现象是鉴别的基础。
不用其他物质的鉴别顺序是先找有特殊性质的物质(如颜色、气味等),然后以此为试剂进一步鉴别其他组内物质。
3.有一种化肥样品,为了确定它是哪种化肥,进行如下实验:
①取少量样品放入试管中,加入3mLNaOH溶液,在酒精灯上微热,把湿润的红色石蕊试纸放在试管口,试纸变蓝;
②另取少量样品于试管中,加入少量水溶液,滴入几滴硝酸钡溶液,有白色沉淀生成,加入足量稀硝酸(HNO3)沉淀不溶解。
由以上实验可判断该化肥是_______________(写化学式)
【答案】
【解析】由①中现象可知该盐为铵盐,因为铵盐遇碱能放出氨气,氨气遇水显碱性能使红色的石蕊试纸变蓝。
由②中现象,能使硝酸钡产生不溶于稀硝酸的沉淀,说明溶液中含有硫酸根离子。
综合以上分析可得该化肥为(NH4)2SO4。
【思路点拨】要掌握常见离子的鉴别方法。
4.下列用字母表示的8种物质由H、C、O、Na、Cl、Ca中的几种元素组成,它们是初中化学常见的物质。
(1)A是大理石的主要成分,遇B溶液产生气泡,该反应的化学方程式为 。
(2)X和Y反应生成Z和W,其中Y、W常作灭火剂,X、Z均含3种元素,W的化学式为 ,X的化学式为 。
(3)向Z的溶液中逐滴加入B的稀溶液,只生成含有相同金属元素的M和N,其中M不含氧元素,它的化学式为 ,该反应的化学方程式为 。
(4)从上述物质中任选2种为一组,按下图所示装置进行实验,将胶头滴管中的液体滴入瓶中,a处水
面降低,b处水面升高。
写出符合要求的4种物质:
友情提示:
填写物质的化学式、名称或俗称
序号
物质
①
②
③
④
⑤
液体
固体
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑
(2)H2ONaOH
(3)NaClNa2CO3+HCl=NaCl+NaHCO3
(4)
盐酸
H2O
CaCO3
Na2CO3
NaHCO3
NaOH
【解析】
(1)碳酸钙为碳酸盐,根据碳酸盐能与酸反应放出二氧化碳的性质,可推断物质B为酸,结合题中元素的要求,判断B物质为HCl溶液。
(2)根据CO2的化学性质,则物质X为可溶性碱,结合题中元素要求,判断物质X可能为NaOH或Ca(OH)2;
若X为Ca(OH)2则Z就为CaCO3,与物质A为CaCO3相矛盾,所以X为NaOH。
(3)B为稀盐酸而Z为氢氧化钠与二氧化碳反应生成的碳酸钠,碳酸钠与盐酸反应生成氯化钠、水、二氧化碳三种物质,而题中描述“只生成含有相同金属元素的M和N”两种物质,因此,根据两物质发生的反应,可判断两物质反应生成氯化钠和碳酸氢钠,且M不含氧元素为NaCl。
(4)前面所推断的物质中,碳酸盐与稀盐酸反应都可放出二氧化碳气体,而氢氧化钠溶于水放出大量的热,还有氢氧化钠与稀盐酸中和时也会放出大量的热。
【思路点拨】
(1)大理石的主要成分为碳酸钙。
(2)水是自然界中分布最广、最廉价的灭火剂;
二氧化碳是一种气体灭火剂,在自然界中存在也较为广泛,价格低、获取容易。
(4)a处液面下降、b处液面上升,说明反应生成气体或放出了大量热,据此现象在上述物质中进行组合。
5.现有一包固体粉末,可能由CaCO3、CaO、Na2CO3中的一种或几种组成。
为确定其组成,进行了如图所示的实验(假设实验过程无损耗)。
请回答:
(1)根据实验可以确定白色沉淀是 ;
原固体粉末中一定含有 ,它的可能组成有 种。
(2)若实验取固体粉末20g,生成白色沉淀10g,最后得到溶质质量分数为5.85%的X溶液200g(只含一种溶质),则X溶液中溶质的质量是 g,固体粉末由 (填化学式,下同)组成,其中质量小于10g的是 。
(1)CaCO3(或“碳酸钙”)Na2CO3(或“碳酸钠”)3
(2)11.7CaCO3、CaO、Na2CO3CaCO3、CaO
(1)白色粉末溶于水能产生白色沉淀,可知该白色沉淀应该为碳酸钙;
又得到的无色溶液能够和稀盐酸反应生成气体,可以知道在固体粉末中一定含有碳酸钠,它可能的组合为:
①碳酸钠,氧化钙;
②碳酸钠,碳酸钙;
③碳酸钠,氧化钙,碳酸钙。
(2)根据
(1)的解答可知X溶液为氯化钠溶液,氯化钠的质量为:
200g×
5.85%=11.7g,根据题意结合化学方程式,可以求出与盐酸反应的碳酸钠的质量为10.6g,进而可以判断出该固体粉末的组成为CaCO3、CaO、Na2CO3,进而可以判断若白色沉淀质量小于10g,则原混合物的组成为氧化钙和碳酸钙,计算过程如下:
解:
设固体粉末中碳酸钠的质量为x,则:
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106117
x11.7g
解得x=10.6g
这里我们求得的只是和盐酸反应的碳酸钠,粉末总质量为20g。
假如白色沉淀是固体粉末中的,则只有20g﹣10.6g=9.4g,而题目中得到的白色沉淀的质量是10g,也就是说白色沉淀并不是完全来自于原固体粉末中,而是有一部分是反应中生成的,即氧化钙和水反应生成了氢氧化钙,而氢氧化钙又和碳酸钠反应生成了碳酸钙沉淀,从而可以判断在混合物中含有氧化钙。
【思路点拨】本题为框图式物质推断题。
完成此类题目,关键是找准解题突破口,根据物质的化学特性直接得出结论,然后利用顺推或逆推或从两边向中间推断,逐步得出其他结论。
举一反三:
【变式1】下列各组物质,相互不能发生反应的是( )
硫酸钠溶液和碳酸钾溶液
硝酸银溶液和盐酸溶液
氢氧化钡溶液和硝酸溶液
氧化镁和稀硫酸
A、硫酸钠与碳酸钾不能反应,不符合复分解反应,故A正确;
B、硝酸银溶液和盐酸溶液反应生成氯化银沉淀和硝酸,故B错;
C、氢氧化钡与硝酸反应生成硝酸钡和水,故C错;
D、氧化镁与稀硫酸反应生成硫酸镁和水,故D错。
【变式2】长期施用(NH4)2SO4化肥的土壤容易酸化。
下列说法不正确的是( )
A.(NH4)2SO4属于氮肥 B.(NH4)2SO4的水溶液能使酚酞试液显红色
C.不宜长期施用(NH4)2SO4化肥 D.(NH4)2SO4化肥不能与碱性物质混合施用
【答案】B
【变式3】已知A是一种白色难溶于水的钙盐,几种物质有如下图的转化关系:
高温煅烧
+澄清石灰水
+Na2CO3溶液
A
B
C
无色溶液D
(1)用化学式表示:
A___________________,B___________________。
(2)写出A与盐酸反应的化学方程式:
______________________________________。
(3)D中含有的溶质可能有哪几种情况?
____________________________________________________________________。
(1)A.CaCO3B.CaO
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)NaOHNaOH和Na2CO3NaOH和Ca(OH)2
类型二、考查有关盐、化肥的计算
6.某纯碱试样中含有杂质氯化钠,为测定试样中Na2CO3的含量,取等质量的四份试样与溶质质量分数相同的盐酸进行实验。
实验数据记录如下表。
编号
纯碱试样的质量/g
60
盐酸的体积/mL
50
100
150
200
生成气体的质量/g
7.3
14.6
22
(1)盐酸的体积消耗150mL后气体质量不再增加,说明纯碱试样中Na2CO3 (填“完全”或“未完全”)反应。
(2)该纯碱中Na2CO3的质量分数是多少?
【答案与解析】
(1)完全
(2)解:
设每份试样中碳酸钠的质量为x。
10644
X22g
x=53g
×
100%=88.3%
答:
该纯碱中碳酸钠的质量分数为88.3%。
【思路点拨】解本题的关键是能够灵活运用图表数据求出碳酸钠的质量。
由③④组反应可以看出60g样品中最多能生成22g二氧化碳。
【变式】某化工厂用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:
碳酸钠≥96%。
为测定该产品中含碳酸钠的质量分数,进行了以下实验:
取12.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应。
实验数据记录如下:
所加盐酸的次数
第一次
第二次
第三次
第四次
盐酸的质量/g
25
烧杯及所盛物质总质量/g
181.2
204.4
228.6
253.6
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是g。
(2)该产品中碳酸钠的质量分数(填“合格”或“不合格”)
(1)1.8
(2)不合格
【巩固练习】
一、选择题(每小题只有一个选项符合题意)
1.下列各组物质表示同一物质的是( )
A.氢氧化钠、生石灰B.氢氧化钠、熟石灰
C.碳酸钠、纯碱D.二氧化碳、水
2.某农民种植的蔬菜因缺氮肥和磷肥而出现生长缓慢,叶色泛黄,且产量低的现象。
下列肥料最适合施用的是( )
A.CO(NH2)2B.KNO3C.NH4H2PO4D.Ca(H2PO4)2
3.下列各物质在溶液中能大量共存的是( )
A.氢氧化钠溶液和氢氧化钙溶液B.碳酸钠溶液和氢氧化钙溶液
C.氯化铜和硝酸银溶液D.氢氧化钠溶液和硝酸铜溶液
4.粗盐提纯的正确操作顺序是(
)
A.溶解、降温、过滤、转移B.溶解、过滤、蒸发、转移
C.称量、溶解、蒸发、过滤D.溶解、过滤、降温、转移
5.下列物质间不能发生反应的是( )
A.氢氧化钠溶液和硫酸溶液B.碳酸钠溶液和氢氧化钙溶液
C.铜和硝酸银溶液D.氢氧化钠溶液和硝酸钾溶液
6.合理使用化肥有利于农作物的生长和减少环境污染。
下列有关化肥的说法正确的(
A.为保证高产尽量多施用化肥
B.氯化铵与碱性物质混合施用
C.提倡农家肥与化肥综合施用D.CO(NH2)2是一种常用的复合肥料
7.盐有广泛的用途,在加工馒头时往往因面团发酵而变酸,要除去酸味,使馒头变得可口,常常在面团中加入( )
A.食盐B.烧碱C.碳酸氢钠D.熟石灰
8.下列各组物质在溶液中能大量共存的一组是()
A.Na2CO3、NaHCO3、HClB.NaCl、AgNO3、HNO3
C.KNO3、KCl、NaOHD.NaOH、BaCl2、H2SO4
9.现有a、b、c、d四种无色溶液,分别是碳酸钾溶液、硫酸溶液、氯化钡溶液、盐酸中的一种。
两两混合后出现如图所示的现象,请确定a、b、c、d分别是()
A.硫酸溶液、碳酸钾溶液、氯化钡溶液、盐酸
B.氯化钡溶液、盐酸、碳酸钾溶液、硫酸溶液
C.碳酸钾溶液、硫酸溶液、盐酸、氯化钡溶液
D.盐酸、硫酸溶液、碳酸钾溶液、氯化钡溶液
10.下列各组物质在pH=14的某无色溶液中,能大量共存的是( )
A.FeCl3、NaCl、KNO3B.NaCl、NaOH、NaNO3
C.CaCl2、NaNO3、Na2CO3D.KNO3、H2SO4、NaCl
11.有一溶液是由盐酸、硫酸、硫酸铜、氯化铜几种溶液中的两种混合而成,向该混合液中滴加Ba(OH)2溶液,溶液的体积与生成沉淀质量的关系如下图所示,则该混合液是( )
A.盐酸、硫酸B.硫酸、氯化铜C.盐酸、氯化铜D.硫酸、硫酸铜
12.分别将下列各组物质同时加到水中,得到无色透明溶液的是( )
A.HNO3、NaCl、K2SO4B.KCl、NaOH、CuSO4
C.BaCl2、NaOH、H2SO4D.FeCl3、Na2SO4、KCl
二、填空题
13.粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。
某班同学在粗盐提纯实验中,为把少量可溶性杂质CaCl2、MgCl2一并除去,将教材中实验方案修改设计如下,请据此回答问题:
(1)实验操作A的名称是________,该操作的目的是________。
(2)写出步骤③中发生反应的主要化学方程式________;
步骤⑥的作用是________。
(3)小刚同学认为该方案实际得到的氯化钠可能比粗盐中含有的氯化钠要多,请你为他找出理由:
________。
14.下表鉴别物质的方法中,方法1和方法2都正确的是。
15.下列物质放在空气中质量会减轻的是。
①碳酸钠晶体;
②烧碱;
③食盐;
④浓盐酸
16.粗盐中常含有CaCl2、MgCl2、Na2SO4等杂质。
粗盐提纯时,先配制成粗盐溶液,然后分步向粗盐溶液中加入NaOH溶液,Na2CO3溶液、BaCl2溶液和盐酸。
若各步操作所加试剂均为过量并过滤分离所得沉淀,最后再蒸发溶剂可制得精盐NaCl。
在下列所设计的四种试剂加入的先后顺序中,不能达到粗盐提纯目的是。
①Na2CO3、BaCl2、NaOH、HCl;
②BaCl2、Na2CO3、NaOH、HCl;
③BaCl2、Na2CO3、HCl、NaOH;
④BaCl2、NaOH、Na2CO3、HCl
17.合理使用化肥,有利于农作物的生长和减少环境污染。
下列有关化肥的说法正确的是。
①为保证高产尽量多施用化肥;
②不能将氯化铵与碱性物质混合施用;
③KNO3是一种常用的复合肥料;
④提倡将农家肥与化肥综合使用
三、计算题
18.把萝卜块放入浓盐水中,萝卜块会皱缩;
把萎蔫的青菜放入清水中,青菜会变挺.这些都是生活常识,其中蕴含着科学道理,启迪我们去思考。
(1)观察人体口腔上皮细胞时,为什么要将口腔上皮细胞涂抹在生理盐水(溶质质量分数为0.9%的氯化钠溶液)中?
(2)现有100克溶质质量分数为4.5%的氯化钠溶液,将它稀释成溶质质量分数为0.9%的生理盐水,需加水多少毫升?
19.有一种不纯的氯化铵,经测定其含氮量为30%,则混入的另一种氮肥可能是。
①碳酸氢铵;
②硝酸铵;
③硫酸铵;
④都不是
20.在一烧杯中盛有22.3g
Na2CO3和NaCl组成的固体混合物,加143.1g水溶解,制成溶液。
向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示。
请根据题意回答问题:
(1)当滴加了73g稀盐酸时,试通过计算求出放出气体的总质量为g。
(2)当滴加稀盐酸至图中B点时,烧杯中溶液里的溶质是(写化学式)。
NaCl和HCl
(3)当滴加了73g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中含溶质的质量。
1.【答案】C
【解析】A中生石灰为氧化钙;
B中熟石灰为氢氧化钙。
2.【答案】C
【解析】蔬菜缺少氮肥和磷肥,应补充氮和磷这两种元素,故选择同时含有这两种元素的复合肥——磷酸二氢铵(NH4H2PO4)。
3.【答案】A
【解析】在溶液中两物质间不能发生化学反应,则能共存。
A中二者不能反应,故选A。
B中Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,C中CuCl2+2AgNO3=2AgCl↓+Cu(NO3)2,D中氢氧化钠和硫酸铜发生反应生成氢氧化铜沉淀,故B、C、D都不能共存。
4.【答案】B
【解析】提纯粗盐,应该先溶解,再过滤,然后将滤液蒸发结晶得到精盐,最后将精盐转移到试剂瓶中。
5.【答案】D
【解析】NaOH和KNO3交换成分无沉淀、气体或水生成,不符合复分解反应发生的条件,所以二者不能发生反应。
故选D。
6.【答案】C
【解析】本题考查化肥的有关知识。
A项化肥应合理施用;
B项氯化铵是一种固态氮肥不能与碱性物质混合使用,因二者相互反应会生成氨气而降低肥效;
D项尿素中只含有N、P、K三种元素中的氮元素,是氮肥而非复合肥。
7.【答案】C
【解析】碳酸氢钠与酸反应,可以消耗生成的酸。
熟石灰、氢氧化钠虽然能够中和