难溶电解质的溶解平衡教案Word文档下载推荐.docx
《难溶电解质的溶解平衡教案Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《难溶电解质的溶解平衡教案Word文档下载推荐.docx(17页珍藏版)》请在冰豆网上搜索。
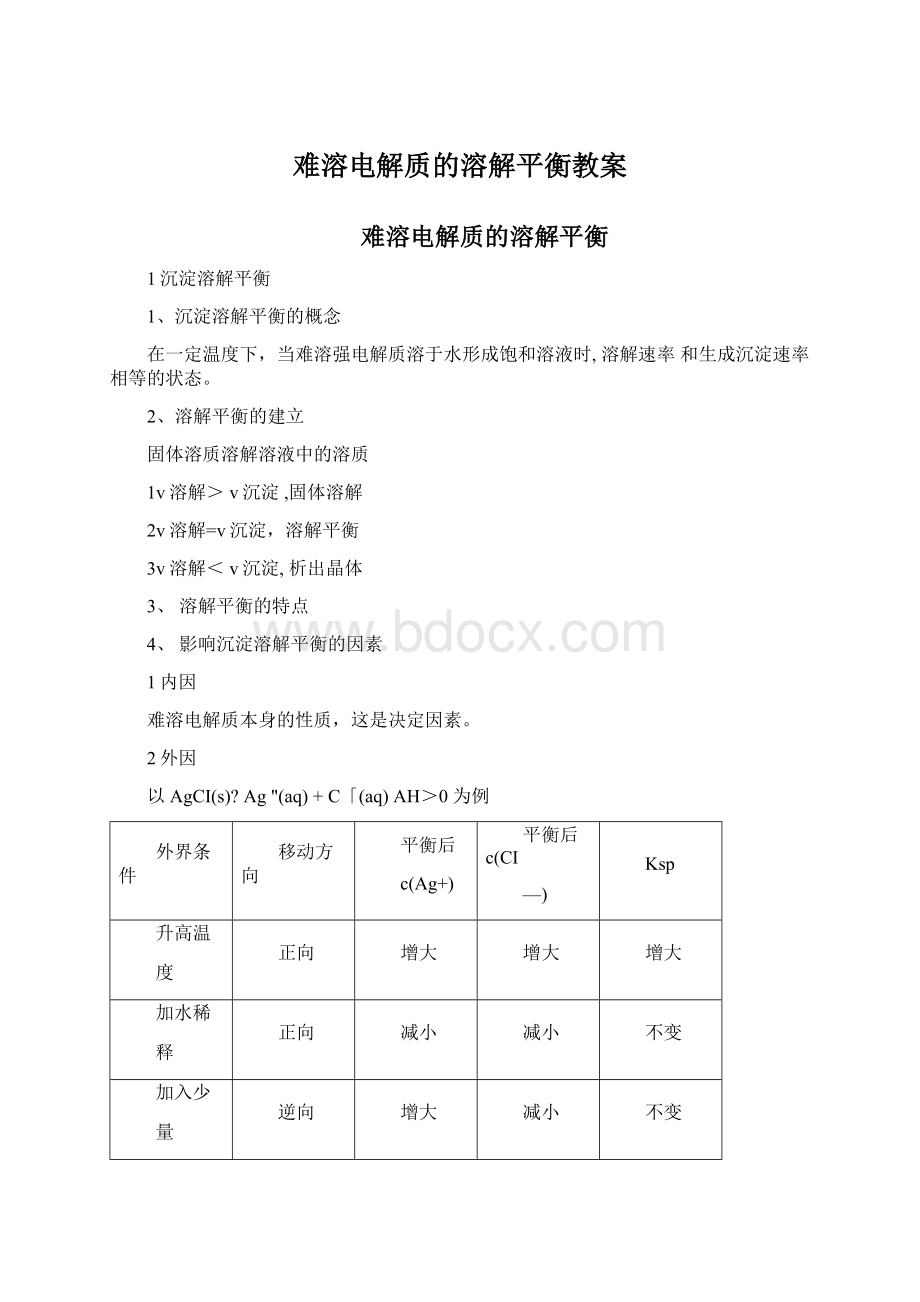
1.溶度积和溶解度的值都可用来表示物质的溶解能力;
2.用溶度积直接比较时,物质的类型必须相同:
AB型物质:
Ksp=c(A+)c(B-);
AB2(或A2B)型物质:
Ksp=c(A)c(B「)[或Ksp=c(A)c(B「)];
A2B3型物质:
Ksp=c2(A3+)c3(B2「)对于同类型物质,心越小,其溶解度越小。
5溶度积常数及应用
1.溶度积和离子积
以AmBn(s)?
mAn+(aq)+nBm-(aq)为例:
离子积
溶度积
概念
沉淀溶解的平衡常数
溶液中有关离子浓度幕
的乘积
符号
Qc
表达式
Ksp(AmBn)=c(A
"
)cn(Bm-),式中的浓度都是平衡浓度
Qc(AmBn)=cm(An"
)cn(Bm
J,式中的浓度是任意
浓度
应用
判断在一定条件下沉淀能否生成或溶解①
Qc>
Ksp:
溶液过饱和,有沉淀析出②Qc=Ksp:
溶液饱和,处于平衡状态③Qc<
溶液未饱和,无沉淀析出
2.Ksp的影响因素
(1)内因:
难溶物质本身的性质,这是主要决定因素。
(2)外因
1浓度:
加水稀释,平衡向溶解方向移动,但Ksp不变。
2温度:
绝大多数难溶盐的溶解是吸热过程,升高温度,平衡向溶解方向移动,Kp增大。
3其他:
向平衡体系中加入可与体系中某些离子反应生成更难溶物质或更难电离物质或气体的离子时,平衡向溶解方向移动,但Ksp不变。
4沉淀溶解平衡的应用
1.沉淀的生成
加入沉淀剂,应用同离子效应,控制溶液
的pH,当时有沉淀生成。
QcKsp
1调节pH法:
加入氨水调节pH至7~8,可
除去氯化铵中的杂质氯化铁。
2加沉淀剂法:
以Na2S、H2S等作沉淀剂,
使Cu2+、Hg2+等生成极难容的硫化物CuS
HgS沉淀
2.沉淀的溶解
3分步沉淀
溶液中含有几种离子,加入某沉淀剂均可生成沉淀,沉淀生成的先后顺序按离子积大于溶度积的先后顺序沉淀,叫作分步沉淀。
Ksp越小越先沉淀,且Ksp相差越大分步沉淀越完全;
如AgCI、AgBr、AgI、Ag2S
一般认为沉淀离子浓度小于1.0X10-5mol/L时,则认为已经沉淀完全
4、同离子效应
(1)同离子效应的来源
HAcH++Ac-加入NaAc,
NaAc=Na++Ac-
溶液中Ac-大大增加,平衡向左移动,降低了HAc的电离度.
同离子效应:
向弱电解质中加入具有相同离子(阳离子或阴离子)的强电解质后,解离平衡发生左移,降低电解质电离度的作用称为同离子效应,电离度降低。
6离子共存问题总结离子能否在同一电解质溶液里大量存在,决定于离子能否发生化学反应,或离子的物理性质是否符合题目的相关规定。
因此,要弄清离子能否在同一溶液中大量共存的问题,关键是掌握离子的性质。
1.不能在酸性溶液中大量共存的离子一般为弱酸根离子或易分解的酸的酸根、易挥发的酸的酸根、水解呈碱性的离子等,如①OH②AIO;
③COJ④HCOJ⑤SiOT⑥SOT⑦HSOJ⑧SO2-⑨S2—
⑩HS-?
CIO-?
L?
PO厂?
HPO4―?
fPO:
女口:
H2O+AIO-+J===AI(OH)3J,AIO-+4H+===AI‘十+2H2O。
2.不能在碱性溶液中大量共存的离子
一般为能生成不溶性的碱的金属离子或生成弱碱的离子或酸式盐的酸根离子等,如:
①H"
②Fe2"
③Fe3"
4Cu2"
⑤Ag"
⑥Zn2"
⑦Mg2"
⑧aL⑨NH:
⑩HCOJ?
HbPO:
?
HPO4-?
HSOJ?
HS^等。
OI
女口:
H2PO「+2OH-===PO4-+2H2O,NH4+OHNHaH2OO
3.相互间反应生成沉淀或微溶物的离子不能大量共存
如①SO2「与Ba2"
、Pb2"
、Ag"
、Ca2"
等不共存;
②CO3「与Ca"
、Mg2"
、Ba2"
③L与Cu2"
、Hg2"
、Fe2"
等不共存;
④C17H35COO「与Ca2"
、Mg2"
等生成沉淀不共存。
4.因氧化性强而不能与强还原性离子大量共存
如①酸性条件下NOJ与「、Fe2"
、S2—、SO3-等不共存;
②酸性条件下SO3―与S2「等不共存(但在碱性条件下可以共存);
3MnO】与I一、§
—、S&
-、B^、C「等不共存。
5.能相互结合形成络合物的离子不能大量共存[来源:
学科网]
女口①Fe3"
与SCN—:
Fe3"
+SCN—===[Fe(SCN)]2"
;
②Ag"
与NH3H2O:
Ag"
+2NH3H2O===[Ag(NH3)2]"
+2H2O。
6.水解显酸性的离子(如A|3"
、Fe3"
等)和水解显碱性的离子(AIO;
、co3-、hco;
、CIO;
等)不能大量共存
①Al3"
与AIO;
、HCO;
:
Al3"
+3AIO;
+6H2O===4AI(OH)3Al3"
+3HCO;
===AI(OH)3J+3CO21;
②Fe3"
与CIO;
Fe"
+3CIO;
+3H2O===Fe(OH)3J+3HCIO:
③Fe2"
2Fe2"
+CIO;
+4OH;
H2O===2Fe(OH)3J+Cl;
。
7.溶液若无色,则不存在有色(溶液中)离子
女口Fe3"
、Cu2"
、MnO;
、Fe"
等。
&
不能在中性溶液中大量存在的离子
AI3"
等弱碱的阳离子,其本性是使溶液呈酸性,它
们不能在中性溶液中大量存在;
C&
、PO3;
等酸根阴离子,
它们的本性是使溶液呈碱性,它们不能在中性
溶液中大量存在。
精析
二、例题
【例题1]
溶解平
【题干]下列对沉淀衡的描述正确的是()
A.反应开始时,溶液中各离子浓度相等
B.
沉淀的速率和溶解的速率相等
溶液中溶质的离子浓度相等,且保持
沉淀溶解达到平衡时,
C.沉淀溶解达到平衡时,不变
如果再加入难溶性的该沉淀物,将促
D.沉淀溶解达到平衡时,
进溶解
【例题2]
【题干]难溶电解质在水溶液中存在着电离平衡。
在常温下,溶液里各离子的浓度以它们系数为次方的乘积是一个常数,叫溶度积
常数(Ksp)。
例如:
Cu(OH)2=Cu2"
+20H「,心=c(Cu2"
)[c(OH「)]2=2X10-20。
当溶液中各离子的浓度次方的乘积大于溶度积时,则产生沉淀,反之沉淀溶解。
■,2+
(1)某CuSO4溶液里c(Cu)=0.02mol/L,如要生成Cu(OH)2沉淀,
应调整溶液的pH,使之大于E达到目的。
(2)要使0.2mol/LCuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度
降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为。
【例题4】
【题干】与c(H"
)c(OH「)=Kw类似,FeS饱和溶液中存在:
FeS(s片Fe2"
+《一,c(Fe"
)c(L)=Ksp。
常温下Ksp=8.1x10一17。
(2)又知FeS饱和溶液中c(H"
)与c&
J之间存在以下限量关系:
c(H"
)c(S2「)=1.0X10-22,为了使溶液中c(Fe2"
)达到1mol/L,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H"
)为
【四、课堂运用
【基础】
1.实验:
①0.1molL-1AgNO3溶液和0.1mol1NaCl溶液等体积混合
得到浊液a,过滤得到滤液b和白色沉淀C;
2向滤液b中滴加0.1mol1KI溶液,出现浑浊;
3向沉淀C中滴加0.1mol1KI溶液,沉淀变为黄色。
下列分析不正确的是()
A.浊液a中存在沉淀溶解平衡:
AgCI(s)?
Ag(aq)+C「(aq)
B.滤液b中不含有Ag+
C.③中颜色变化说明AgCl转化为AgI
D.实验可以证明AgI比AgCl更难溶
2.
C.CaSO
D.Ag2S
下列属于微溶物质的是()
A.AgClB.BaCb
3.在含有浓度均为0.01mol/L的Cl—、Br—、1—离子的溶液中,缓慢且少量的加入AgNO3稀溶液,结合溶解度判断析出三种沉淀的先后顺序是()
A.
B.Agl、AgBr、AgCI
D.三种沉淀同时析出
AgCI、AgBr、AgI
C.AgBr、AgCl、AgI
2.已知溶液中存在平衡:
AH<
0,下列有关该平衡体系的
Ca(OH)2(s)Ca2"
(aq)+2OH—(aq)
说法正确的是
1升高温度,平衡逆向移动
2向溶液中加入少量碳酸钠粉末能增大钙离子浓度
3除去氯化钠溶液中混有的少量钙离子,可以向溶液中加入适量的
NaOH溶液
4恒温下向溶液中加入CaO,溶液的pH升高
5给溶液加热,溶液的pH升高
6向溶液中加入Na2CO3溶液,其中固体质量增加
7向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
A.①⑥B.①⑥⑦
C.②③④⑥D.①②⑥⑦
3.已知Ksp(AgCl)=1.56X10—10,Ksp(AgBr)=7.7X10—13,Ksp(Ag2CrO4)=
向该溶液中逐滴加入0.010生沉淀的先后顺序为(
——2—
A.CI、Br、CrO4
C.Br、Cl、CrO4
【拔高】
1.下列叙述不正确的是
A.CaCQ能够溶解在
9.0X10—12。
某溶液中含有Cl—、Br—和CrO4—,浓度均为0.010molL—1,
molL—1的AgNO3溶液时,三种阴离子产
2——-
B.CrO4、Br、Cl
—2—
D.
C02的水溶液中
Br、CrO4、Cl
B.Mg(OH)2可溶于盐酸,不溶于NHQI溶液
C.AgCl可溶于氨水
D.MgSO4溶液中滴加Ba(OH)2得到两种沉淀
2.水是人类生存和发展的宝贵资源,而水质的污染问题却越来越严重。
目前,世界各国已高度重视这个问题,并采取积极措施进行治理。
(1)工业废水中常含有不同类型的污染物,可采用不同的方法处理。
以下处理措施和方法都正确的是字母编号,可多选)。
选项
污染物
处理措施
方法类别
A
废酸
加生石灰中
和
物理法
B
Cu2+等重金属离子
加硫化物沉降
化学法
C
含纯碱的废水
加石灰水反应
(2)下图是某市污水处理的工艺流程示意图:
1下列物质中不可以作为混凝剂
号,可多选)。
A.偏铝酸钠
C.碱式氯化铝
2混凝剂除去悬浮物质的过程是
A.物理变化
C既有物理变化又有化学变化
CN-的废水过程中,液氯在碱性条件下可以将(其毒性仅为氰化物的千分之一),氰酸盐进一]
(沉降剂)使用的是
B.氧化铝
D.氯化铁
填字母编号)。
B.化学变化
填字母编
(3)在氯氧化法处理含氰化物氧化成氰酸盐被氧化为无毒物质。
某厂废水中含KCN,
其浓度为650mg二现用氯氧化法处理,发
生如下反应:
KCN+2KOH+CI2===KOCN+2KC1+H2O再投入过量液氯,可将氰酸盐进一步氧化为氮气。
请配平下列化学方程式:
KOCN+
KOH+
Cl2
CO2+
N2+
KC1+
H2O。
若处理上述
水20L,使KCN完全转化为无毒物质,至少需液氯
课程小结
1、沉淀和溶解之间的转换以及影响沉淀溶解平衡的因素
2、溶解平衡一般是吸热的,温度升高平衡右移,Ksp增大,但Ca(OH)2相反
3、沉淀溶解平衡图像上点的认识
2.在25C时,FeS的心=6.3X0-18,CuS的Kp=1.3X0―36,ZnS的Ksp=1.3X
10―24。
下列有关说法中正确的是
()
C.
25C时,CuS的溶解度大于ZnS的溶解度
25C时,饱和CuS溶液中Cu2"
的浓度为1.3X10―36molL-1
向物质的量浓度相同的FeCb、ZnCl2的混合液中加入少量NazS,只有FeS沉淀
生成
D.除去某溶液中的Cu2"
,可以选用FeS作沉淀剂
【巩固】
1.
(1)已知Ksp(AgCI)=1.8X10-10,则将AgCl放在蒸馏水中形成饱和溶液,溶液中的c(Ag"
)是多少?
(2)已知Ksp[Mg(OH)2]=1.8X0“1,则将Mg(OH)2放入蒸馏水中形成饱和溶液,溶液的pH为多少?
⑶在0.01mol1的MgCl2溶液中,逐滴加入NaOH溶液,刚好出现沉淀时,溶液的pH是多少?
当Mg2"
完全沉淀时,溶液的pH为多少?
2.已知Ksp(AgCl)=1.8X10-10,K(Ag2CrO4)=1.9X0一12,现在向0.001molL-1K2CrO4和0.01molL^1KCl混合液中滴加0.01mol1AgNOs溶液,通过计算回答:
(1)C「、CrO4―谁先沉淀?
⑵刚出现Ag2CrO4沉淀时,溶液中C「浓度是多少?
(设混合溶液在反
应中体积不变)
1.已硫酸工业中废渣称为硫酸渣,其成分为SiO2、FeO3、AI2O3、MgO。
某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。
Kb=
已知溶液pH=3.7时,Fe"
已经沉淀完全;
一水合氨电离常数1.8X10-,其饱和溶液中c(OH「)约为1X0—moll"
请回答:
填以下字
(25C时,氢氧化镁的Ksp=5.6X10
(1)写出A与氢氧化钠溶液反应的化学方程式:
溶性的该沉淀物,由于固体的浓度为常数,故平衡不发生移动。
【答案】
(1)5
(2)6
【解析】
(1)根据题意:
当c(Cu2r[c(OH「)]2=2X10-20时开始出现沉淀,贝Uc(OH「)
船mol/L‘需mol/L=1。
-mol/L,c(H上1。
--mol/L,pH
=5,所以要生成Cu(0H)2沉淀,应调整pH>
5o
⑵要使Cu2+浓度降至0.2mol/L/1000=2X10一4mol/L,c(OHr)=
2X10-20
、mol/L=
\y2X10
—8I—6
10-mol/L,c(H)=10-mol/L。
此时溶液的pH=6。
答案】
(1)7.92X10-8gFeS在水中存在下列平衡:
FeS(s)Ff(aq)+S2-(aq),而Fe2+、sT均可以发生水解:
Fe++2H2O涯£
夜Fe(0H)2+2H+、
S2-+H2O'
崖®
HS-+OH,
使上述平衡中的c(Fe2+)、c(g-)降低,平衡向右移动,造成更多的FeS溶解
(2)1.11X10-3mol/L
(1)由FeS(s遅ffiFe++《-
c(Fe2+)=VKSP^/8.1X10-^=9X10-9mol/L
即1L水中可溶解9X10-9mol的FeS
由100:
S=1000:
(9X10-9x88)g所以S=7.92X10一8g
1.0X10-22
c(S2-)
(2)c(Fe2+)=1mol/L,贝卩c(S2-)=^^5=
=8.1X10-17mol/L。
又0
(1)c(S2-)=1.0X10-22,所以c(H*)=
叫=1.11X10-3mol/Lo
8.1X10「
【答案】AB
【解析】在浊液a中,存在AgCl的沉淀溶解平衡,正确;
B项,向滤液b中加
入0.1mol•L1
更难溶解,向有应,生成黄色的
KI溶液,出现浑浊,说明含有少量Ag:
错误;
由于Agl比AgCl
AgCl存在的c中加入0.1mol•LkI溶液,能发生沉淀转化反Agl,C项和D项都正确。
BaC2易溶,AgCl、AgzS属难溶物。
Agl比AgBr、AgCl更难溶于水,故Ag+不足时先生成Agl,析出沉淀的
先后顺序是Agl、AgBr、AgCl,答案为B。
【答案】A
⑦错。
根据已知的三种阴离子的浓度计算出要产生三种沉淀所需所需Ag+浓度最小的先沉淀。
156X10—10
【解析】②会生成CaCO3,使Ca2+浓度减小,错误;
加入氢氧化钠溶液会使平衡左移,有Ca(OH)2沉淀生成,但Ca(OH)2的溶度积较大,要除去Ca2+,应把Ca+转化为更难溶的CaCO3,③错误;
恒温下Ksp不变,加入CaO后,溶液仍为Ca(OH)2的饱和溶液,pH不变,④错;
加热,Ca(OH)2的溶解度减小,溶液的pH降低,⑤错;
加入Na2CO3溶液,沉淀溶解平衡向右移动,Ca(OH)2固体转化为CaCQ固体,固体质量增加,⑥正确;
加入NaOH固体平衡向左移动,Ca(OH)2固体质量增加,
Ag*的最
小浓度,
-L—1;
要产生AgCl沉淀,c(Ag+)>
—mol•「=1.56X10—8mol
L—1;
c(AgJ
Br、
Cl、
度可以促进沉淀生成。
A项中CaC03(s)崖瑾Cf(aq)+CO3-(aq),WCO遅腋H
77X10—13
要产生AgBr沉淀,c(Ag+)>
—mol-L—1=7.7X10—11mol-
解;
D项中反应的离子方程式为Mg2++S&
一+Ba2++2OH_===Mg(OH)2;
+BaSO4;
,得到两种沉淀。
(1)BC⑵①B②C(3)243216235.5
(1)工业废水中的废酸可加生石灰中和,属于化学变化。
CuS、HgS、Ag2S均难溶,所以加硫化物如Na2S可沉淀Cu2+等重金属离子,消除污染;
纯碱可加入石灰水生成CaCO3沉淀而除去。
(2)偏铝酸钠、碱式氯化铝、氯化铁水解生成胶体,除去悬浮物,而AI2O3难溶于
水,不能产生胶体,不能作混凝剂。
在除去悬浮物的过程中既有物理变化又有化学变化。
⑶根据KCN+2KOH+CI2===KOCN+2KCl+H2O、2KOCN+4KOH+
20LX0.650g-L_1
65g•mo|T
3Cl2===2CO2+N2+6KCl+2H2O,n(KCN)=—一一=0.2mol,
0.2mol
n(Cb)=0.2mol+—2—X3=0.5mol,
所以m(Cl2)=0.5molX71g•mol_1=35.5g。
【答案】D
【解析】1L溶液中溶解的CuS的质量为^/T3x10一18X96g,同理1L溶液中溶解的ZnS的质量为{13x10一12X97g,所以CuS的溶解度小于ZnS的溶解度,A、B错误;
FeS的Ksp大于ZnS,所以C选项应只有ZnS生成;
D选项依据沉淀的转化,溶度积大的FeS可以转化为溶度积小的CuS。
(1)由AgCI(s)崖珂iAg+(aq)+Cl_(aq)
知c(Ag+)=c(Cl_)
所以Ksp(AgCI)=1.8X10_10=c(Ag+)•c(Cl_)=c2(Ag+)
解得c(Ag+)=1.3X10一5mol-L_1
⑵由Mg(OH)2(s)涯琏Mg2+(aq)+2OH_(aq)
_112丰2一
解得c(OH_)=3.3X10_4mol-L_1
Kw
知Ksp[Mg(0H)2]=1.8X10_=c(Mg)•c(OH一)=
所以c(H+)=—=3.0X10_11mol•L_1
cOH
所以pH=10.5
⑶由Ksp[Mg(OH)2]=1.8X10_11=c(Mg2+)•c2(OH一)=0.01•cQH_)
——5_1
c(OH)=4.2X10mol-L
+I'
w—10—1
c(H戶—=2.4X10mol-L
所以pH=9.6,即当pH=9.6时,开始出现由于一般认为残留在溶液中的离子浓度小于故Mg2+完全沉淀时有:
-11
1X10-5•c2(OH-)=1.8X10
所以c(OH-)=1.34X10-3mol-L-1
c(H+)=—'
7,-=7.46X10-12mol-L-1cOH
所以pH=11.1
(1)CI-先沉淀
(2)4.13X10-6mol
Mg(0H)2沉淀。
1X10-mol•L-1时,沉淀已经完全。
-L-1
KspAgC