高三一轮复习 第八章 水溶液中的离子平衡教案总结Word文档格式.docx
《高三一轮复习 第八章 水溶液中的离子平衡教案总结Word文档格式.docx》由会员分享,可在线阅读,更多相关《高三一轮复习 第八章 水溶液中的离子平衡教案总结Word文档格式.docx(12页珍藏版)》请在冰豆网上搜索。
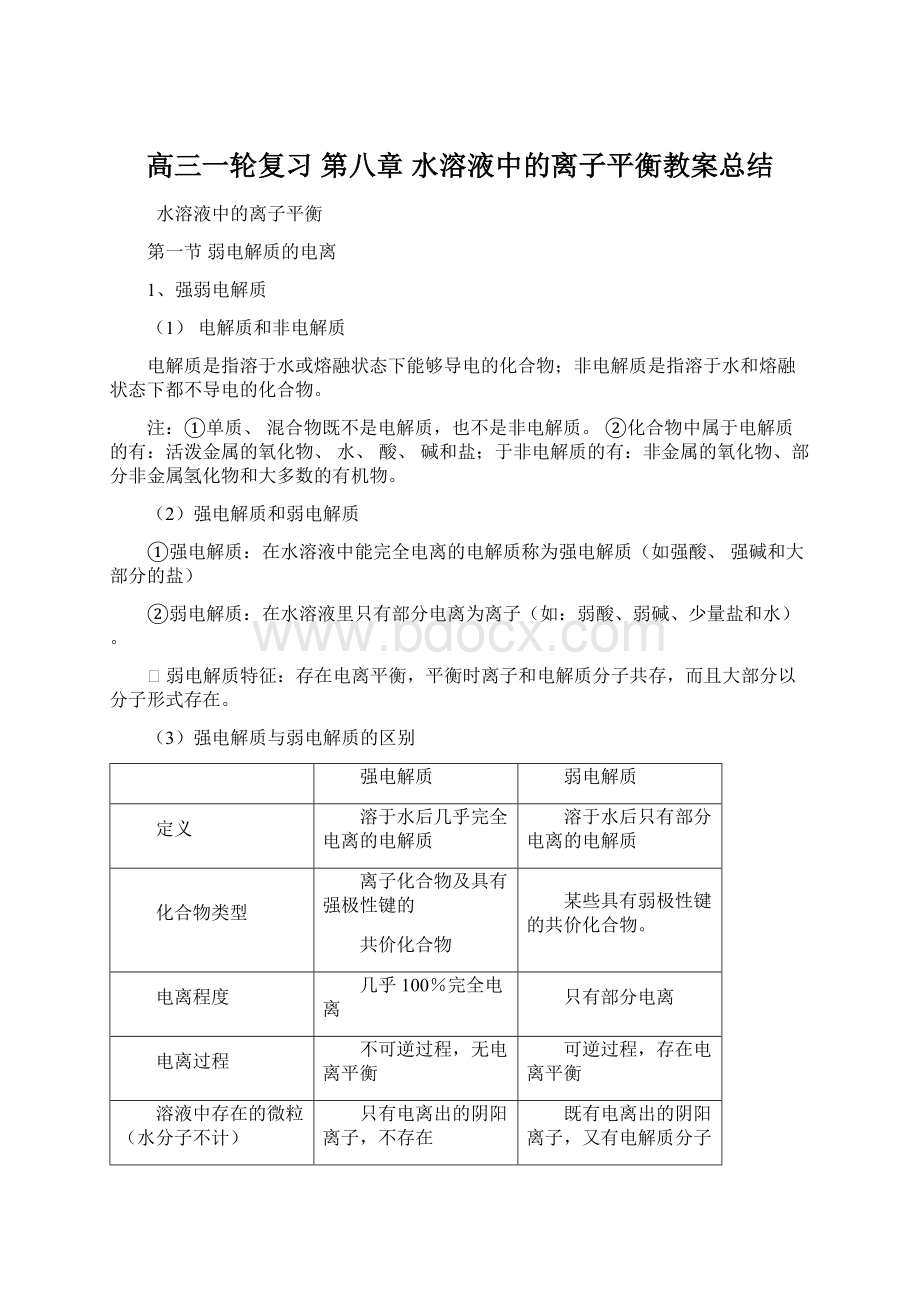
不可逆过程,无电离平衡
可逆过程,存在电离平衡
溶液中存在的微粒(水分子不计)
只有电离出的阴阳离子,不存在
电解质分子
既有电离出的阴阳离子,又有电解质分子
实例
绝大多数的盐(包括难溶性盐)
强酸:
强碱:
弱酸:
H2CO3、CH3COOH等。
弱碱:
NH3·
H2O、Cu(OH)2Fe(OH)3等。
少数盐:
(CH3COO)2Pb、HgCl2和水(H2O)
电离方程式
NaHSO4(aq)=
NaHSO4(熔融)=
H2S
Al(OH)3
2、弱电解质的电离
(1)弱电解质电离平衡的建立(弱电解质的电离是一种可逆过程)和
(2)电离平衡的特点
弱电解质的电离平衡和化学平衡一样,同样具有“逆、等、动、定、变”的特征。
①逆:
弱电解质的电离过程是可逆的。
②等:
达电离平衡时,分子电离成离子的速率和离子结合成分子的速率相等
③动:
动态平衡,即达电离平衡时分子电离成离子和离子结合成分子的反应并没有停止。
④定:
一定条件下达到电离平衡状态时,溶液中的离子浓度和分子浓度保持不变,溶液里既有离子存在,也有电解质分子存在。
且分子多,离子少。
⑤变:
指电离平衡是一定条件下的平衡,外界条件改变,电离平衡会发生移动。
(3)电离常数
①概念:
在一定条件下,弱电解质在达到电离平衡时,溶液中电离所生成的各种离子浓度的乘积跟溶液中未电离的分子浓度的比是一个常数。
这个常数叫做电离平衡常数,简称电离常数,用K来表示。
通常用Ka表示弱酸的电离常数,用Kb表示弱碱的电离常数。
②
③意义:
K值越大,表示该弱电解质越易电离,所对应的弱酸或弱碱相对较强。
④电离常数的影响因素
a.电离常数随温度变化而变化,但由于电离过程热效应较小,温度改变对电离常数影响不大,其数量级一般不变,所以室温范围内可忽略温度对电离常数的影响
b.电离常数与弱酸、弱碱的浓度无关,同一温度下,不论弱酸、弱碱的浓度如何变化,电离常数是不会改变的。
即:
电离平衡常数与化学平衡常数一样,只与温度有关。
(3)影响电离平衡的因素
①内因:
电解质本身的性质,是决定性因素。
②外因
a.温度:
因电离过程吸热较少,在温度变化不大的情况下,一般不考虑温度变化对电离平衡的影响。
b.浓度:
在一定温度下,浓度越大,电离程度越小。
因为溶液浓度越大,离子相互碰撞结合成分子的机会越大,弱电解质的电离程度就越小。
因此,稀释溶液会促进弱电解质的电离。
c.外加物质:
若加入的物质电离出一种与原电解质所含离子相同的离子,则会抑制原电解质的电离,使电离平衡向生成分子的方向移动(同离子效应);
若加入的物质能与弱电解质电离出的离子反应,则会促进原电解质的电离,使电离平衡向着电离的方向移动。
影响醋酸电离的因素
HAcH++Ac-
条件变化
平衡移动方向
C(H+)
n(H+)
电离度
K
温度升高
浓
度
加H2O
加冰HAc
外
加
物
质
加NaOH(s)
加HCl(g)
加NaAc(s)
第二节水的电离和溶液的酸碱性
1、水的电离
(1)水的电离特点
水是极弱的电解质,能发生微弱电离,电离过程吸热,存在电离平衡。
其电离方程式为
(2)水的离子积
①定义:
一定温度下,水的离子积是一个定值。
我们把水溶液中叫做水的离子积常数。
在25℃时,
②一定温度时,Kw是个常数,Kw只与温度有关,温度越高Kw越大
③任何水溶液中,水所电离而生成的
④任何稀溶液中,
影响水电离平衡的因素:
a.温度:
温度越高,温度越高Kw越大。
b.酸碱抑制水的电离;
盐类水解促进水的电离。
2、溶液的酸碱性与pH
(1)溶液的酸碱性的本质——C(H+)、C(OH-)的关系
①中性溶液:
②酸性溶液:
③碱性溶液:
(2)溶液pH的计算pH=—lgC(H+)
溶液显酸性:
①单一酸溶液pH=—lgC(H+)
pH=a,加H2O稀释10n倍,则pH=a+n
pH=a,加H2O稀释10n倍,则pH<
a+n
单一酸溶液的稀释
②强酸混合液的pH
lgC(H+)=
c(H+)1V1+c(H+)2V2
V1
+V2
规律:
当两种强酸溶液的ΔpH≥2,且等体积混合,pH(混)=pH(小)+0.3
③强酸强碱溶液混合
c(H+)V(H+)-c(OH-)V(OH-)
V(H+)+V(OH-)
思考:
溶液显碱性时pH的计算
3、酸碱中和滴定
(1)中和滴定的概念
用已知物质的量浓度的酸(或碱)来测定未知物质的量浓度的碱(或酸)的实验方法。
(2)酸碱中和反应的实质
酸碱中和反应的实质是酸电离产生的H+与碱电离产生的OH-结合生成水的反应。
(3)原理:
在中和反应中,使用一种已知物质的量浓度的酸(或碱)溶液与未知物质的量浓度的碱(或酸)溶液完全中和,测出二者所用的体积,根据化学方程式中酸碱物质的量比求出未知溶液的物质的量浓度。
(4)指示剂的选择
①强酸和强碱相互滴定时,既可选择酚酞,也可选择甲基橙作指示剂;
②强酸滴定弱碱时,应选择甲基橙作指示剂;
③强碱滴定弱酸时,应选择酚酞作指示剂。
变色范围:
甲基橙3.1-4.4(橙色)石蕊5.0-8.0(紫色)酚酞8.2-10.0(浅红色)
中和滴定的操作过程:
(1)滴定管的刻度,O刻度在上,往下刻度标数越来越大,全部容积大于它的最大刻度值,因为下端有一部分没有刻度。
滴定时,所用溶液不得超过最低刻度,不得一次滴定使用两滴定管酸(或碱),也不得中途向滴定管中添加。
滴定管可以准确读到小数点后一位。
(2)药品:
标准液;
待测液;
指示剂。
(3)准备过程:
准备:
检漏、洗涤、润洗、装液、赶气泡、调液面。
(洗涤:
用洗液洗→检漏:
滴定管是否漏水→用水洗→用标准液洗(或待测液洗)→装溶液→排气泡→调液面→记数据V(始)
(4)试验过程:
洗、取、滴、读、算。
滴:
锥形瓶下垫一张白纸,滴定过程中左手控制滴定管,右手不断震荡锥形瓶,眼睛注视锥形瓶中溶液的颜色变化,直至加入一滴溶液使锥形瓶中溶液变色,且半分钟之内不褪色,滴定结束。
3、酸碱中和滴定的误差分析:
利用n酸c酸V酸=n碱c碱V碱进行分析
式中:
n——酸或碱中氢原子或氢氧根离子数;
c——酸或碱的物质的量浓度;
V——酸或碱溶液的体积。
当用酸去滴定碱确定碱的浓度时,则:
c碱=
4.操作注意事项
(1)滴速:
先快后慢,当接近终点时,应一滴一摇。
(2)终点:
最后一滴恰好使指示剂颜色发生明显的改变且半分钟内不变色,读出V(标)记录。
(3)在滴定过程中,左手控制活塞或玻璃小球,右手摇动锥形瓶,两眼注视锥形瓶内溶液颜色的变化。
(4)仪器洗涤
①酸式滴定管水洗后,未润洗(偏高);
②酸式滴定管水洗后,误用待测液润洗(偏高);
③碱式滴定管水洗后,未润洗(偏低);
④锥形瓶水洗后,用待测液润洗(偏高)。
(5)量器读数
①滴定前俯视酸式滴定管,滴定后平视(偏高);
滴定前仰视酸式滴定管,滴定后俯视(偏低)如图所示;
③滴定完毕后,立即读数,半分钟后颜色又褪去(偏低)。
(5)操作不当
①滴定前酸式滴定管尖嘴部分有气泡,滴定结束后气泡消失(偏高);
②滴定过程中,振荡锥形瓶时,不小心将溶液溅出(偏低);
③滴定过程中,锥形瓶内加少量蒸馏水(无影响)。
第三节盐类的水解
1、探究盐溶液的酸碱性
强碱和弱酸反应生成的盐的水溶液呈碱性;
强酸和弱碱反应生成的盐的水溶液呈酸性;
强酸和强碱反应生成的盐的水溶液呈中性。
2、盐溶液呈现不同酸碱性的原因
(1)探究盐溶液呈现不同酸碱性的原因
盐溶液的酸碱性与盐所含的离子在水中能否与水电离出的H+或OH-生成弱电解质有关。
(2)盐类水解的定义:
在溶液中盐电离出来的离子跟水电离出来的H+或OH-原结合生成弱电解质的反应,叫做盐类的水解。
盐类水解的实质是水的电离平衡发生了移动。
可看作中和反应的逆反应。
(3)盐类水解规律:
①“有弱才水解,无弱不水解;
越弱越水解,都弱都水解;
谁强显谁性,同强显中性”
②多元弱酸根,浓度相同时正酸根比酸式酸根水解程度大,碱性更强。
(如:
Na2CO3>NaHCO3)
✧酸式盐溶液的酸碱性:
a只电离不水解:
如HSO4-显酸性
b电离程度>水解程度,显酸性(如:
HSO3-、H2PO4-)
c水解程度>电离程度,显碱性(如:
HCO3-、HS-、HPO42-)
多元弱酸的酸式酸根离子既有水解倾向又有电离倾向,以水解为主的,溶液显碱性;
以电离为主的溶液显酸性。
例如:
HCO3-、HPO42-在溶液中以水解为主,其溶液显碱性;
HSO3-、H2PO4-在溶液中以电离为主,其溶液显酸性。
✧混合溶液的酸碱性:
a.电离程度>水解程度,显酸性
b.水解程度>电离程度,显碱性
✧双水解反应:
①构成盐的阴阳离子均能发生水解的反应。
双水解反应相互促进,水解程度较大,有的甚至水解完全。
使得平衡向右移。
②常见的双水解反应完全的为:
Fe3+、Al3+与AlO2-、CO32-(HCO3-)、S2-(HS-)、SO32-(HSO3-);
S2-与NH4+;
CO32-(HCO3-)
与NH4+其特点是相互水解成沉淀或气体。
双水解完全的离子方程式配平依据是两边电荷平衡,如:
2Al3++3S2-+6H2O==2Al(OH)3↓+3H2S↑
③盐类水解的特点:
(1)可逆(与中和反应互逆)
(2)程度小(3)吸热
(4)影响盐类水解的外界因素:
①温度:
温度越高,水解程度越大(水解吸热,越热越水解)
②浓度:
浓度越小,水解程度越大(越稀越水解)
③酸碱:
促进或抑制盐的水解(H+促进阴离子水解而抑制阳离子水解;
OH-促进阳离子水解而抑制阴离子水解)
(5)盐类水解的应用:
水解的应用
原理
1、净水
明矾净水
2、去油污
用热碱水冼油污物品
△
CO32-+H2OHCO3-+OH-
3、药品的保存
①配制FeCl3溶液时常加入少量盐酸
Fe3++3H2OFe(OH)3+3H+
②配制Na2CO3溶液时常加入少量NaOH
4、制备无水盐
由MgCl2·
6H2O制无水MgCl2在HCl气流中加热
若不然,则:
MgCl2·
6H2OMg(OH)2+2HCl+4H2O
Mg(OH)2MgO+H2O
5、泡沫灭火器
用Al2(SO4)3与NaHCO3溶液混合
Al3++3HCO3-=Al(OH)3↓+3CO2↑
(6)盐类水解方程式的书写一般要注意一下几点:
a一般来说盐类水解的程度不大,是中和反应的逆反应,由于中和反应趋于完成,所以盐类的水解反应是微弱的,盐类水解的离子方程式写“”。
由于盐类的水解程度一般都很小,通常不生成沉淀和气体,因此盐类水解的离子方程式中一般不标“↓”或“↑”的气标,也不把生成物(如NH3·
H2O、H2CO3等)写成其分解产物的形式。
b能发生双水解的离子组,一般来说水解都比较彻底,由于不形成水解平衡,书写时生成物出现的沉淀、气体物质要标明状态,即标上“↓”、“↑”符号,中间用“==”连接,如NaHCO3溶液与Al2(SO4)3溶液混合:
Al3++3HCO3-==Al(OH)3↓+3CO2↑
c多元弱酸的酸根离子水解是分步进行的,且以第一步水解为主;
多元弱碱的阳离子水解复杂,可看做一步水解。
扩展:
溶液中微粒浓度的大小比较
☆☆基本原则:
抓住溶液中微粒浓度必须满足的三种守恒关系:
①电荷守恒:
任何溶液均显电中性,各阳离子浓度与其所带电荷数的乘积之和=各阴离子浓度与其所带电荷数的乘积之和
②物料守恒(即原子个数守恒或质量守恒):
某原子的总量(或总浓度)=其以各种形式存在的所有微粒的量(或浓度)之和。
③质子守恒:
即水电离出的H+浓度与OH-浓度相等。
第四节难溶电解质的溶解平衡
1、难溶电解质的溶解平衡
(1)难溶物质的溶解度根据溶解度大小,我们把物质分为难溶、易溶、微溶和不溶等。
溶解度与溶解性的关系
(2)沉淀溶解平衡
①沉淀溶解平衡的定义
在一定条件下,难溶电解质溶于水形成饱和溶液时,溶解速度与沉淀速度相等,溶质的离子与该固态物质之间建立了动态平衡,叫做沉淀溶解平衡。
②溶解平衡的特征
“逆”——沉淀溶解过程是可逆的。
“动”——动态平衡,溶解的速率和沉淀的速率并不为0。
“等”——。
“定”——达到平衡时,溶液中离子的浓度保持不变。
“变”——当改变外界条件时,溶解平衡将发生移动,达到新的平衡。
溶解平衡常为吸热,但Ca(OH)2为放热,升温其溶解度减少。
(3)溶解平衡方程式的书写
注意在沉淀后用(s)标明状态,并用“”。
如:
Ag2S(s)2Ag+(aq)+S2-(aq)
2、沉淀反应的应用
由于难溶电解质的溶解平衡也是动态平衡,因此可以通过改变条件使平衡移动——溶液中的离子转化为沉淀,或沉淀转化为溶液中的离子。
(1)沉淀的溶解
加入的试剂能与沉淀所产生的离子发生反应,生成挥发性物质或弱电解质(弱酸、弱碱或水)使溶解平衡向溶解的方向移动,则沉淀就会溶解。
(2)沉淀的转化
溶解度大的生成溶解度小的,溶解度小的生成溶解度更小的。
AgNO3AgCl(白色沉淀)AgBr(淡黄色)AgI(黄色)Ag2S(黑色)
(3)溶度积
在一定条件下,难溶强电解质AmBn溶于水形成饱和溶液时,溶质的离子与该固态物质之间建立动态平衡,这时,离子浓度的乘积为一常数,叫做溶度积Ksp。
②表达式:
对于难溶电解质在任一时刻都有
通过比较溶度积与溶液中有关离子浓度幂的乘积——离子积Qc的相对大小,可以判断难溶电解质在给定条件下沉淀能否生成或溶解。
Qc>
Ksp,溶液过饱和,有沉淀析出,直至溶液饱和,达到新的平衡。
Qc=Ksp,溶液饱和,沉淀与溶解处于平衡状态。
Qc<
Ksp,溶液未饱和,无沉淀析出,若加入过量难溶电解质,难溶电解质溶解直至溶液饱和。
③影响因素:
外因:
a浓度:
加水,平衡向溶解方向移动,但Ksp不变。
b温度:
升温,多数平衡向溶解方向移动。
c同离子效应:
平衡向生成沉淀方向移动。
(4)沉淀生成的主要方式
①加沉淀剂法:
Ksp越小(即沉淀越难溶),沉淀越完全;
沉淀剂过量能使沉淀更完全。
②调pH值除某些易水解的金属阳离子:
如加MgO除去MgCl2溶液中FeCl3。
③同离子效应法