高中化学复习知识点沉淀转化文档格式.docx
《高中化学复习知识点沉淀转化文档格式.docx》由会员分享,可在线阅读,更多相关《高中化学复习知识点沉淀转化文档格式.docx(14页珍藏版)》请在冰豆网上搜索。
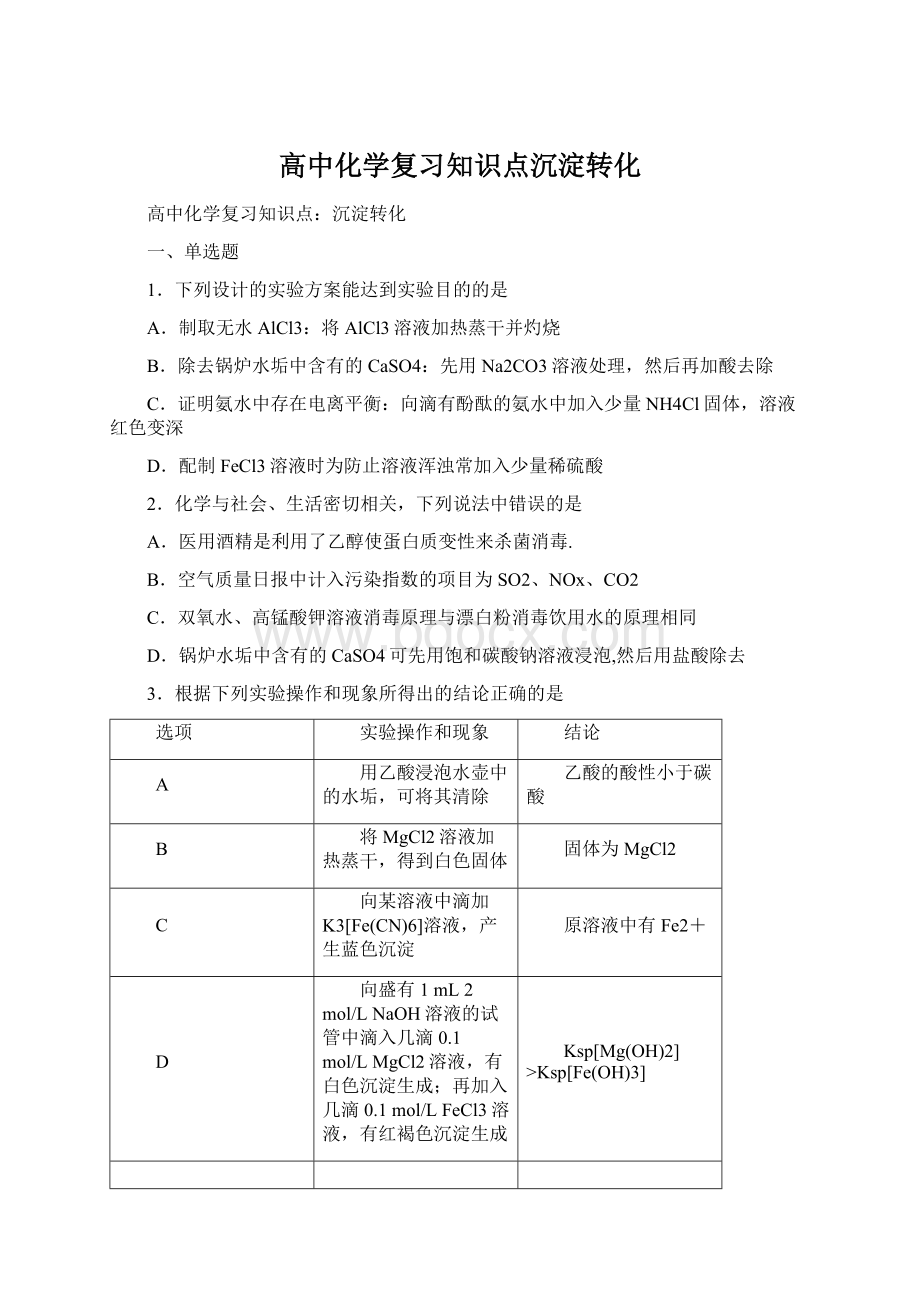
D
向盛有1mL2mol/LNaOH溶液的试管中滴入几滴0.1mol/LMgCl2溶液,有白色沉淀生成;
再加入几滴0.1mol/LFeCl3溶液,有红褐色沉淀生成
Ksp[Mg(OH)2]>
Ksp[Fe(OH)3]
A.AB.BC.CD.D
4.下列装置能达到实验目的的是()
A.探究AgCl和AgI之间的转化
B.比较Cl2、Br2、I2的氧化性强弱
C.制备Fe(OH)2
D.用已知浓度的氢氧化钠溶液测定盐酸浓度的实验
5.下列实验装置中所用仪器、试剂、现象和结论均正确的是
装置
现象
装置Ⅲ中有浅黄色沉淀生成
苯和浓溴水发生取代反应
高锰酸钾溶液褪色,溴的四氯化碳溶液褪色
石蜡油的分解产物中含有乙烯
分液漏斗液体流下,锥形瓶中产生大量气体
快速制备和收集一定量的氨气
试管中依次出现白色,黄色沉淀
说明Ksp(AgCl)>
Ksp(AgI)
6.根据下列实验操作和现象所得到的结论正确的是
实验
向苯酚浊液中加入Na2CO3溶液
溶液变澄清
酸性:
苯酚>
碳酸
向20%蔗糖溶液中加入少量稀硫酸,加热;
再加入银氨溶液并水浴加热
未出现银镜
蔗糖未水解
向2支盛有2mL相同浓度银氨溶液的试管中,分别加入2滴相同浓度的NaCl和NaI溶液
一支无明显现象,另一支产生黄色沉淀
相同条件下,AgI比
AgCl的溶解度小
C2H5OH与浓硫酸170℃共热,制得的气体通入酸性KMnO4溶液
KMnO4溶液褪色
乙烯能被KMnO4氧化
7.下列实验操作规范且能达到相应实验目的的是
实验目的
实验操作
配制100g4%的NOH溶液
称取4.0gNaOH放在烧杯中,再加入96.0mL水,搅拌均匀
B.
分离KClO3与MnO2制取O2后的残渣
溶解、过滤、洗涤、干燥滤渣得到MnO2,滤液蒸发结晶并干燥得到KClO3
证明
Ksp(BaSO4)<
Ksp(BaCO3)
向BaCO3溶液中加入饱和Na2SO4溶液
检验Al和Fe2O3反应后固体中是否含Fe2O3
取样,溶于足量稀硫酸,滴加KSCN溶液不变红,说明不含Fe2O3
8.取1mL0.1mol·
L-1AgNO3溶液进行如下实验(实验中所用试剂浓度均为0.1mol·
L
):
下列说法不正确的是
A.实验①白色沉淀是难溶的AgCl
B.由实验②说明AgI比AgCl更难溶
C.若按①③②顺序实验,看不到黑色沉淀
D.若按②①③顺序实验,看不到白色沉淀
二、多选题
9.室温下进行下列实验,根据实验操作和现象所得到的结论正确的是()
向CuSO4溶液中通入H2S,生成黑色沉淀(CuS)
H2S的酸性比H2SO4强
向PbO2中滴加浓盐酸,出现黄绿色气体
PbO2具有氧化性
在酒精灯上加热铝箔,铝箔熔化但不滴落
熔点:
氧化铝>铝
向NaCl和NaBr混合溶液中滴加少量AgNO3溶液,出现淡黄色沉淀(AgBr)
Ksp(AgCl)>Ksp(AgBr)
10.下列根据实验操作和现象所得出的结论正确的是()
实验现象
向浓度均为0.1mol·
L-1的NaCl和NaI混合溶液中滴加少量AgNO3溶液
先出现黄色沉淀
Ksp(AgCl)<Ksp(AgI)
苯酚>HCO3-
用饱和碳酸钠溶液浸泡锅炉沉积物后,再加入稀盐酸
有气泡产生
可除去锅炉沉积物中的CaSO4
淀粉与稀硫酸混和一段时间后,滴加银氨溶液并水浴
无银镜出现
淀粉没有水解
三、综合题
11.某电镀铜厂有两种废水,分别含有CN-和Cr2O72-等有毒离子,拟用NaClO和Na2S2O3按照下列流程进行处理。
请完成下列填空:
(1)HCN有剧毒,电子式是__,其分子属于__(填“极性”、“非极性”)分子。
(2)表示原子结构的化学用语有:
原子结构示意图、核外电子排布式、轨道表示式。
从中选择最详尽描述核外电子运动状态的方式,来表示氧原子的最外层电子的运动状态:
__,其中最外层有__种不同能量的电子。
(3)下列事实能说明氯与硫两元素非金属性相对强弱的是___。
a.相同条件下水溶液的pH:
NaClO>Na2S2O3
b.还原性:
H2S>HCl
c.相同条件下水溶液的酸性:
HClO3>H2SO3
d.稳定性:
HCl>H2S
(4)写出流程③的离子方程式为:
___。
(5)反应③中,每消耗0.5molCr2O72-转移的电子数为___;
(6)取少量待测水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀,解释产生该现象的原因___。
12.最近有科学家提出“绿色自由”的构想:
把含有CO2的空气吹入K2CO3溶液中,然后再用高温水气分解出CO2,经与H2化合后转变为甲醇燃料.
(1)在整个生产过程中饱和K2CO3溶液的作用是_______;
不用KOH溶液的理由是_________。
(2)在合成塔中,每44gCO2与足量H2完全反应生成甲醇时,可放出49.5kJ的热量,试写出合成塔中发生反应的热化学方程式_______________;
转化过程中可循环利用的物质除了K2CO3外,还有___________。
(3)请评述合成时选择2×
105Pa的理由_____________________________________。
(4)BaCO3的溶解平衡可以表示为BaCO3(s)⇌Ba2++CO32﹣
①写出平衡常数表达式___________________;
②用重量法测定空气中CO2的体积分数时,选用Ba(OH)2而不是Ca(OH)2为沉淀剂,原因之一是:
25℃时,BaCO3的溶解平衡常数K=2.58×
10﹣9,而CaCO3的溶解平衡常数K=4.96×
10﹣9;
原因之二是_________________________。
(5)某同学很快就判断出以下中长石风化的离子方程式未配平:
4Na0.5Ca0.5Al1.5Si2.5O6+6CO2+17H2O=2Na++2Ca2++5HCO3﹣+4H4SiO4+3Al2SiO5(OH)4
该同学判断的角度是______________。
(6)甲醇可制成新型燃料电池,总反应为:
2CH3OH+3O2+4KOH=2K2CO3+6H2O该电池负极的电极反应式为:
CH3OH﹣6e+8OH﹣=CO32﹣+6H2O则正极的电极反应式为:
______________。
参考答案
1.B
【解析】
【详解】
A.AlCl3在加热时水解生成Al(OH)3和HCl,HCl易挥发,蒸干灼烧得到的是Al2O3,无法获得AlCl3晶体,选项A错误;
B.硫酸钙难以除去,可加入碳酸钠转化为碳酸钙,加入盐酸即可除去,选项B正确;
C.一水合氨为弱碱,溶液中存在电离平衡:
NH3•H2O
NH4++OH-,加入酚酞后溶液变为红色,而NH4Cl=NH4++Cl-,其中的NH4+会抑制氨水的电离,使溶液碱性减弱,颜色变浅,选项C错误;
D、Fe3+易水解,水解生成H+,水解的离子方程式为Fe3++3H2
Fe(OH)3+3H+,配制溶液时,可加入酸抑制FeCl3水解,防止生成沉淀而导致溶液变浑浊,由于溶液是FeCl3溶液,所以选加HCl,不能用其它的酸,选项D错误。
答案选B。
2.B
【分析】
A.乙醇使蛋白质变性,医用酒精能杀菌消毒,故A正确;
B.CO2不是空气质量日报污染指数项目,故B错误;
C.双氧水、高锰酸钾溶液消毒,漂白粉消毒饮用水都是利用强氧化性,故C正确;
D.锅炉水垢中含有的CaSO4可先用饱和碳酸钠溶液浸泡转化为碳酸钙沉淀,然后用盐酸除去,故D正确;
选B。
3.C
A.用乙酸浸泡水壶中的水垢,可将其清除,根据强酸制弱酸的原理,乙酸的酸性大于碳酸,故A错误;
B.将MgCl2溶液加热蒸干发生水解得到
固体,最终分解得到MgO,故B错误;
C.向某溶液中滴加K3[Fe(CN)6]溶液,产生蓝色沉淀则可证明Fe2+的存在,故C正确;
D.NaOH过量,均为沉淀生成,不能比较Ksp,故D错误;
故答案选:
C。
4.C
A.硝酸银过量,生成氯化银沉淀后,Ag+剩余,继续生成碘化银沉淀,无法探究AgCl和AgI之间的转化,故A错误;
B.氯气依次通过两棉球,通过现象可以证明氯气的氧化性强于Br2和I2,但无法比较Br2、I2的氧化性,故B错误;
C.根据装置特点分析,先打开a和b,A中生成的氢气排出装置的空气,防止Fe(OH)2被氧化,关闭a时,生成的氢气将A中反应产物硫酸亚铁通过导管压入B中的氢氧化钠溶液中,反应得到Fe(OH)2,故C正确;
D.氢氧化钠溶液应该装在碱式滴定管内(下部为橡胶管),故D错误;
故选C。
5.D
A.溴易挥发,溴及生成HBr均与硝酸银反应,则装置Ⅲ中有浅黄色沉淀,不能说明取代反应的发生,故A错误;
B.高锰酸钾、溴的四氯化碳溶液均褪色,可知生成不同于烷烃的气体,则石蜡油的分解产物中含有不饱和烃,不一定就是乙烯,故B错误;
C.收集一定量的氨气时,试管口要塞上一团棉花,以防止对流,故C错误;
D.先制得AgCl的悬浊液,向白色AgCl悬浊液中滴加足量的KI溶液,试管中白色沉淀转化为黄色沉淀,说明AgI溶解度更小,AgCl和AgI组成相似,可以比较Ksp,说明Ksp(AgCl)>Ksp(AgI),故D正确;
故选D。
6.C
A.苯酚浊液中滴加Na2CO3溶液,反应生成苯酚钠、碳酸氢钠,可知苯酚的酸性比碳酸的酸性弱,A项错误;
B.做银镜反应加入银氨溶液前,要先中和水解的硫酸,B项错误;
C.相同浓度银氨溶液的试管中,分别加入2滴相同浓度的NaCl和NaI溶液,出现黄色沉淀,说明生成碘化银沉淀,说明Ksp(AgI)<Ksp(AgCl),C项正确;
D.反应中可能生成其他的还原性气体使KMnO4溶液褪色,验证乙烯能被KMnO4氧化前要先除杂,D项错误;
答案选C。
7.A
A、100g4%的NOH溶液,溶质的质量为4.0g,溶剂水的质量为96.0g,称取4.0gNaOH放在烧杯中,再加入96.0mL水,搅拌均匀即可,A正确;
B、KClO3与MnO2制取O2后的残渣为不溶水的MnO2和溶于水的KCl,溶解、过滤、洗涤、干燥滤渣得到MnO2,滤液蒸发结晶并干燥得到KCl,B错误;
C、向BaCO3悬浊液中加入足量饱和Na2SO4溶液,当沉淀不再变化时,加入稀盐酸,无明显现象,即可证明Ksp(BaSO4)<
Ksp(BaCO3),C错误;
D、Al和Fe2O3反应后固体中一定含有Fe单质,若含有Fe2O3,与酸发应后生成Fe3+,Fe3+可能与Fe单质反应成Fe2+,加入KSCN溶液也不变红,D错误。
正确答案为A。
点睛:
本题难点在C和D选项,对C选项:
沉淀之间的转化,必须是一种沉淀转化为另外一种沉淀,而不是生成的,如C中应该使用BaCO3悬浊液,一种沉淀转化为另一种沉淀,可通过颜色的改变来观察,如无颜色的变化,则必须通过其他方法来证明确实生成了新的沉淀,如C中BaCO3和BaSO4均为白色沉淀,无法直接观察,可通过向生成的沉淀中加硝酸,看沉淀是否溶解来判断。
对D选项:
要考虑反应后固体中加硫酸后,Fe单质可能与Fe3+反应生成Fe2+,溶液也不显色。
8.C
取1mL0.1mol·
L-1AgNO3溶液中加入过量氯化钠溶液生成氯化银白色沉淀,滴加过量KI溶液生成黄色沉淀碘化银,再加入过量硫化钠溶液生成硫化银沉淀,沉淀转化的实质是向更难溶的方向进行。
A.分析可知,实验①白色沉淀是难溶的AgCl,A正确;
B.由实验②说明AgI比AgCl更难溶,可以实现沉淀转化,B正确;
C.若按①③顺序实验,硫化银溶解度小于氯化银,也可以实现转化看到黑色沉淀生成,C错误;
D.由实验②说明AgI比AgCl更难溶,若按②①顺序实验,此条件下碘化银不能转化为氯化银,看不到白色沉淀,D正确;
9.BC
A.H2S是弱酸,H2SO4是强酸,结论错误,A错误;
B.Cl从-1价升高到0价,被氧化,PbO2具有氧化性,B正确;
C.铝箔表面迅速形成氧化铝,内部依然是铝,铝箔熔化但不滴落,说明外面的氧化铝熔点高于里面的Al,C正确;
D.向NaCl和NaBr混合溶液中滴加少量AgNO3溶液,出现淡黄色沉淀(AgBr),有可能是Cl-浓度太小,D错误。
答案选BC。
【点睛】
根据沉淀溶解平衡:
可以知道,两种离子形成沉淀是需要条件的,即Qc
Ksp,所以D答案没有出现白色沉淀,出现淡黄色沉淀不一定是白色沉淀转换为淡黄色沉淀了,还可能是Cl-浓度太小了。
10.BC
A.同类型的沉淀,溶度积小的沉淀先析出,即Ksp(AgCl)>
Ksp(AgI),A选项错误;
B.苯酚与碳酸钠反应生成苯酚钠和碳酸氢钠,则溶液变澄清,说明酸性:
HCO3-,B选项正确;
C.用饱和碳酸钠溶液浸泡锅炉沉积物后,锅炉沉积物会转化为碳酸钙,再加入稀盐酸,碳酸钙溶解,可除去锅炉沉积物中的CaSO4,C选项正确;
D.淀粉在酸性条件下水解生成葡萄糖,葡萄糖的银镜反应应在碱性条件下进行,题目没有调节溶液至碱性,D选项错误;
本题主要考查化学实验方案的评价,设计离子检验、有机物性质实验及淀粉的水解等,综合性较强,选项B为易错点,注意把握实验的严密性和可行性的评价。
11.
极性
2bd3S2O32-+4Cr2O72-+26H+→6SO42-+8Cr3++13H2O3.0NA(或1.806×
1024)Cu2++2OH-=Cu(OH)2↓、Cu(OH)2(s)+S2−(aq)
CuS(s)+2OH-(aq)或相同温度下,S(CuS)<
S[Cu(OH)2],使沉淀的溶解平衡向更难溶的方向转化
⑴利用达到稳定需要的电子来分析电子对数,HCN没有对称性。
⑵最详尽描述核外电子运动状态的是轨道表示式,1个能级就是一种能量电子。
⑶a.最高价氧化物对应水化物的相同阳离子的盐(一般钠盐)的pH越大,则对应酸越弱,非金属性越弱,因此比较相同条件下水溶液的pH:
NaClO>Na2S2O3,不能比较非金属性,因为不是最高价氧化物对应水化物的钠盐;
b.非金属性越强,其简单氢化物还原性越弱,还原性:
H2S>HCl,说明氯非金属性与硫强;
c.非金属越强,其最高价氧化物对应水化物酸性越强,相同条件下水溶液的酸性:
HClO3>H2SO3,不是最高价氧化物对应水化物的酸性,因此不能比较;
d.非金属性越强,其简单氢化物越稳定,稳定性:
HCl>H2S,因此能说明氯非金属性比硫强。
⑷流程③是S2O32−与Cr2O72−在酸性条件下反应生成SO42−、Cr3+和H2O。
⑸根据离子方程式分析化合价降低得到电子数目。
⑹加入NaOH溶液观察到有蓝色沉淀生成,Cu2++2OH-=Cu(OH)2↓,继续加至不再产生蓝色沉淀为止,生成了氢氧化铜,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀,说明难溶的氢氧化铜转变成更难溶的硫化铜。
⑴HCN有剧毒,氢和碳共用一对电子,碳和氮共用三对电子,因此电子式是
,HCN没有对称性,其分子属于极性分子;
故答案为:
;
极性。
⑵最详尽描述核外电子运动状态的是轨道表示式,氧原子的最外层有6个电子,其最外层电子的运动状态:
,1个能级就是一种能量,因此最外层有2种不同能量的电子;
2。
NaClO>Na2S2O3,不能比较非金属性,因为不是最高价氧化物对应水化物的钠盐,故a不符合题意;
H2S>HCl,说明氯非金属性与硫强,故b符合题意;
HClO3>H2SO3,不是最高价氧化物对应水化物的酸性,因此不能比较,故c不符合题意;
HCl>H2S,因此能说明氯非金属性比硫强,故d符合题意;
综上所述,答案为bd。
⑷流程③是S2O32−与Cr2O72−在酸性条件下反应生成SO42−、Cr3+和H2O,其离子方程式为:
3S2O32−+4Cr2O72−+26H+=6SO42−+8Cr3++13H2O;
3S2O32−+4Cr2O72−+26H+=6SO42−+8Cr3++13H2O。
⑸反应③中,根据离子方程式可知1molCr2O72−转移了6mol电子,因此每消耗0.5molCr2O72−转移的电子物质的量为0.5mol×
6=3mol,电子数为3NA;
3NA(或1.806×
1024);
⑹取少量待测水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,Cu2++2OH-=Cu(OH)2↓,继续加至不再产生蓝色沉淀为止,生成了氢氧化铜再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀,说明难溶的氢氧化铜转变成更难溶的硫化铜,Cu(OH)2(s)+S2−(aq)
CuS(s)+2OH-(aq);
Cu2++2OH-=Cu(OH)2↓、Cu(OH)2(s)+S2−(aq)
S[Cu(OH)2],使沉淀的溶解平衡向更难溶的方向转化。
12.富集CO2生成的K2CO3难分解产生CO2CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=﹣49.5kJ/mol水蒸气适当加压有利于提高反应速率和原料利用率,但压强太高增大成本K=c(Ba2+)c(CO32﹣)BaCO3的式量大,相对误差小未配平两边电荷数O2+2H2O+4e-=4OH﹣
(1)碳酸氢钾不稳定,加热时分解生成碳酸钾和二氧化碳、水,碳酸钾不分解;
(2)4.4kgCO2的物质的量是100mol,100mol二氧化碳和足量氢气反应放出4947KJ热量,据此计算1mol二氧化碳与足量氢气反应放出的热量,从而写出其热化学反应方程式;
根据合成甲醇的方程可知,反应生成甲醇和水蒸气,水蒸气可以给碳酸氢钾分解提供能量;
(3)合成甲醇的反应为体积减小的反应,增大压强平衡正移;
(4)①溶解平衡方程式书写平衡常数表达式;
②重量法测定空气中CO2的体积分数,要求称量准确,误差小;
(5)书写离子方程式要注意原子守恒和电荷守恒;
(6)碱性甲醇燃料电池中,甲醇在负极失电子,氧气在正极得电子。
(1)在整个生产过程中饱和K2CO3溶液的作用是富集二氧化碳,二氧化碳和饱和的碳酸钾溶液反应生成碳酸氢钾,碳酸氢钾不稳定,加热时分解生成碳酸钾、二氧化碳和水,KOH溶液与二氧化碳是碳酸钾,K2CO3难分解产生CO2;
(2)44gCO2的物质的量是1mol,1mol二氧化碳和足量氢气反应放出49.5kJ热量,所以其热化学反应方程式为:
CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=﹣49.5kJ/mol;
根据合成甲醇的方程可知,反应生成甲醇和水蒸气,水蒸气可以给碳酸氢钾分解提供能量,所以转化过程中可循环利用的物质除了K2CO3外,还有水蒸气;
(3)合成甲醇的反应为体积减小的反应,增大压强平衡正移,有利于提高反应速率和原料利用率,但是压强太高对反应的设备要求很高,又提高了生产成本,所以不能太高;
4)①BaCO3的溶解平衡可以表示为BaCO3(s)⇌Ba2++CO32﹣,平衡常数表达式为K=c(Ba2+)c(CO32﹣);
②重量法测定空气中CO2的体积分数,要求称量准确,误差小,BaCO3的式量大,称量的相对误差小;
(5)书写离子方程式要注意原子守恒和电荷守恒,4Na0.5Ca0.5Al1.5Si2.5O6+6CO2+17H2O=2Na++2Ca2++5HCO3﹣+4H4SiO4+3Al2SiO5(OH)4中电荷不守恒,原子个数也不守恒,所以离子方程式错误;
(6)碱性甲醇燃料电池中,甲醇在负极失电子,氧气在正极得电子生成氢氧根离子,则正极反应式为:
O2+2H2O+4e-=4OH﹣。