专题十 水的电离和溶液的酸碱性Word下载.docx
《专题十 水的电离和溶液的酸碱性Word下载.docx》由会员分享,可在线阅读,更多相关《专题十 水的电离和溶液的酸碱性Word下载.docx(21页珍藏版)》请在冰豆网上搜索。
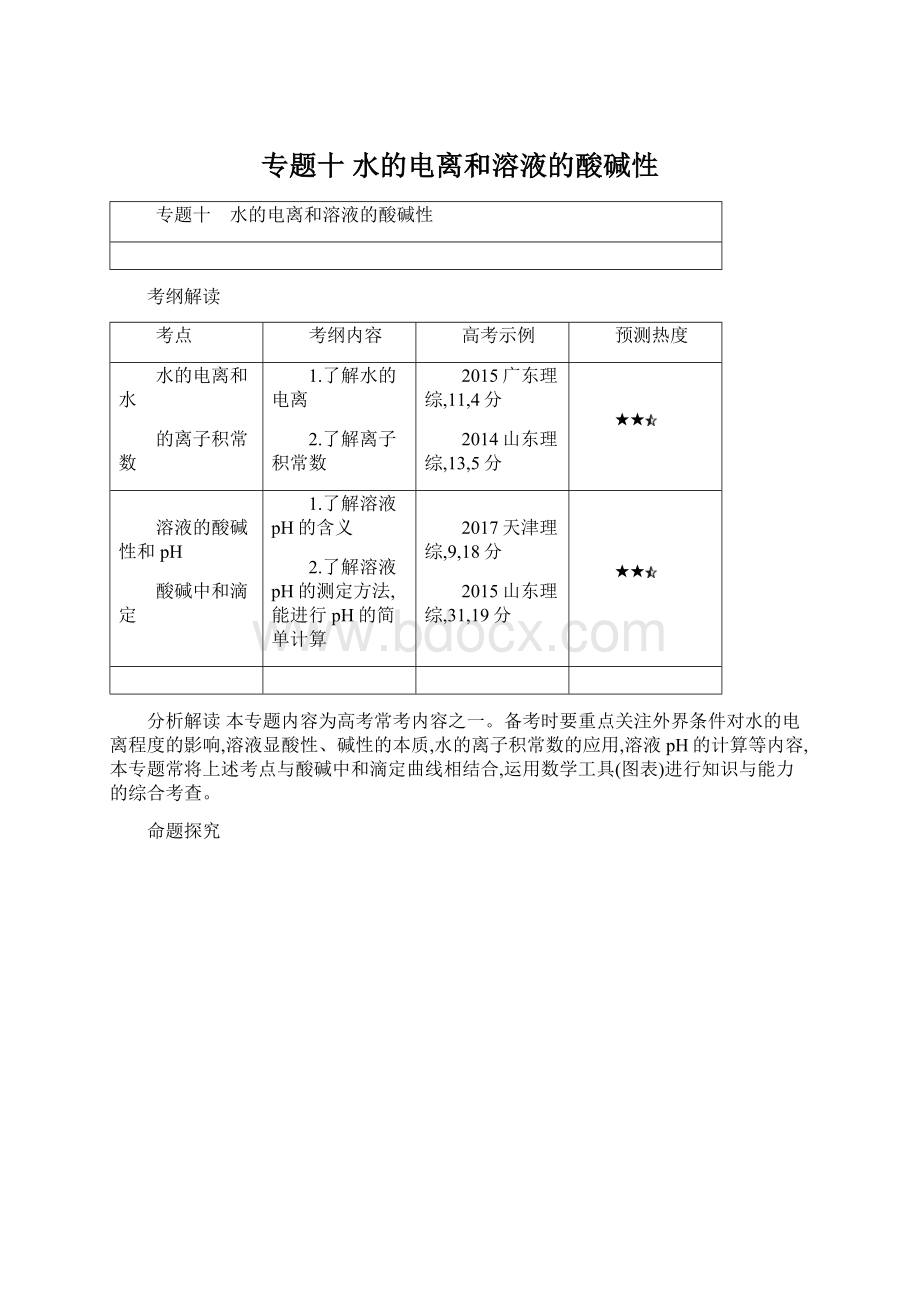
D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
4.(2013山东理综,13,4分)某温度下,向一定体积0.1mol·
L-1的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示,则( )
A.M点所示溶液的导电能力强于Q点
B.N点所示溶液中c(CH3COO-)>
c(Na+)
C.M点和N点所示溶液中水的电离程度相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
考点二 溶液的酸碱性和pH 酸碱中和滴定
1.(2016天津理综,6,6分)室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·
L-1的三种酸(HA、HB和HD)溶液,滴定曲线如图所示,下列判断错误的是( )
A.三种酸的电离常数关系:
KHA>
KHB>
KHD
B.滴定至P点时,溶液中:
c(B-)>
c(Na+)>
c(HB)>
c(H+)>
c(OH-)
C.pH=7时,三种溶液中:
c(A-)=c(B-)=c(D-)
D.当中和百分数达100%时,将三种溶液混合后:
c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
2.(2015重庆理综,3,6分)下列叙述正确的是( )
A.稀醋酸中加入少量醋酸钠能增大醋酸的电离程度
B.25℃时,等体积等浓度的硝酸与氨水混合后,溶液pH=7
C.25℃时,0.1mol·
L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱
D.0.1molAgCl和0.1molAgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-)
3.(2015广东理综,12,4分)准确移取20.00mL某待测HCl溶液于锥形瓶中,用0.1000mol·
L-1NaOH溶液滴定,下列说法正确的是( )
A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B.随着NaOH溶液滴入,锥形瓶中溶液pH由小变大
C.用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定
D.滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小
答案 B
4.(2013浙江理综,12,6分)25℃时,用浓度为0.1000mol·
L-1的NaOH溶液滴定20.00mL浓度均为0.1000mol·
L-1的三种酸HX、HY、HZ,滴定曲线如下图所示。
下列说法正确的是( )
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:
HZ<
HY<
HX
B.根据滴定曲线,可得Ka(HY)≈10-5
C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:
c(X-)>
c(Y-)>
c(OH-)>
c(H+)
D.HY与HZ混合,达到平衡时:
c(H+)=
+c(Z-)+c(OH-)
5.(2017天津理综,9,18分)用沉淀滴定法快速测定NaI等碘化物溶液中c(I-),实验过程包括准备标准溶液和滴定待测溶液。
Ⅰ.准备标准溶液
a.准确称取AgNO3基准物4.2468g(0.0250mol)后,配制成250mL标准溶液,放在棕色试剂瓶中避光保存,备用。
b.配制并标定100mL0.1000mol·
L-1NH4SCN标准溶液,备用。
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中。
b.加入25.00mL0.1000mol·
L-1AgNO3溶液(过量),使I-完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.1000mol·
L-1NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。
三次测定数据如下表:
实验序号
1
2
3
消耗NH4SCN标准溶液体积/mL
10.24
10.02
9.98
f.数据处理。
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有 。
(2)AgNO3标准溶液放在棕色试剂瓶中避光保存的原因是 。
(3)滴定应在pH<
0.5的条件下进行,其原因是 。
(4)b和c两步操作是否可以颠倒 ,说明理由
。
(5)所消耗的NH4SCN标准溶液平均体积为 mL,测得c(I-)= mol·
L-1。
(6)在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为 。
(7)判断下列操作对c(I-)测定结果的影响(填“偏高”“偏低”或“无影响”)。
①若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果 。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果 。
答案 (18分)
(1)250mL(棕色)容量瓶、胶头滴管
(2)避免AgNO3见光分解
(3)防止因Fe3+的水解而影响滴定终点的判断(或抑制Fe3+的水解)
(4)否(或不能) 若颠倒,Fe3+与I-反应,指示剂耗尽,无法判断滴定终点
(5)10.00 0.0600
(6)用NH4SCN标准溶液进行润洗
(7)偏高 偏高
6.(2015山东理综,31,19分)毒重石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·
2H2O的流程如下:
(1)毒重石用盐酸浸取前需充分研磨,目的是 。
实验室用37%的盐酸配制15%的盐酸,除量筒外还需使用下列仪器中的 。
a.烧杯b.容量瓶c.玻璃棒d.滴定管
(2)加入NH3·
H2O调pH=8可除去 (填离子符号),滤渣Ⅱ中含 (填化学式)。
加入H2C2O4时应避免过量,原因是 。
已知:
Ksp(BaC2O4)=1.6×
10-7,Ksp(CaC2O4)=2.3×
10-9
Ca2+
Mg2+
Fe3+
开始沉淀时的pH
11.9
9.1
1.9
完全沉淀时的pH
13.9
11.1
3.2
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
2Cr
+2H+
Cr2
+H2O Ba2++Cr
BaCrO4↓
步骤Ⅰ:
移取xmL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用bmol·
L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V0mL。
步骤Ⅱ:
移取ymLBaCl2溶液于锥形瓶中,加入xmL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用bmol·
L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。
滴加盐酸标准液时应使用酸式滴定管,“0”刻度位于滴定管的 (填“上方”或“下方”)。
BaCl2溶液的浓度为 mol·
若步骤Ⅱ中滴加盐酸时有少量待测液溅出,Ba2+浓度测量值将 (填“偏大”或“偏小”)。
答案
(1)增大接触面积从而使反应速率加快 a、c
(2)Fe3+ Mg(OH)2、Ca(OH)2 H2C2O4过量会导致生成BaC2O4沉淀,产品产量减少
(3)上方
偏大
教师用书专用(7—12)
7.(2014四川理综,6,6分)下列溶液中粒子的物质的量浓度关系正确的是( )
A.0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:
c(C
)>
c(HC
B.20mL0.1mol/LCH3COONa溶液与10mL0.1mol/LHCl溶液混合后溶液呈酸性,所得溶液中:
c(CH3COO-)>
c(Cl-)>
c(CH3COOH)>
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:
c(Cl-)+c(H+)>
c(N
)+c(OH-)
D.0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:
c(H+)+c(CH3COOH)
8.(2013大纲全国,12,6分)下图表示水中c(H+)和c(OH-)的关系,下列判断错误的是( )
A.两条曲线间任意点均有c(H+)×
c(OH-)=KW
B.M区域内任意点均有c(H+)<
C.图中T1<
T2
D.XZ线上任意点均有pH=7
9.(2013课标Ⅱ,13,6分)室温时,M(OH)2(s)
M2+(aq)+2OH-(aq) Ksp=a。
c(M2+)=bmol·
L-1时,溶液的pH等于( )
A.
lg(
)B.
)
C.14+
lg(
)D.14+
10.(2013江苏单科,11,4分)下列有关说法正确的是(双选)( )
A.反应NH3(g)+HCl(g)
NH4Cl(s)在室温下可自发进行,则该反应的ΔH<
B.电解法精炼铜时,以粗铜作阴极,纯铜作阳极
C.CH3COOH溶液加水稀释后,溶液中
的值减小
D.Na2CO3溶液中加入少量Ca(OH)2固体,C
水解程度减小,溶液的pH减小
答案 AC
11.(2014重庆理综,9,15分)中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g·
某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。
图1
图2
(1)仪器A的名称是 ,水通入A的进口为 。
(2)B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为 。
(3)除去C中过量的H2O2,然后用0.0900mol·
L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的 ;
若滴定终点时溶液的pH=8.8,则选择的指示剂为 ;
若用50mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积(填序号) (①=10mL,②=40mL,③<
10mL,④>
40mL)。
(4)滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为:
g·
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施
。
答案
(1)冷凝管或冷凝器 b
(2)SO2+H2O2
H2SO4
(3)③ 酚酞 ④
(4)0.24
(5)原因:
盐酸的挥发;
改进措施:
用不挥发的强酸如硫酸代替盐酸,或用蒸馏水代替葡萄酒进行对比实验,扣除盐酸挥发的影响
12.(2013江苏单科,18,12分)硫酸镍铵[(NH4)xNiy(SO4)m·
nH2O]可用于电镀、印刷等领域。
某同学为测定硫酸镍铵的组成,进行如下实验:
①准确称取2.3350g样品,配制成100.00mL溶液A;
②准确量取25.00mL溶液A,用0.04000mol·
L-1的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-
NiY2-+2H+),消耗EDTA标准溶液31.25mL;
③另取25.00mL溶液A,加足量的NaOH溶液并充分加热,生成NH356.00mL(标准状况)。
(1)若滴定管在使用前未用EDTA标准溶液润洗,测得的Ni2+含量将 (填“偏高”“偏低”或“不变”)。
(2)氨气常用 检验,现象是 。
(3)通过计算确定硫酸镍铵的化学式(写出计算过程)。
答案 (12分)
(1)偏高
(2)湿润的红色石蕊试纸 试纸颜色由红变蓝
(3)n(Ni2+)=0.04000mol·
L-1×
31.25mL×
10-3L·
mL-1=1.250×
10-3mol
n(N
)=
=2.500×
n(S
=
=2.500×
m(Ni2+)=59g·
mol-1×
1.250×
10-3mol=0.07375g
m(N
)=18g·
2.500×
10-3mol=0.04500g
m(S
)=96g·
10-3mol=0.2400g
n(H2O)=
10-2mol
x∶y∶m∶n=n(N
)∶n(Ni2+)∶n(S
)∶n(H2O)=2∶1∶2∶10
硫酸镍铵的化学式为(NH4)2Ni(SO4)2·
10H2O
三年模拟
A组 2016—2018年模拟·
基础题组
1.(人教选4,三-2-1,变式)①0.1mol/L盐酸 ②0.1mol/LH2SO4溶液 ③0.1mol/LNaOH溶液 ④0.1mol/LCH3COOH溶液。
相同条件下,有关上述溶液的说法正确的是( )
A.溶液中水的电离程度:
④>
①>
③>
②
B.相同体积的①和④,与NaOH溶液中和时,消耗NaOH的物质的量①>
④
C.相同体积的③和④混合后,二者恰好反应,所得溶液显中性
D.四种溶液的pH由小到大的顺序是:
②<
①<
④<
③
2.(2018宁夏大学附中月考,13)T℃时,某浓度醋酸钠溶液的pH=10,下列说法一定正确的是( )
A.溶液中由水电离出的c(OH-)=1×
10-10mol·
L-1
B.溶液中存在:
c(H+)·
c(OH-)=1×
10-14
C.溶液中存在:
c(CH3COOH)
D.溶液中存在:
c(CH3COOH)+c(CH3COO-)=c(Na+)
3.(2017河南南阳等六市联考,13)某温度下,向一定体积0.1mol·
L-1的氨水中逐滴加入等浓度的盐酸,溶液中pOH[pOH=-lgc(OH-)]与pH的变化关系如图所示。
下列说法不正确的是( )
A.M点和N点溶液中H2O的电离程度相同
B.Q点溶液中,c(N
)+c(NH3·
H2O)=c(Cl-)
C.M点溶液的导电性小于Q点溶液的导电性
D.N点溶液加水稀释,
变小
4.(2017山东省实验中学一诊,14)下列叙述正确的是( )
A.常温下,AgCl在同物质的量浓度的AgNO3和NaCl溶液中的溶解度比较,前者大
B.常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合后形成溶液a,等物质的量浓度的盐酸与NaOH溶液等体积混合后形成溶液b,水的电离程度a>
b
C.若将适量CO2通入0.1mol·
L-1Na2CO3溶液中至溶液恰好呈中性,则溶液中(不考虑溶液体积变化):
2c(C
)+c(HC
)=0.1mol·
D.常温下,已知醋酸的电离平衡常数为Ka,醋酸根离子的水解平衡常数为Kh,水的离子积为KW,则有Ka·
Kh=KW
5.(2016河南顶级名校调研,9)在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。
下列说法中正确的是( )
A.a点对应的溶液中能大量存在:
Fe3+、Na+、Cl-、S
B.b点对应的溶液中能大量存在:
N
、Ba2+、OH-、I-
C.c点对应的溶液中能大量存在:
Na+、Ba2+、Cl-、C
D.d点对应的溶液中能大量存在:
Na+、K+、S
、Cl-
6.(2018湖北部分重点中学联考,7)常温下,盐酸与氢氧化钠溶液相互滴定的滴定曲线如下图,下列叙述不正确的是( )
A.滴定过程的任何时刻都存在:
c(H+)+c(Na+)=c(OH-)+c(Cl-)
B.曲线b是氢氧化钠溶液滴定盐酸的滴定曲线
C.氢氧化钠溶液的物质的量浓度为0.1mol·
D.P点时恰好完全中和,溶液呈中性
7.[2018陕西渭南质量检测(Ⅰ),12]下列说法中不正确的是( )
A.常温下用pH=3的某酸溶液与pH=11的某碱溶液等体积混合,若混合溶液的pH=4,则反应生成的盐可能为强碱弱酸盐
B.石灰乳悬浊液中存在下列平衡:
Ca(OH)2(s)
Ca2+(aq)+2OH-(aq),恒温条件下,向石灰乳悬浊液中加入少量生石灰时,pH增大
C.常温下pH=4的NH4Cl溶液和盐酸,由水电离的氢离子的浓度的比值为106∶1
D.常温下将0.1mol·
L-1的醋酸溶液加水稀释,溶液中c(CH3COO-)/c(CH3COOH)的值增大
8.(2017江西红色七校一联,3)用标准盐酸滴定未知浓度的NaOH溶液,下列操作不会引起实验误差的是( )
A.用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定
B.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,后装入NaOH溶液进行滴定
C.用碱式滴定管取10.00mLNaOH溶液放入用蒸馏水洗净的锥形瓶中,加入少量的蒸馏水再进行滴定
D.用酚酞作指示剂滴至红色刚变无色时即停止加盐酸
9.(2017湖南衡阳联考一,13)氨分子中的一个氢原子被甲基取代后,所得甲胺(CH3NH2)的性质与氨相似,CH3NH2·
H2O也是一元弱碱,25℃时电离常数Kb=4.0×
10-5。
现用0.0500mol/L的稀硫酸滴定10mL0.1000mol/L的甲胺溶液,溶液中c(OH-)的负对数(pOH)与所加稀硫酸的体积(V)的关系如图所示。
下列说法正确的是 ( )
A.甲胺在水中的电离方程式为:
CH3NH2·
H2O
CH3N
+OH-
B.A、B、C三点溶液中,水电离出来的c(H+):
B>
C>
A
C.C点溶液中
=2.5×
10-5
D.B点溶液中存在c(CH3NH2·
H2O)>
c(CH3N
10.(2016河北衡水中学五调,7)常温下,在pH为3的FeCl3溶液、pH为11的Na2CO3溶液和pH为3的盐酸中水的电离程度分别为a1、a2、a3,则它们之间的关系是( )
A.a1<
a2<
a3B.a1=a2>
a3
C.a1>
a2>
a3D.无法判断
B组 2016—2018年模拟·
提升题组
(满分65分 时间:
30分钟)
一、选择题(每小题6分,共36分)
1.(人教选4,三-2-4,变式)下列有关体积相同、pH相同的盐酸和CH3COOH溶液的说法正确的是( )
A.盐酸中水的电离程度更小
B.与足量镁粉反应时,CH3COOH溶液中放出的H2更多
C.与NaOH溶液中和时,盐酸消耗的NaOH更多
D.同倍稀释后两溶液的pH仍相同
2.(2018江西西路片七校一联,9)下列叙述正确的是( )
A.某溶液的pH=7,则该溶液为中性溶液
B.一定温度下,向AgCl饱和溶液中加入少量NaCl固体,Ksp(AgCl)减小
C.常温下,反应X(s)+Y(l)
2Z(g)不能自发进行,则该反应的ΔH>
D.常温下,0.01mol·
L-1的NaOH溶液中由水电离的c(H+)=1.0×
10-2mol·
3.(2017湖北四地七校联盟一联,6)常温下,下列说法中不正确的是 ( )
A.pH=2与pH=1的CH3COOH溶液中c(H+)之比为1∶10
B.0.1mol·
L-1的CH3COOH溶液中,由水电离出的c(H+)为1×
10-13mol·
C.pH=12的NaOH溶液和pH=2的CH3COOH溶液等体积混合后所得溶液的pH<
7
D.pH=2的H2SO4溶液和pH=2的CH3COOH溶液等体积混合后所得溶液的pH=2
4.(2017江西九江十校第二次联考,13)25℃时,向100mL0.1mol·
L-1NH4HSO4溶液中滴加0.1mol·
L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。
下列说法错误的是( )
A.a点时溶液的pH<
B.a点到b点的过程中,溶液的导电能力减弱
C.ab段上的点(不包括a点)均满足关系式:
)+c(Na+)<
2c(S
D.b点时离子浓度大小顺序为:
c(S
c(H+)>
c(OH-)
5.(2017湖南邵阳第二次联考,12)0.1mol·
L-1NH4Al(SO4)2溶液的pH随温度变化的关系如曲线Ⅰ所示,下列说法中正确的是( )
A.0.1mol·
L-1NH4Al(SO4)2溶液中c(N
)大于等浓度的NH4HSO4溶液中c(N
B.向100mL0.1mol·
L-1NH4Al(SO4)2溶液中逐滴滴加80mL0.05mol·
L-1NaOH溶液时,溶液pH的变化如曲线Ⅱ所示
C.升高温度,NH4Al(SO4)2溶液的pH减小,是因为升温促进了NH4Al(SO4)2的电离
D.20℃时,0.1mol·
L-1NH4Al(SO4)2溶液中:
)-c(N
)-3c(Al3+)=10-3mol·
6.(2016浙江台州