高三下学期化学统练10试题Word文档格式.docx
《高三下学期化学统练10试题Word文档格式.docx》由会员分享,可在线阅读,更多相关《高三下学期化学统练10试题Word文档格式.docx(14页珍藏版)》请在冰豆网上搜索。
②
1.60
145
③
0.40
④
0.0020
580
分析实验数据所得出的结论不正确的是()w.w.w.k.s.5.u.c.o.m
A.增大c(CH3COCH3),v(Br2)增大B.实验②和③的v(Br2)相等
C.增大c(HCl),v(Br2)增大D.增大c(Br2),v(Br2)增大
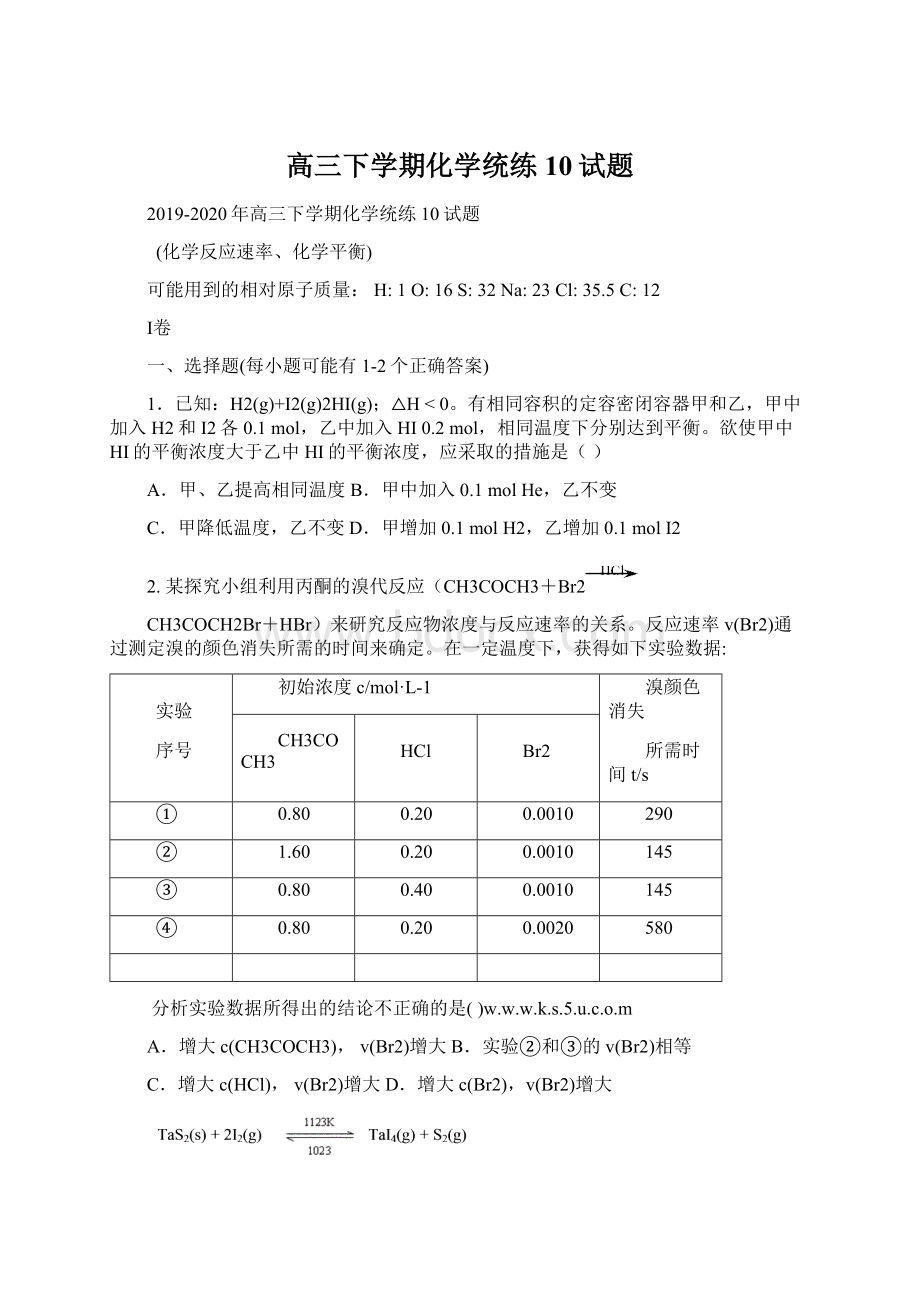
3.难挥发性二硫化钽(TaS2)可采用如下装置提纯。
将不纯的TaS2粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。
反应如下:
下列说法正确的是()
A.在不同温度区域,TaI4的量保持不变B.在提纯过程中,I2的量不断减少
C.在提纯过程中,I2的作用是将TaS2从高温区转移到低温区
D.该反应的平衡常数与TaI4和S2的浓度乘积成反比
4.取5等份NO2,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:
2NO2(g)N2O4(g),△H<0。
反应相同时间后,分别测定体系中NO2的百分量(NO2%),并作出其随反应温度(T)变化的关系图。
下列示意图中,可能与实验结果相符的是()
5.I2在KI溶液中存在下列平衡:
I2(aq)+I-(aq)I3-(aq)
某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。
A.反应I2(aq)+I-(aq)I3-(aq)的△H>
B.若温度为T1、T2,反应的平衡常数分别为K1、K2则K1>K2
C.若反应进行到状态D时,一定有v正>v逆
D.状态A与状态B相比,状态A的c(I2)大
6.下图表示反应X(g)4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化曲线:
下列有关该反应的描述正确的是()
A.第6min后,反应就终止了
B.X的平衡转化率为85%
C.若升高温度,X的平衡转化率将大于85%
D.若降低温度,v正和v逆将以同样倍数减小
7.2SO2(g)+O2(g)
2SO3(g)是制备硫酸的重要反应。
下列叙述正确的是()
A.催化剂V2O5不改变该反应的逆反应速率
B.增大反应体系的压强、反应速度一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为
8.在体积可变的密闭容器中,加入一定量X、Y,发生反应mX(g)nY(g)△H=QkJ·
mol-1。
反应达到平衡时,Y的物质的量浓度与温度、气
体体积的关系如下表所示:
气体体积
c(Y)/mol·
温度℃
1
2
3
100
1.00
0.75
0.53
200
1.20
0.09
0.63
300
1.30
0.70
A.m>nB.Q<0
C.温度不变,压强增大,Y的质量分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
9.X、Y、Z三种气体,取X和Y按1:
1的物质的量之比混合,放入密闭容器中发生如下反应:
X+2Y2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:
2,则Y的转化率最接近于()
A.33%B.40%C.50%D.65%
10.在相同温度和压强下,对反应CO2(g)+H2(g)CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,,实验起始时放入容器内各组分的物质的量见下表
物质的量
CO2
H2
CO
H2O
甲
amol
amol
0mol
乙
2amol
丙
丁
上述四种情况达到平衡后,n(CO)的大小顺序是()
A.乙=丁>
丙=甲B乙>
丁>
甲>
丙C.丁>
乙>
丙=甲D.丁>
丙>
11.等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生气体体积V的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的实验组别可能是()
A.4-3-2-1B.1-2-3-4C.3-4-2-1D.1-2-4-3
12.在密闭容器中进行如下反应:
H2(g)+I2(g)2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示.符合图示的正确判断是()
A.T1>T2,ΔH>0B.T1>T2,ΔH<0
C.T1<T2,ΔH>0D.T1<T2,ΔH<0
13.向某密闭容器中充入1molCO和2molH2O(g),发生反应:
CO+H2O(g)CO2+H2。
当反应达到平衡时,CO的体积分数为x。
若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是()
A.0.5molCO+2molH2O(g)+1molCO2+1molH2
B.1molCO+1molH2O(g)+1molCO2+1molH2
C.0.5molCO+1.5molH2O(g)+0.4molCO2+0.4molH2
D.0.5molCO+1.5molH2O(g)+0.5molCO2+0.5molH2
14.已知:
C(s)+CO2(g)2CO(g) △H>0。
该反应达到平衡后,下列条件有利于反应向正方向进行的是()
A.升高温度和减小压强B.降低温度和减小压强
C.降低温度和增大压强D.升高温度和增大压强
15.右图是恒温下某化学反应的反应速率随反应时间变化的示意图。
下列叙述与示意图不相符合的是()
A.反应达平衡时,正反应速率和逆反应速率相等
B.该反应达到平衡态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡态Ⅱ
C.该反应达到平衡态Ⅰ后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ
D.同一种反应物在平衡态Ⅰ和平衡态Ⅱ时浓度不相等
16.一定温度下可逆反应:
A(s)+2B(g)2C(g)+D(g);
△H<
0。
现将1molA和2molB加入甲容器中,将4molC和2molD加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。
A.保持温度和活塞位置不变,在甲中再加入1molA和2molB,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍
B.保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增大
C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍
D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略)
17.一定条件下,体积为10L的密闭容器中,1molX和1molY进行反应:
2X(g)+Y(g)Z(g),经60s达到平衡,生成0.3molZ。
A.以X浓度变化表示的反应速率为0.001mol/(L·
s)
B.将容器体积变为20L,Z的平衡浓度变为原来的
C.若增大压强,则物质Y的转化率减小
D.若升高温度,X的体积分数增大,则该反应的△H>0
18.在某一容积为2L的密闭容器内。
加入0.8molH2和0.6molI2,在一定的条件下发生如下反应:
H2(g)+I2(g)2HI(g);
下图表示该反应各物质浓度随时间变化。
下列判断不正确的是()
A.根据图中数据,反应开始至达到平衡时,平均速率v(HI)为0.167mol/(L·
min)
B.反应达平衡时,混合物中H2的物质的量为0.3mol
C.反应达平衡时,混合物中I2的物质的量浓度为0.1mol/L
D.反应达平衡时,混合物中HI的物质的量为1mol
19.能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质。
合成甲醇的反应为:
CO(g)+2H2(g)CH3OH(g);
△H=-ΑkJ·
mol-1(A>
0)。
在一定温度下,向一个容积不变的密闭容器中通入2.5molCO和7.5molH2,达到平衡时,CO的转化率为90%,下列说法正确的是()
A、工业生产应在较低的温度下进行
B、反应中吸收热量为2.25ΑkJ
C、平衡混合气体中碳、氢元素的质量比1:
6
D、平衡时容器内的压强为开始时的0.55倍
20.下述实验能达到预期目的的是
编号
实验内容
实验目的
A
将SO2通入酸性KMnO4溶液中
证明SO2具有氧化性
B
将Cl2通入NaBr溶液中
比较氯与溴的氧化性强弱
C
将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却降温
研究温度对化学平衡的影响
D
分别向2支试管中加入相同体积不同浓度的H2O2溶液,再向其中1支加入少量MnO2
研究催化剂对H2O2分解速率的影响
21.一定条件下,氮气和氢气合成氨气,反应达到平衡时,测得混合气体中氨气的体积分数为20.0%,与反应前的体积相比,反应后体积缩小的百分率是()
A.16.7%B.20.0%C.80.0%D.83.3%
22.T℃时,A气体与B气体反应生成C气体。
反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是()
A.在(t1+10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动
B.(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向正反应方向移动
C.T℃时,在相同容器中,若由0.3mol·
L—1A、0.1mol·
L—1B和0.4mol·
L—1C混合反应,达到平衡后,C的浓度仍为0.4mol·
L—1
D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
23.反应A2+B22AB在不同条件下,产物AB百分含量随时间变化关系如图所示,a为500℃,b为300℃时情况,c为300℃时从时间t3开始压缩容器的情况,则下列叙述正确的是()
A.A2、B2、AB均为气体,正反应放热
B.AB为气体,A2、B2中最少有一种为非气体,正反应放热
C.AB为气体,A2、B2中最少有一种为非气体,正反应吸热
D.AB为固体,A2、B2中最少有一种为非气体,正反应吸热
24.A、B两种气体可以建立如下平衡:
2AB,T1时测得平衡混和气体的平均相对分子质量为M1,T2时测得平衡混和气体平均相对分子质量为M2,如果T2>
T1,M1>
M2,则升高温度时,此平衡体系移动方向为()
A、正向B、逆向C、不移动D、无法确定
25.对于反应N2(g)+3H2(g)2NH3(g),在一密闭容器中加入一定量的N2和H2,达到平衡时气体压强为P1,迅速缩小体积使气体压强为P2,一段时间后达到新的平衡,此时气体的压强为P3,则P1、P2、P3的大小关系()
A.P2>P1<P3B.P2>P3>P1C.P2>P1>P3D.P2>P1=P3
II卷
二、非选择题(共50分)
26.甲酸甲酯水解反应方程式为:
HCOOCH3(l)+H2O(l)HCOOH(l)+CH3OH(l);
△H>
某小组通过试验研究该反应(反应过程中体积变化忽略不计)。
反应体系中各组分的起始量如下表:
组分
HCOOCH3
HCOOH
CH3OH
物质的量/mol
1.99
0.01
0.52
甲酸甲酯转化率在温度T1下随反应时间(t)的变化如下图:
(1)根据上述条件,计算不同时间范围内甲酸甲酯的平均反应速率,结果见下表:
反应时间范围/min
0~5
10~15
20~25
30~35
40~45
50~55
75~80
平均反应速率/(10-3mol·
min-1)
1.9
7.4
7.8
4.4
1.6
0.8
0.0
请计算15-20min范围内甲酸甲酯的减少量为mol,该时间段内甲酸甲酯的平均反应速率为mol·
min-1。
(2)上述反应的平衡常数表达式可表达为:
,则该反应在温度T1下的K值为。
(3)其他条件不变,仅改变温度为T2(T2大于T1),画出温度T2下甲酸甲酯转化率随反应时间变化的预期结果示意图。
27.联氨(N2H4)及其衍生物是一类重要的火箭燃料。
N2H4与N2O4反应能放出大量的热。
(1)已知:
2NO2(g)===N2O4(g)△H=-57.20kJ·
mol-1。
一定温度下,在密闭容器中上述反应达到平衡。
其他条件不变时,下列措施能提高NO2转化率的是(填字母)。
A.减小NO2的浓度B.降低温度
C.增加NO2的浓度D.升高温度
(2)25℃时,1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量。
则反应2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)的△H=kJ·
(3)
一定温度下,将1molN2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。
温度由T1继续升高到T2的过程中,气体逐渐变为无色。
若保持T2,增大压强,气体逐渐变为红棕色。
气体的物质的量n随温度T变化的关系如图所示。
①温度在T1-T2之间,反应的化学方程式是。
②温度在T2-T3之间,气体的平均相对分子质量是(保留1位小数)______________
28.超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。
科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:
2NO+2CO2CO2+N2。
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间(s)
4
5
c(NO)(mol/L)
1.00×
10-3
4.50×
10-4
2.50×
1.50×
c(CO)(mol/L)
3.60×
3.05×
2.85×
2.75×
2.70×
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)已知在上述条件下该反应能够自发进行,则反应的△H0(填写“>”、“<”、“=”)。
(2)前2s内的平均反应速率v(N2)=。
(3)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是。
A.选用更有效的催化剂B.升高反应体系的温度
C.降低反应体系的温度D.缩小容器的体积
(4)研究表明:
在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。
为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
T(℃)
NO初始浓度
(mol/L)
CO初始浓度
催化剂的比表面积(m2/g)
Ⅰ
280
1.20×
5.80×
82
Ⅱ
124
Ⅲ
350
①请在上表空格中填入剩余的实验条件数据。
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号。
29.氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
SiO2+C+N2Si3N4+CO
(1)配平上述反应的化学方程式(将化学计量数填在方框内);
(2)该反应的氧化剂是,其还原产物是;
(3)该反应的平衡常数表达式为K=;
(4)若知上述反应为放热反应,则其反应热△H0(填“大于”、“小于”或“等于”);
升高温度,其平衡常数值(填“增大”、“减小”或“不变”);
(5)若使压强增大,则上述平衡向反应方向移动(填“正”或“逆”);
(6)若已知CO生成速率为v(CO)=18mol/(L.min),则N2消耗速速率为v(N2)=mol/(L.min)。
天津市南开中学xx高三化学统练10
(化学反应速率、化学平衡)
班级姓名学号
26.
(1)mol,mol·
(2)。
27.
(1)
(2)△H=kJ·
(3)①。
②______________
28.
(1)△H0(填写“>”、“<”、“=”)。
(2)v(N2)=。
(3)。
(4)
29.:
(1)
(2),;
(3)K=;
(4)△H0
(5);
(6)mol/(L.min)。
(化学反应速率、化学平衡)参考答案
6
7
8
9
10
0+
BD
BC
10+
AC
20+
26.答案:
(1)15—20min范围内甲酸甲酯的减少量为0.045mol;
甲酸甲酯的平均反应速率为0.009mol·
min-1
(2)1/7;
(3)
27.答案:
(1)BC
(2)-1224.96
(3)①2NO22NO+O2②30.7
28.答案:
(1)<;
(2)1.875×
10-4mol/(L⋅s);
(3)C、D;
(4)①280;
10-3;
②如图:
29.
(1)3,6,2,1,6
(2)N2,Si3N4
4)小于;
减小(5)逆(6)6