理综试题1213讲解Word文档下载推荐.docx
《理综试题1213讲解Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《理综试题1213讲解Word文档下载推荐.docx(16页珍藏版)》请在冰豆网上搜索。
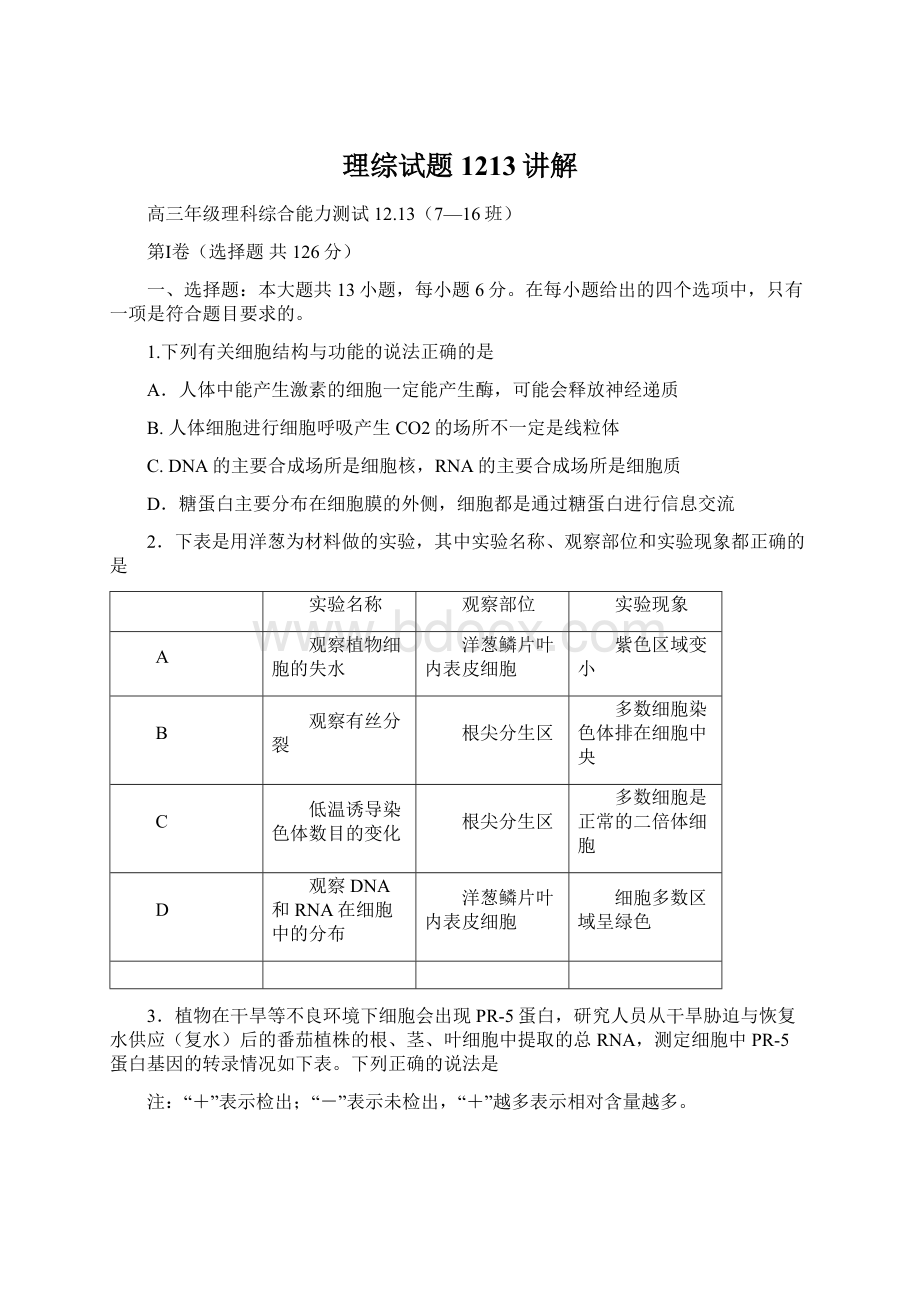
复水8h
复水24h
对照
根
-
+++
++
茎
+
叶
A.干旱导致萎蔫的植株PR-5基因被破坏
B.对照组说明在叶分化过程中PR-5基因丢失
C.干旱后复水促进了PR-5基因的表达
D.复水后根比茎叶产生了更多的PR-5基因
4.为研究提高大棚内CO2浓度对油桃光合作用的影响,测得自然种植的大棚和人工一次性施加CO2的大棚内油桃光合速率变化曲线如右图。
请据图以下正确的是
A.曲线变化规律可知人工施加CO2最佳时间为10时
B.7—8时限制光合速率的主要环境因素是光照强度
C.17时叶肉细胞内产生ATP部位有叶绿体、线粒体
D.阴影部分面积表示两种处理的一昼夜净光合速率差
5.图甲表示果蝇卵原细胞中的一对同源染色体,图乙表示该卵原细胞形成的一个卵细胞中的一条染色体,两图中的字母均表示对应位置上的基因。
下列相关叙述中正确的是
A.图甲中的同源染色体上最多只有三对等位基因
B.图乙中的卵细胞在形成过程中肯定发生了基因突变
C.图中的非等位基因在减数分裂过程中发生了自由组合
D.基因D、d的本质区别是碱基对的排列顺序不同
6.下列各项关于正常人体内发生的生理活动的叙述中,正确的是
A.效应T细胞与靶细胞结合而导致靶细胞死亡,不属于细胞凋亡
B.激素、神经递质一经靶细胞接受
并起作用后就被灭活
C.神经细胞释放的递质需要经血液运输发挥作用
D.激素具有一定的特异性,胰岛素与胰高血糖素的靶细胞种类完全不同
7.某pH=1的ZnCl2和HCl的混合溶液中含有FeCl3杂质,通过水解除去杂质,需将溶液调至pH=4,在调节溶液pH时,应选用的试剂是()
A.NaOH
B.ZnO
C.Na2CO3
D.Fe2O3
8.pH=1的两种一元酸HX与HY溶液,分别取50mL加入足量的镁粉,充分反应后,收集到H2体积分别为V1和V2。
若相同条件下V1>
V2,则下列说法正确的是()
A.HX可能是强酸
B.等浓度时HX的酸性比HY的酸性弱
C.两酸的浓度大小c(HX)<
c(HY)
D.将两种一元酸均稀释100倍,稀释后两溶液的pH均为3
9.25℃时,下列各组离子在指定溶液中一定能大量共存的是()
A.pH=1的溶液中:
Na+、K+、MnO4-、CO32-
B.c(H+)=1×
10-13mol/L的溶液中:
Mg2+、Cu2+、SO42-、NO3-
C.0.1mol/LNH4HCO3溶液中:
K+、Na+、NO3-、Cl-
D.0.1mol/LFeCl3溶液中:
Fe2+、NH4+、SCN-、SO42-
10.室温下,下列溶液中离子浓度关系正确的是()
A.Na2S溶液:
>
B.Na2C2O4溶液:
C.Na2CO3溶液:
D.CH3COONa和CaCl2混合溶液:
11.一定温度下,下列溶液的离子浓度关系式正确的是()
A.pH=5的H2S溶液中,c(H+)=c(HS-)=1×
10-5mol·
L-1
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:
c(Na+)+c(H+)=c(OH-)+
D.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):
①>
②>
③
12.在一定温度下,10mL0.40mol/LH2O2发生催化分解。
不同时刻测定生成O2的体积(已折算为标准状况)如下表。
t/min
2
4
6
8
10
V(O2)/mL
0.0
9.9
17.2
22.4
26.5
29.9
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平衡反应速率:
v(H2O2)≈3.3×
10-2mol/(L·
min)
B.6~10min的平衡反应速率:
v(H2O2)<
3.3×
C.反应到6min时,c(H2O2)=0.30mol/L
D.反应到6min时,H2O2分解了50%
13.室温下,在0.2mol·
L-1Al2(SO4)3溶液中,逐滴加入1.0mol·
L-1NaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如下图,下列有关说法正确的是()
A.a点时,溶液呈酸性的原因是Al3+水解,离子方程式为Al3++3OH-
Al(OH)3
B.a→b段,溶液的pH增大,Al3+浓度不变
C.b→c段,加入的OH-主要用于生成Al(OH)3沉淀
D.d点时,Al(OH)3沉淀开始溶解
二、选择题:
本大题共8小题,每小题6分,其中15—19题只有一项符合题目要求,14、20、21题有多项符合题目要求。
全部选对的得6分,选对但不全的得3分,有选错的得0分。
14.关于物体所受合外力的方向,下列说法正确的是
A.物体做速率逐渐增加的直线运动时,其所受合外力的方向一定与速度方向相同
B.物体做变速率曲线运动时,其所受合外力的方向一定改变
C.物体做变速率圆周运动时,其所受合外力的方向一定指向圆心
D.物体做匀速率曲线运动时,其所受合外力的方向总是与速度方向垂直
15.—质点沿x轴做直线运动,其v-t图像如图所示。
质点在t=0时位于x=5m处,开始沿x轴正向运动。
当t=8s时,质点在x轴上的位置为()
A.x=3mB.x=8m
C.x=9mD.x=14m
16.图1为伽利略研究自由落体运动实验的示意图,让小球由倾角为θ的光滑斜面滑下,然后在不同的θ角条件下进行多次实验,最后推理出自由落体运动是一种匀加速直线运动.分析该实验可知,小球
对斜面的压力、小球运动的加速度和重力加速度与各自最大值的比值y随θ变化的图像分别对应图X3�3中的( )
A.①、②和③
B.③、②和①
C.②、③和①
D.③、①和②
图1 图2
17.将一平板折成如图所示,AB部分水平且粗糙,BC部分光滑且与水平方向成θ角,板绕竖直轴OO/匀速转动,放AB板E处和放在BC板F处的物块均刚好不滑动,两物块到转动轴的距离相等,则物块与AB板的动摩擦因数为()
A.
B.
C.
D.
18.一物块静止在光滑的水平面上,现用一水平力拉物块,拉力随位移变化的关系如图所示,则物体运动的速度随位移变化的关系为()
19.“嫦娥一号”是我国首次发射的探月卫星,它在距月球表面高度为200km的圆形轨道上运行,运行周期为127分钟.已知引力常量G=6.67×
10-11N·
m2/kg2,月球半径约为1.74×
103km,利用以上数据估算月球的质量约为( )
A.8.1×
1010kg B.7.4×
1013kg
C.5.4×
1019kgD.7.4×
1022kg
20.如图所示,图线Ⅰ为某灯泡两端的电压随电流变化的曲线,图线Ⅱ是某电池路端电压随电流变化的曲线,现将图线Ⅰ对应的灯泡直接接在图线Ⅱ对应的电池两端,过较长一段时间后,电池的电动势基本不变,电池的内阻明显变大,则()
A.灯泡的电阻肯定增大
B.电源的输出功率肯定增大
C.电源的总功率肯定减小
D.电源的效率肯定减小
21.如图所示,在x轴上相距为L的两点固定两个等量异种点电荷+Q、-Q,虚线是以+Q所在点为圆心、为半径的圆,a、b、c、d是圆上的四个点,其中a、c两点在x轴上,b、d两点关于x轴对称.下列判断正确的是( )
A.b、d两点处的电势相同
B.四个点中c点处的电势最低
C.b、d两点处的电场强度相同
D.将一试探电荷+q沿圆周由a点移至c点,+q的电势能减小
第Ⅱ卷
三、非选择题:
包括必考题和选考题两部分。
第22题~第32题为必考题,每个试题考生都必须作答。
第33题~第38题为选考题,考生根据要求作答。
(一)必考题(11题,共129分)
22.(8分)测量小物块Q与平板P之间动摩擦因数的实验装置如图所示.AB是半径足够大的、光滑的四分之一圆弧轨道,与水平固定放置的P板的上表面BC在B点相切,C点在水平地面的垂直投影为C′.重力加速度大小为g,实验步骤如下:
①用天平称出物块Q的质量m;
②测量出轨道AB的半径R、BC的长度L和CC′的长度h;
③将物块Q在A点从静止释放,在物块Q落地处标记其落地点D;
④重复步骤③,共做10次;
⑤将10个落地点用一个尽量小的圆围住,用米尺测量圆心到C′的距离s.
(1)
用实验中的测量量表示:
(ⅰ)物块Q到达B点时的动能EkB=________;
(ⅱ)物块Q到达C点时的动能EkC=________;
(ⅲ)在物块Q从B运动到C的过程中,物块Q克服摩擦力做的功Wf=________;
(ⅳ)物块Q与平板P之间的动摩擦因数μ=________________________.
23.(10分)虚线方框内是由电阻、电源组成的线性网络电路,若将方框内的电路等效成电动势为
、内阻为
的电源。
为了研究它的输出特性,将电流表、电阻箱按图甲所示的方式连接在它的输出端A、B之间。
电键S闭合后,实验中记录的几组电流表示数I、电阻箱阻值R,并在坐标纸中将其描绘出来。
(1)根据描绘出的坐标点在图乙所示的坐标纸上画出R-
图线。
(2)从图线上求出等效电源的电动势
=__________V。
(3)若改用一个电压表和一个电阻箱测量等效电源的电动势和内阻,请在丙图中将电路图补充完整。
(4)若采用第三问设计方案,根据实验数据绘出
图象是一条直线,若直线的斜率为k,在
坐标轴上的截距为b,则等效电源的电动势
=____________,内电阻
=__________。
(用k、b表示)
24.质量为m=4kg的小物块静止于水平地面上的A点,现用F=10N的水平恒力拉动物块一段时间后撤去,物块继续滑动一段位移停在B点,A、B两点相距x=20m,物块与地面间的动摩擦因数μ=0.2,g取10m/s2,求:
(1)物块在力F作用过程发生位移x1的大小;
(2)撤去力F后物块继续滑动的时间t.
25.(16分)山谷中有三块石头和一根不可伸长的轻质青藤,其示意图如下.图中A、B、C、D均为石头的边缘点,O为青藤的固定点,h1=1.8m,h2=4.0m,x1=4.8m,x2=8.0m.开始时,质量分别为M=10kg和m=2kg的大、小两只滇金丝猴分别位于左边和中间的石头上,当大猴发现小猴将受到伤害时,迅速从左边石头的A点水平跳至中间石头.大猴抱起小猴跑到C点,抓住青藤下端,荡到右边石头上的D点,此时速度恰好为零.运动过程中猴子均可看成质点,空气阻力不计,重力加速度g=10m/s2.求:
(1)大猴从A点水平跳离时速度的最小值;
(2)猴子抓住青藤荡起时的速度大小;
(3)猴子荡起时,青藤对猴子的拉力大小.
26.(12分)
(一)、室温下,有以下四种溶液:
①pH=2的HCl溶液;
②pH=2的NH4Cl溶液;
③pH=12的NaOH;
④pH=12的CH3COONa溶液.请回答下列问题:
(1)①④溶液中由水电离出来的c(H+)的比是:
(2)将②③溶液等体积混合后,溶液的pH7(填“>
”“<
”或“=”)
(3)将①④溶液均稀释至原来的10倍后,它们的pH之和14(填“>
”或“=”)
(4)向300mL溶液③中通入44.8mLCO2(标准状况)气体,充分反应后,溶液中粒子浓度关系正确的是()
A.c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-)
B.2c(Na+)=3c(HCO3-)+c(CO32-)+c(H2CO3)
C.c(Na+)>
c(CO32-)>
c(HCO3-)>
c(OH-)>
c(H+)
D.c(Na+)>
c(H+)
(二)、已知在400℃时,N2(g)+3H2(g)
2NH3(g)△H<
0的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应V(N2)正V(N2)逆(填:
>、<、=、不能确定)。
欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积百分数增加,可采取的正确措施是(填序号)
A.缩小体积增大压强B.升高温度C.加催化剂D.使氨气液化移走
27.(18分)在氧化还原反应中,氧化过程和还原过程是同时发生的两个半反应:
Cu2O-2e-+2H+=2Cu2++H2O是一个半反应式,下列五种物质FeSO4、Fe2(SO4)3、CuSO4、Na2CO3、KI中的一种物质A能使上述半反应顺利发生。
(1)写出并配平该反应的离子方程式:
_______________________________
(2)向
(1)中反应后的溶液里加入酸性高锰酸钾溶液,还原产物Mn2+(无色),反应的离子方程式:
判断Cu2+、MnO4—、Fe3+的氧化性由强到弱的顺序是(用离子符号表示)___________。
(3)某同学用上述原理测定一种含Cu2O的矿石中的质量分数。
称量5.0g矿石溶于足量A和硫酸的混合溶液中,充分反应后,用酸性高锰酸钾溶液滴定,消耗0.1000mol·
L-1的高锰酸钾溶液的体积为100.00mL。
①滴定终点的颜色____________________。
②该同学测得矿石样品中Cu2O的质量分数为_________________________
③下列情况使测定结果一定偏高的是_________________________
A、开始和终点都是仰视读数B、没有用待测液润洗锥形瓶
C、称量时,砝码与样品放反了D、样品中含有较强还原性杂质
E、高锰酸钾溶液中含有NO3—F、用酸性高锰酸钾溶液润洗滴定管
28.(10分)化学实验室通常用粗锌和稀硫酸反应制氢气,因此在制氢废液中含有大量的硫酸锌。
同时,由于粗锌中还含有铁等杂质,使得溶液中混有一定量的硫酸亚铁,为了充分利用制氢废液,常用其制备皓矾(ZnSO4·
7H2O)。
某校化学兴趣小组的同学以制氢气的废液为原料来制取皓矾。
制备皓矾的实验流程如下图所示。
已知:
开始生成氢氧化物沉淀到沉淀完全的pH范围分别为Fe(OH)3:
2.7~3.7;
Fe(OH)2:
7.6~9.6;
Zn(OH)2:
5.7~8.0,试回答下列问题:
(1)加入的试剂①,供选择使用的有:
氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,最好选用________,其理由是.
(2)加入的试剂②:
供选择使用的有:
a.Zn粉、b.ZnO、c.Zn(OH)2、d.ZnCO3、e.ZnSO4等,可选用__________。
(3)从晶体1→晶体2,该过程的名称是__________。
(4)在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是
。
29.(7分)以下是研究单细胞真核生物——雨生红球藻得到的曲线图,请分析回答:
(1)雨生红球藻产生氧气的场所是(填细胞器名称),只有当光合作用强度于细胞呼吸强度时,雨生红球藻才释放出氧气。
(2)由曲线图可知,雨生红球藻光合作用强度受的影响;
在以上实验条件下,光照强度为6klx、温度为℃时,最适合雨生红球藻生长。
(3)据曲线图计算,在光照强度为4klx、温度为30℃时,雨生红球藻呼吸速率是nmolO2·
cell-1·
h-1(计算结果保留整数位)。
(4)雨生红球藻细胞呼吸强度与光照强度(有关、基本无关、无法确定),理由是。
30.(8分)开两性花的二倍体陆地棉易得黄萎病,研究人员已从海岛棉分离出抗黄萎病基因(StVe,简称基因S),发现整合到陆地棉的2号染色体和线粒体上的基因S能表达出等效的抗性,但线粒体上的基因S表达的抗性会逐代减弱。
请回答下列问题:
(1)符合长期种植要求的种子(幼苗)是下列图示中的。
(2)为了快速地获得更多的符合生产要求的种子,将上述6种幼苗全部种植,逐步进行如下操作:
①将所有具有抗性的植株自交得到自交系一代,同时还将这些具有抗性的植株作为父本(其精子内的线粒体不会进入卵细胞)与表现型为的植株杂交得到杂交系一代,将杂交系一代种子全部种植,检测其抗性。
若同一株系的植株全部表现为,则其对应的自交系一代就是符合要求的种子。
②让所有有抗性的杂交系一代植株自交,得到自交系二代种子,这些种子类型是(种子类型用上图中的序号表示),对应的比例是。
(3)某种群陆地棉,基因型为AA、Aa的植株分别为90%、9%,它们能够正常繁殖,但基因型为aa植株不能产生卵细胞,能产生花粉。
问该种群自由交配一代后,具有正常繁殖能力的植株占。
31.(14分)小麦品种是纯合体,生产上用种子繁殖。
控制小麦高杆的基因A和控制小麦矮杆的基因a是一对等位基因。
控制小麦抗病的基因B和控制小麦感病的基因b是一对等位基因,两对基因位于两对同源染色体上。
(1)若要通过杂交育种的方法选育矮杆(aa)抗病(BB)的小麦新品种,所选择亲本的基因型是_____________________;
确定表现型为矮杆抗病小麦是否为理想类型的最适台的方法
是_____________________。
(2)某同学设计了培育小麦矮杆抗病新品种的另一种育种方法,过程如右图所示。
其中的③表示_________________技术,乙植株中矮杆抗病个体占__________________。
(3)为探究DNA分子的半保留复制特点。
某同学首先采用适当的方法使小麦根尖细胞染色体的DNA全部被3H胸腺嘧啶脱氧核苷标记,然后转移到不含3H胸腺嘧啶脱氧核苷的培养基培养,观察细胞中每条染色体的染色单体的标记情况。
①对根尖细胞的有丝分裂进行观察时,最佳选择是有丝分裂_____________期的细胞。
②转移培养基培养后,细胞第一次有丝分裂的标记特点是每条染色体的_________条染色单体被标记,细胞第二次有丝分裂的标记特点是每条染色体的__________条染色单体被标记。
32.(10分)下图甲表示反射弧中三个神经元及其联系,其中—O—(表示从树突到胞体,
再到轴突及末梢(即一个完整的神经元模式);
图乙表示突触的亚显微结构模式图。
联系图解回答下列问题:
(1)图甲中,若①代表小腿上的感受器,则⑤(代表神经末梢及其支配的腿上肌肉)称
为_________,③称为____________________。
(2)图甲中刺激d点,则除d点外,图中发生兴奋的点还有_________(用字母表示)。
(3)图乙中二氧化碳浓度最高处在[]________________中,该结构的作用是为神经兴奋的传导提供___________。
(4)手术过程中,使用某种局部麻醉剂,能使乙图中[⑨]______________中释放的___________不能作用于[]______________,从而暂时失去兴奋传导功能。
(5)兴奋通过图乙的传递过程中,信号的变化情况是__________________________,传递方向的特点是___________________。
(二)选考题:
共45分。
请考生从给出的3道物理题,3道化学题、2道生物题中每科任选一题作答,并用2B铅笔在答题卡上把所选题目的题号涂黑。
注意所做题目的题号必须与所涂题目的题号一致,在答题卡上选答区域指定位置答题。
如果多做,则每学科按所做的第一题计分。
35.【物理——选修3-5】
(15分)
如图所示,竖直平面内的四分之一圆弧轨道下端与水平桌面相切,小滑块A和B分别静止在圆弧轨道的最高点和最低点.现将A无初速释放,A与B碰撞后结合为一个整体,并沿桌面滑动.已知圆弧轨道光滑,半径R=0.2m;
A和B的质量相等;
A和B整体与桌面之间的动摩擦因数μ=0.2.重力加速度g取10m/s2.求:
(1)碰撞前瞬间A的速率v;
(2)碰撞后瞬间A和B整体的速率v′;
(3)A和B整体在桌面上滑动的距离l.
37.(18分)明矾石经处理后得到明矾【KAl(SO4)2·
12H2O】。
从明矾制备Al、K2SO4和H2SO4的工艺过程如下所示:
焙烧明矾的化学方程式为:
4KAl(SO4)2·
12H2O+3S=2K2SO4+2Al2O3+9SO2+48H2O
(1)在焙烧明矾的反应中,还原剂是
(2)从水浸后的滤液中得到K2SO4晶体的方法是
(3)A12O3在一定条件下可制得AIN,其晶体结构如图所示,该晶体中Al的配位数是
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是
(5)焙烧产生的SO2可用于制硫酸。
已知25℃、101kPa时:
2SO2(g)+O2(g)
2SO3(g)
△H1=一197kJ/mol;
2H2O(g)=2H2O
(1)
△H2=一44kJ/mol;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)
△H3=一545kJ/mol。
①
则SO3(g)与H2O(l)反应的热化学方程式是
②焙烧948t明矾(M=474g/mol),若SO2的利用率为96%,可生产质量分数为98%的硫酸
t。
40.[生物—现代生物科技专题](15分)
科学家从129品系小