届二轮复习 以物质的量为中心的计算 专题卷全国通用Word文档下载推荐.docx
《届二轮复习 以物质的量为中心的计算 专题卷全国通用Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《届二轮复习 以物质的量为中心的计算 专题卷全国通用Word文档下载推荐.docx(21页珍藏版)》请在冰豆网上搜索。
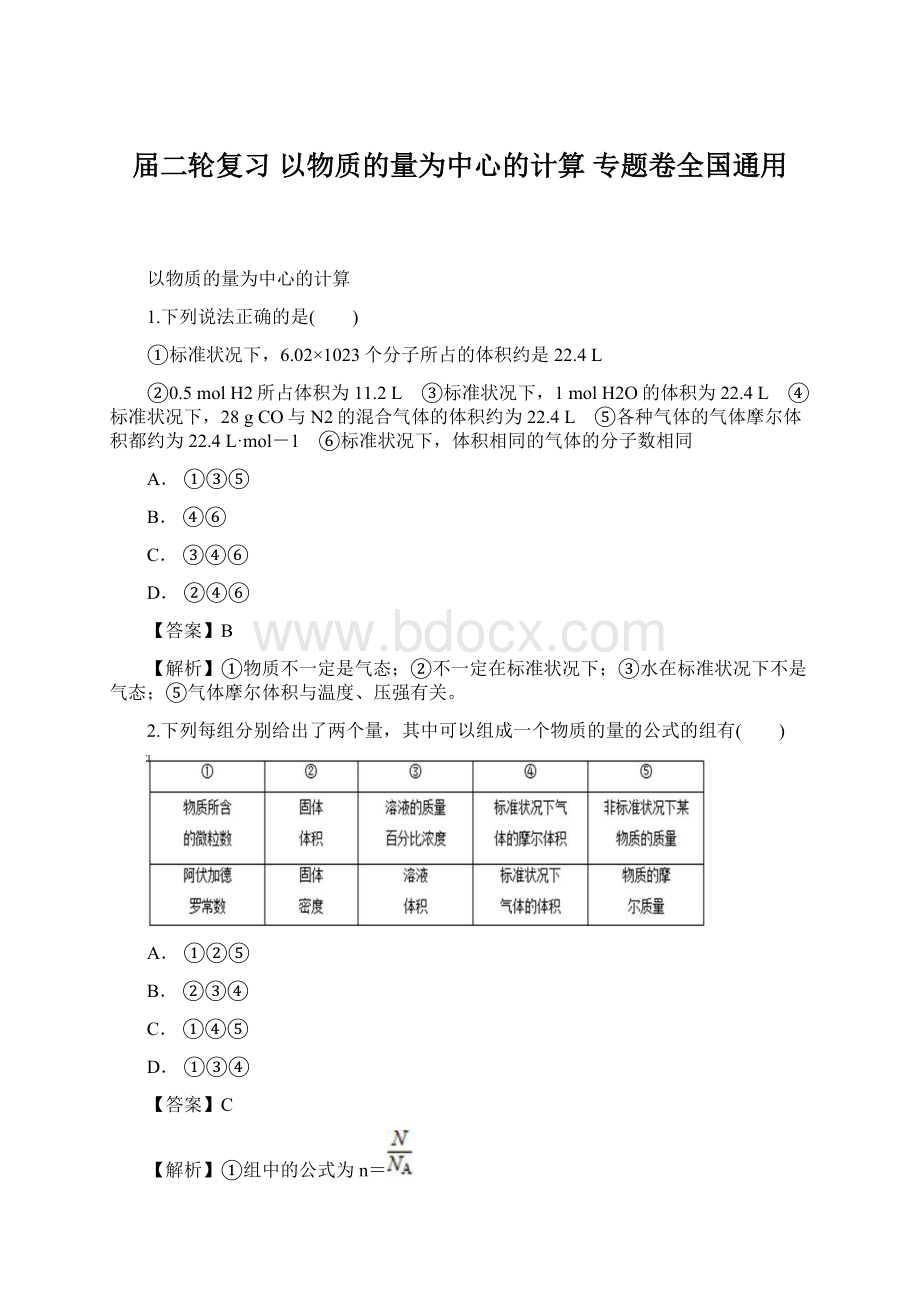
②mg该硫原子的物质的量为
mol ③该硫原子的摩尔质量是aNAg ④ag该硫原子所含的电子数为16NA
A.①③
B.②④
C.①②
D.②③
【解析】①该硫原子的相对原子质量为该原子的质量除以12C原子质量的
,即
,正确;
②mg硫原子的个数为
,其物质的量为
mol,正确;
③该原子的摩尔质量是aNAg/mol,错误;
④一个硫原子所含电子数为16,而16NA为1mol硫原子所含电子数,错误。
5.下列叙述正确的是( )
A.常温常压下,4.6gNO2气体约含有1.81×
1023个原子
B.在标准状况下,80gSO3所占的体积约为22.4L
C.常温下,0.1mol/L醋酸的pH约为1
D.标准状况下,22.4L氯气与足量氢氧化钠溶液反应,转移的电子数为2NA
【答案】A
【解析】标准状况下SO3不是气体,故B错误;
CH3COOH是弱电解质,部分电离,常温下,0.1mol/L醋酸的pH大于1,故C错误;
标准状况下,22.4L氯气与足量氢氧化钠溶液反应,转移的电子数为NA,故D错误。
6.下列说法中,正确的是( )
A.CO2的摩尔质量为44g
B.1molN2的质量是14g
C.标准状况下,1molCO2所占的体积约是22.4L
D.将40gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为1mol/L
【解析】1mol二氧化碳的质量是44g,二氧化碳的摩尔质量是44g/mol,A错误;
1molN2的质量是28g,B错误;
标准状况下,1molCO2所占的体积约是22.4L,C正确;
溶液的体积不是1L,D错误。
7.下列说法中正确的是( )
A.22.4L•mol-1就是气体摩尔体积
B.1molH2的质量只有在标准状况下才约为2g
C.标准状况下,18g水的体积为22.4L
D.1molH2和O2的混合气体在标准状况下的体积约为22.4L
【答案】D
【解析】温度和压强影响气体的体积,标况下气体摩尔体积为22.4L/mol,不是标准状况下,气体摩尔体积不一定为22.4L/mol,A错误;
摩尔质量公式与条件无关,1molH2的质量在任何条件下都约为2g,B错误;
标准状况下,水是液体,不能用气体摩尔体积公式计算,C错误;
标准状况下,V=nVm=1mol×
22.4L/mol=22.4L,D正确。
8.下列说法正确的是( )
A.单位物质的量的气体所占的体积就是气体摩尔体积
B.摩尔是物质的量的单位
C.阿伏加德罗常数就是6.02×
1023
D.CO2的摩尔质量为44g
【解析】在温度压强一定条件下,单位物质的量的气体所占的体积就是气体摩尔体积,A错误;
物质的量是七个国际物理量之一,其单位是摩尔,符号为mol,B正确;
阿伏加德罗常数近似为6.02×
1023mol-1,C错误;
摩尔质量以g/mol为单位,数值上等于其相对分子质量,故CO2的摩尔质量为44g/mol,D错误。
9.下列溶液中的Cl-物质的量与100ml1mol•L-1AlCl3溶液中Cl-相等的是( )
A.150ml1mol•L-1NaCl溶液
B.100ml3mol•L-1KClO3溶液
C.75ml2mol•L-1MgCl2溶液
D.50ml1mol•L-1FeCl3溶液
【解析】先计算溶液中氯离子的物质的量浓度=盐的浓度×
化学式中氯离子个数,再根据n=cv分别求出物质的量。
10.下列所得溶液的物质的量浓度等于0.1mo/L的是( )
A.将0.1mol氨气充分溶解在1L水中
B.将10g质量分数为98%的硫酸与990g水混合
C.将8g三氧化硫溶于水并配成1L溶液
D.将0.1mol氧化钾溶于水并配成1L溶液
【答案】
【解析】将0.1mol氨气充分溶解在1L水中,所得溶液的体积不是1L,溶液的浓度不是0.1mol/L,A错误;
将10g质量分数为98%的硫酸与990g水混合,所得溶液中含有硫酸9.8g,物质的量为0.1mol,溶液质量为1000g,但是硫酸溶液的密度大于1g/mL,溶液的体积小于1L,所以溶液的物质的量浓度大于0.1mol/L,B错误;
8g三氧化硫的物质的量为0.1mol,0.1mol三氧化硫与水反应生成0.1mol硫酸,所得溶液浓度为0.1mol/L,C正确;
0.1mol氧化钾与水反应生成了0.2mol氢氧化钾,配成1L溶液后的浓度为0.2mol/L,D错误。
11.下列说法中正确的是( )
A.1mol任何物质都含有6.02×
B.1molNe中含有约6.02×
1024个电子
C.1mol水中含2mol氢和1mol氧
D.摩尔是化学上常用的一个物理量
【解析】有些物质是由离子或原子构成的,故A错;
使用摩尔表示物质的量时,应用化学式表明粒子的种类,故C错;
摩尔是物质的量的单位,而不是物理量,故D错。
12.工业上将氨气和空气的混合气体通过铂铑合金网发生氨氧化反应,若有标准状况下VL氨气完全反应,并转移n个电子,则阿伏加德罗常数(NA)可表示为( )
A.
B.
C.
D.
【解析】根据反应的化学方程式4NH3+5O2
4NO+6H2O,当有标准状况下VLNH3完全反应时,NH3的物质的量为
mol,转移电子数为
mol,已知在此反应中转移电子数为n,则n=
×
NA,所以,NA=
,故选D。
13.设阿伏加德罗常数为NA,标准状况下某O2和N2的混合气体mg含有b个分子,则ng该混合气体在相同状况下所占的体积(L)应是( )
【解析】mg含有b个分子,则ng该混合气体含有的分子数是
,则混合气体的物质的量是
,则混合气体的体积是
,故A正确。
14.标准状况下,mgA气体与ngB气体分子数相等,下列说法不正确的是( )
A.标准状况下,同体积的气体A和气体B的质量比为m∶n
B.25℃时,1kg气体A与1kg气体B的分子数之比为n∶m
C.同温同压下,气体A与气体B的密度之比为m∶n
D.标准状况下,等质量的A与B的体积比为m∶n
【解析】标准状况下,mgA气体与ngB气体分子数相等,根据阿伏加德罗定律,则A、B的物质的量相等,由
=
,标准状况下,同体积的A、B的物质的量相等,质量比等于摩尔质量之比,为m∶n,A正确;
等质量的A、B的物质的量之比等于摩尔质量的反比,为n∶m,B正确;
同温同压下,气体密度之比等于摩尔质量之比,为m∶n,C正确;
标准状况下,等质量的A、B的体积比等于物质的量之比等于摩尔质量的反比,为n∶m,D错误。
15.氢气的摩尔质量为Mg/mol,密度是ρg/L,阿伏加德罗常数为NA,则下列表达正确的是( )
A.单位体积中所含氢气分子数目为
B.单位质量中所含氢气分子数目为ρNA
C.单个氢气分子的质量为
g
D.单个氢气分子占有的体积为
L
【解析】单位体积中所含氢气分子数目为
,A项错误;
单位质量中所含氢气分子数目为
,B项错误;
单个氢气分子的质量为
g,C项正确;
在标准状况下,单个氢气分子占有的体积才为
L,D项错误。
16.将等物质的量的金属Na、Mg、Al分别与100mL2mol/L盐酸溶液反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如图,则下列说法错误的是( )
A.x=2.24
B.钠的物质的量为0.2mol
C.反应时,Na、Mg、Al均过量
D.曲线b为Mg与盐酸反应的图象
【解析】由图象可以看出,生成的气体体积相等,则盐酸完全反应,x=2.24,A项正确;
根据生成的氢气为2.24L,可知钠失去0.2mol电子,钠的物质的量为0.2mol,B项正确;
反应时如果钠过量,则钠会与水反应,生成的气体多于2.24L,故C项错误;
根据反应速率可知a、b、c依次是Na、Mg、Al与盐酸反应的图象,D项正确。
17.某氯原子的质量是ag,12C原子的质量是bg,用NA表示阿伏加德罗常数,下列说法中正确的是( )
①氯元素的相对原子质量一定是
②mg该氯原子的物质的量一定是
③该氯原子的摩尔质量是aNAg/mol
④ag该氯原子所含质子数是17mol
A.①③
B.②④
C.①④
【解析】①氯元素的相对原子质量是根据各种氯原子在自然界所占的原子百分含量算出来的平均值,不是某种氯原子的相对原子质量;
②mg该氯原子的原子个数为
,物质的量为
mol;
③NA个该氯原子的质量为aNAg,即该氯原子的摩尔质量是aNAg/mol;
④ag该氯原子的物质的量为
mol,所含质子的物质的量为
mol,质子数为17。
18.下列说法正确的是( )
A.等质量的乙烯和丙烯中,所含碳原子数之比为2∶3
B.等体积、等浓度的NH4Cl溶液和稀氨水中,所含NH
的数目相等
C.等物质的量的Cl2分别与足量的Fe和Cu反应,转移的电子数相等
D.等物质的量的过氧化钡(BaO2)和Ba(OH)2固体中,阴阳离子个数之比为2∶1
【解析】乙烯、丙烯最简式相同,质量相等时,其碳原子数之比为1∶1,A项错误。
NH4Cl是强电解质而NH3·
H2O是弱电解质,等体积、等浓度的NH4Cl溶液和稀氨水中,前者所含NH
的数目多,B项错误。
过氧化钡(BaO2)中,阴阳离子个数之比为1∶1,Ba(OH)2中,阴阳离子个数之比为2∶1,故D项错误。
19.下列有关说法正确的是 ( )
A.臭氧的摩尔质量是48g
B.同温同压条件下,等质量的氧气和臭氧体积比为2∶3
C.16g臭氧中含有6.02×
D.1.00mol臭氧中含有电子总数为18×
6.02×
【解析】摩尔质量的单位应是g·
mol-1,A项错误;
同温同压条件下,等质量的氧气和臭氧体积比为3∶2,B项错误;
1.00mol臭氧中含有电子总数为24×
1023,D项错误。
20.下列说法正确的是 ( )
①标准状况下,6.02×
②0.5molH2所占体积为11.2L
③标准状况下,1molH2O的体积为22.4L
④标准状况下,28gCO与N2的混合气体的体积约为22.4L
⑤各种气体的气体摩尔体积都约为22.4L·
mol-1
⑥标准状况下,体积相同的气体的分子数相同
【解析】①物质不一定是气态;
②不一定在标准状况下;
③水在标准状况下不是气态;
21.标准状况下,1L的密闭容器中恰好可盛放n个N2分子和m个H2分子组成的混合气体,则阿伏加德罗常数可近似表示为 ( )
A.22.4(m+n)
B.22.4×
1023(m+n)
C.m+n
D.22.4(m+n)/(6.02×
1023)
【解析】由阿伏加德罗常数的定义可知,它指的是1mol微粒中所含有的微粒数的多少,由标准状况下22.4L气体所含有的分子数为1mol,1L气体中所含有的气体分子数为(m+n),可知阿伏加德罗常数可近似表示为22.4(m+n)。
22.某硫原子的质量是ag,12C原子的质量是bg,若NA只表示阿伏加德罗常数的数值,则下列说法中正确的是 ( )
①该硫原子的相对原子质量为aNA
②mg该硫原子的物质的量为m/amol
③该硫原子的摩尔质量是aNAg·
④ag该硫原子所含有的电子数为16
A.①②③
B.①②④
C.②③④
【解析】1mol硫原子的质量为aNAg,则硫原子的相对原子质量为aNA,该硫原子的摩尔质量为aNAg·
mol-1,①③正确;
mg该硫原子的物质的量为
mol,②错;
ag该硫原子即一个硫原子,所含电子数为16,④正确;
综上所述①③④正确。
23.下列关于物质的量、摩尔质量的叙述正确的是( )
A.0.012kg12C中含有约6.02×
1023个碳原子
B.1molH2O中含有2mol氢和1mol氧
C.物质的量就是1mol物质的质量
D.2mol水的摩尔质量是1mol水的摩尔质量的2倍
【解析】B项,应表达为1molH2O中含有2molH和1molO;
C项,物质的量表示一定数目粒子的集合体,而不是表示物质的质量;
D项,水的摩尔质量是固定不变的,是18g·
mol-1。
24.
Hf是我国科学家首次合成的一种过渡金属的新核素,该核素在高科技领域有着重要的用途。
若一个该核素的质量为ag,12C核素的质量为bg,NA是阿伏伽德罗常数,下列说法中错误的是( )
A.NA=
B.Wg
Hf的物质的量为
mol
C.
Hf的摩尔质量为
g/mol
D.等物质的量的
Hf、12C的质量比为b∶a
【解析】由相对原子质量的定义知,M(Hf)=
g/mol,又1molHf含有NA个原子,故M(Hf)=aNA,由此可知A、B、C项正确。
25.某硫原子的质量是ag,12C原子的质量是bg,若NA只表示阿伏加德罗常数的数值,则下列说法中正确的是( )
A.①③
C.①②
【解析】①该硫原子的相对原子质量为该原子的质量除以
12C原子质量的
③该原子的摩尔质量是aNAg/mol,不正确;
④一个硫原子所含电子数为16,则16NA为1mol硫原子所含电子数,不正确。
26.在反应x+2y=R+2M中,已知R和M的摩尔质量之比为22:
9,当1.6gx与y完全反应后,生成4.4gR,则在此反应中y和M的质量比为( )
A.16:
9
B.23:
C.32:
D.46:
【解析】题目给出了R和M的摩尔质量之比为22:
9,反应中生成了2molM,所以R和M的质量比应为22:
18,生成4.4gR同时生成3.6gM,再由质量守恒定律求得参加反应的y的质量为6.4g,进而求得y和M的质量之比为6.4:
3.6=16:
9。
27.设NA为阿伏加德罗常数的值。
下列说法正确的是()
A.1L1mol·
L-1的NaClO溶液中含有ClO-的数目为NA
B.78g苯含有C=C双键的数目为3NA
C.常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA
D.标准状况下,6.72LNO2与水充分反应转移的电子数目为0.1NA
【解析】A错误,ClO-水解,ClO-数目小于NA。
B错误,苯中没有真正的双键,而是介于单键和双键之间的一种独特的键。
C正确,相对分子质量皆为28的CO和N2混合气体,因分子中原子数目均为二个,则原子数为NA。
D错误,6.72L即0.3molNO2溶于水,转移的电子数目为0.2NA。
28.NA为阿伏伽德罗常数,下列叙述错误的是()
A.18gH2O中含的质子数为10NA
B.12g金刚石含有的共价键数为4NA
C.46gNO2和N2O4混合气体中含有原子总数为3NA
D.1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
【解析】金刚石中C:
C-C=1:
2,12g金刚石含有的共价键数为2NA,选择B。
29.设NA表示阿伏伽德罗常数。
(1)已知一个NO、NO2分子的质量分别是ag、bg。
则一个氧原子的质量是________,氧原子的摩尔质量是(用含a、b数字的式子表示)________,10gNO2物质的量为(用含b的式子表示)________。
(2)已知H2+Cl2
2HCl,在某密闭容器中使NA个Cl2与2molH2充分反应后,容器中气体分子数目为________NA,此时气体总质量为________。
(3)含有NA个OH-的Ca(OH)2的质量是________,n(Ca2+)=________。
(1)(b-a)g (b-a)NA
(2)3 75g (3)37g 0.5mol
【解析】
(1)NO、NO2分子组成相差1个氧原子,故1个氧原子的质量为(b-a)g,1molO的质量为(b-a)NAg。
NO2的摩尔质量为bNAg/mol,10gNO2物质的量为
mol。
(2)反应前气体分子数目共为3NA,由反应知,反应前后气体分子数目不变,故反应后气体分子数目仍为3NA,由质量守恒原理知,容器中气体总质量75g。
(3)1molCa(OH)2含2NA个OH-,故含有NA个OH-的Ca(OH)2物质的量为0.5mol,质量为37g。
30.卫生部发出公告,自2011年5月1日起,禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。
过氧化钙(CaO2)是一种安全无毒物质,带有结晶水,通常还含有CaO。
(1)称取5.42g过氧化钙样品,灼热时发生如下反应:
2[CaO2·
xH2O]
2CaO+O2↑+2xH2O,得到O2在标准状态下体积为672mL,该样品中CaO2的物质的量为________。
(2)另取同一样品5.42g,溶于适量稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO37.0g。
①样品中CaO的质量为________。
②样品中CaO2·
xH2O的x值为________。
(1)0.06mol
(2)①0.56g ②0.5
(1)n(O2)=
=0.03mol
由2(CaO2·
xH2O)~O2
则n(CaO2)=2n(O2)=0.06mol
(2)①n(CaCO3)=
=0.07mol
由Ca2+守恒知含n(CaO)=0.07mol-0.06mol=0.01mol
m(CaO)=0.56g
②5.42g样品中含水=5.42g-0.06mol×
72g/mol-0.01mol×
56g·
mol-1=0.54g
n(H2O)=
故n(CaO2)∶n(H2O)=0.06mol∶0.03mol=1∶0.5
即x=0.5
31.在标准状况下,①6.72LCH4气体②3.01×
1023个HCl气体分子③13.6gH2S气体④0.2molNH3,按下列要求对这四种气体的关系从大到小进行排列(用上述数字序号表示):
(1)标准状况下四种气体的体积是__________________
________________________________________________________________________。
(2)四种气体的质量为______________________________________。
(1)②>
③>
①>
④
(2)②>
④
【解析】四种气体的物质的量分别为0.3mol、0.5mol、0.4mol、0.2mol。
(1)标准状况下气体的体积与物质的量成正比,所以有
V(HCl)>
V(H2S)>
V(CH4)>
V(NH3)。
(2)四种气体的质量分别为:
m(CH4)=0.3mol×
16g/mol=4.8g
m(HCl)=0.5mol×
36.5g/mol=18.25g
m(H2S)=13.6g
m(NH3)=0.2mol×
17g/mol=3.4g。
32.
(1)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为 。
(2)在25℃、101kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为 。
(3)两个相同容积的密闭容器X、Y,在25℃下,X中充入agA气体,Y中充入agCH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为 。
(4)相同条件下,体积比为1∶2和质量比为1∶2的H2和O2的混合气体,其平均相对分子质量分别是 和 。
(1)64
(2)30g·
(3)44g·
mol-1 (4)22 5.33
(1)M=1.92g/0.03mol=64g·
(2)T、p相同时,体积之比等于物质的量之比,15∶8=
∶
M(A)=
30g·
(3)T、V相同时,压强之比等于物质的量之比,
4∶11=
M(A)=44g·
(4)体积比为1∶2的H2和O2混合,
=
=22
质量比为1∶2的H2和O2混合,
≈5.33。
33.
(1)0.7molH2O的质量为 __________________________________,
其中含有 个水分子,氢原子的物质的量为