考点5化学反应速率和化学平衡Word文档下载推荐.docx
《考点5化学反应速率和化学平衡Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《考点5化学反应速率和化学平衡Word文档下载推荐.docx(9页珍藏版)》请在冰豆网上搜索。
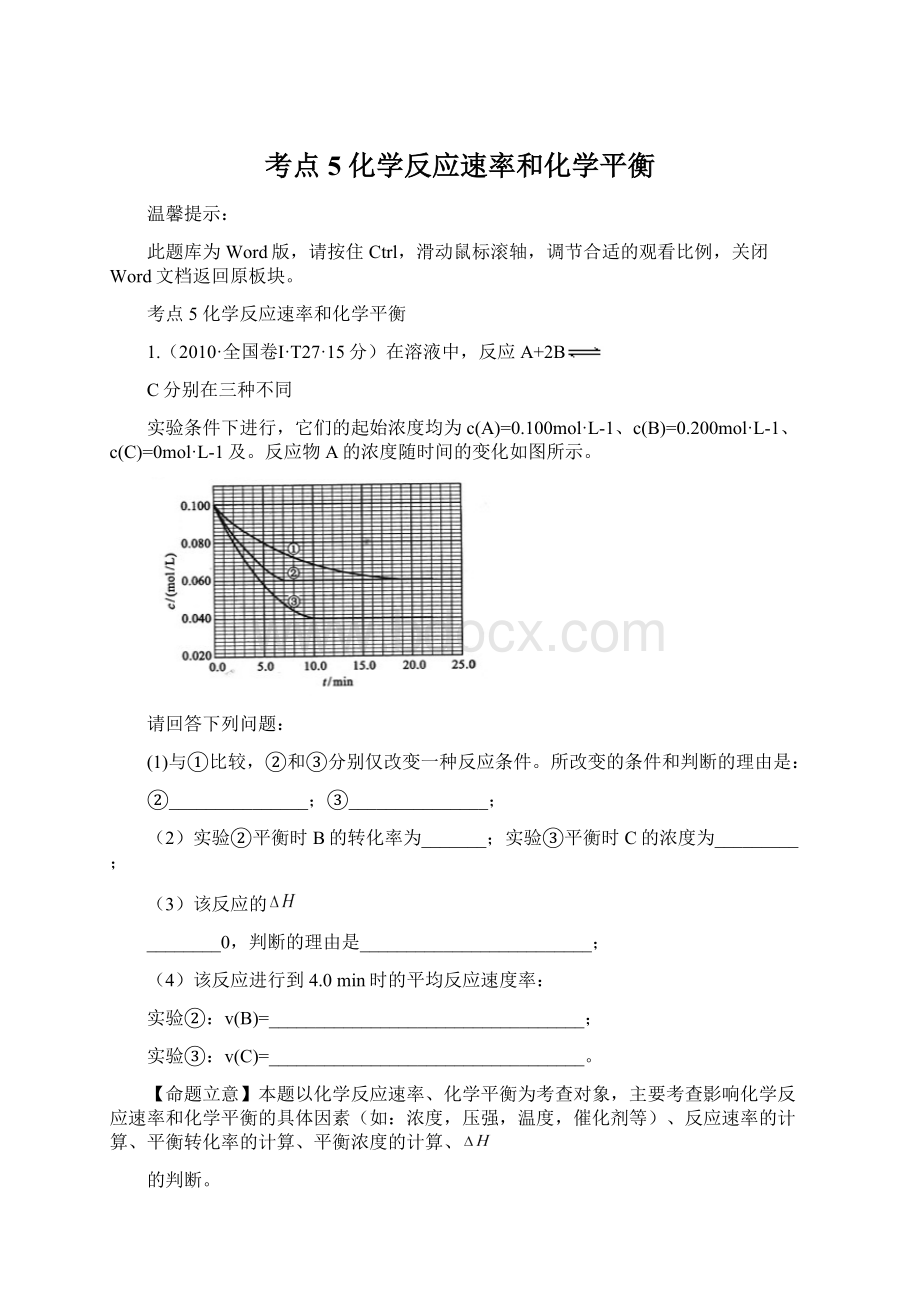
v(C)=__________________________________。
【命题立意】本题以化学反应速率、化学平衡为考查对象,主要考查影响化学反应速率和化学平衡的具体因素(如:
浓度,压强,温度,催化剂等)、反应速率的计算、平衡转化率的计算、平衡浓度的计算、
的判断。
【思路点拨】
(1)
(2)计算化学反应速率的公式:
【规范解答】
(1)②使用了(正)催化剂;
理由:
因为从图像可看出,两者最终的平衡浓度相同,即最终的平衡状态相同,而②比①所需要的时间短,显然反应速率加快了,故由影响反应速率和影响平衡的因素可知是加入(正)催化剂;
③升高温度;
因为该反应是在溶液中进行的反应,所以不可能是改变压强引起速率的改变,又由于各物质起始浓度相同,故不可能是改变浓度影响反应速率,再由于③和①相比达平衡所需时间短,平衡时浓度更小,故不可能是使用催化剂,而只能是升高温度来影响反应速率。
(2)设溶液为1L,则②中达平衡时A转化了0.04mol,由反应计量数可知B转化了0.08mol,所以B的转化率为
;
同样在③中A转化了
0.06mol,则生成C为0.06mol,体积不变,即平衡时c(C)=0.06mol·
L-1
(3)
﹥0;
由③和①进行对比可知升高温度后A的平衡浓度减小,即A的转化率升高,平衡向正反应方向移动,而升温是向吸热的方向移动,所以正反应是吸热反应,
﹥0。
(4)从图上读数,进行到4.0min时,实验②的A的浓度为:
0.072mol·
L-1,则△c(A)=0.10-0.072=0.028mol/L,v(A)=Δc(A)/Δt=
=
0.007mol·
(min·
L-1)所以vB=2v(A)=0.014mol·
(L·
min)-1;
进行到4.0min时实验③的A的浓度为:
0.064mol·
L-1:
△c(A,)=0.10-0.064=0.036mol·
L-1,v(A)′=Δc(A)′=
=0.009mol(L·
min-1),所以v(C)=v(A)=
0.009mol·
min)-1
答案:
(1)②加催化剂;
达到平衡的时间缩短,平衡时A的浓度未变
③温度升高;
达到平衡的时间缩短,平衡时A的浓度减小
(2)40%(或0.4)0.06mol·
L-1(3)﹥升高温度平衡向正反应方向移动,故该反应是吸热反应
(4)0.014mol·
min)-10.009mol·
L-1·
min-1
2.(2010·
全国卷II·
T8·
6分)在相同条件下,下列说法错误的是
A.氯气在饱和食盐水中的溶解度小于在纯水中的溶解度
B.碘在碘化钾溶液中的溶解度大于在纯水中的溶解度
C.醋酸在醋酸溶液中电离的程度大于在纯水中电离的程度
D.工业上生产硫酸的过程中使用过量的空气可提高SO2的利用率
【命题立意】本题以化学平衡和电离平衡为考查对象,主要考查化学平衡和电离平衡的应用及外界条件对平衡的影响。
【思路点拨】利用勒夏特列原理来分析外界条件对化学平衡及电离平衡的影响。
【规范解答】选C。
A选项,由于在饱和食盐水中有大量的Cl-,会抑制氯气与水的反应,从而降低氯气在饱和食盐水中的溶解度,所以A说法正确;
B选项,由于I2+KI====KI3,故碘在碘化钾溶液中的溶解度大于在纯水中的溶解度;
C选项,对于弱电解质来说,浓度越大电离程度越小,醋酸在醋酸溶液中电离的程度小于在纯水中电离的程度,故C错误。
D选项,利用勒夏特列原理可知,用过量的空气相当于增大了氧气的浓度,平衡向正反应方向移动,故可提高SO2的利用率,D说法正确。
3.(2010·
全国卷Ⅱ·
15分)向2L密闭容器中通入amol气体A和bmol
气体B,在一定条件下发生反应;
已知:
平均反应速率
反应2min时,A的浓度减少了
,B的物质的量减少了
mol,有amolD生成。
回答下列问题:
(1)反应2min内,vA=,vB=。
(2)化学方程式中,
、
、
。
(3)反应平衡时,D为2amol,则B的转化率为。
(4)如果只升高反应温度,其他反应条件不变,平衡时D为1.5amol则该反应的△H0;
(填“>”“<”或“=”)
(5)如果其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较:
①反应速率(填:
“增大”“减小或“不变”)。
理由是;
②平衡时反应物的转化率(填:
理由是
__________________。
【命题立意】本题以化学平衡、化学反应速率为考查对象,主要考查化学反应速率的计算与应用、转化率、外界条件对化学平衡的影响等。
【思路点拨】①利用速率公式:
进行运算,根据化学反应速率之比等于化学计量数之比,得出x、y、p、q的值。
②
③利用勒夏特列原理分析外界条件对化学平衡的影响等。
(1)由题意可知:
ΔC(A)=
mol·
L-1,V(A)=
由Δn(B)=
mol,V(B)=
(2)根据化学反应速率之比又等于Δn之比,可得:
x:
y:
q=
:
a=2:
3:
6,又由于
,所以有:
p:
q=2:
1:
6。
(3)平衡时,D为2amol,根据反应:
2A+3B
C+6D可知消耗n(B)=amol,
所以B的转化率=
。
(4)升高温度,平衡向吸热方向移动,根据平衡时D为1.5mol,原平衡时D为2mol,平衡向逆反应方向移动,即正反应为放热反应,ΔH<
0.
(5)将容器的体积由2L变为1L,相当于加压,反应速率增大,平衡向逆反应方向移动,所以反应物的转化率会减小。
min)-1
mol·
min)-1
(2)2316
(3)
(4)<
(5)①增大体积减小,反应物的浓度增大,因而使反应速率增大
②减小体积减小,气体的压强增大,平衡向气体分子数少的方向(即逆反应方向)移动,因而使反应物转化率减小速率之比等于化学计量数之比,又由于反应容器的体积一定,时间都是2min故转化率减小。
4.(2010·
四川高考·
T13·
6分)反应aM(g)+bN(g)
cP(g)+dQ(g)达到平衡
时M的体积分数y(M)与反应条件的关系如图所示。
其中:
Z表示反应开始时N的物质的量与M的物质的量之比。
下列说法正确的是
A.同温同Z时,加入催化剂,平衡时Q的体积分数增加
B.同压同Z时,升高温度,平衡时Q的体积分数增加
C.同温同Z时,增加压强,平衡时Q的体积分数增加
D.同温同压时,增加Z,平衡时Q的体积分数增加
【命题立意】本题以化学平衡为考查对象,主要考查外界条件对化学平衡的影响。
【思路点拨】利用勒夏特列原理及定一议二的方法考虑外界条件对化学平衡的影响。
【规范解答】选B。
A项,加入催化剂,对平衡无影响,Q的体积分数不变,故A错误。
B项,同压同Z时,升高温度,由图像可知M的体积分数y(M)减小,说明平衡向正反应方向进行,所以平衡时Q的体积分数增加,B正确。
C项,同温同Z时,增加压强,对照两个图可知压强越大,M的体积分数y(M)越大,即平衡向逆反应方向移动,平衡时Q的体积分数应减小,所以C错误。
D项,同温同压时增加Z平衡不一定右移,故Q的体积分数不一定增加,所以D错误。
5.(2010·
重庆高考·
T10·
6分)COCl2(g)
CO(g)+Cl2(g);
△H>
0,当反
应达到平衡时,下列措施:
①升温②恒容通入惰性气体③增加CO浓度④减压⑤加催化剂⑥恒压通入惰性
气体,能提高COCl2转化率的是
A.①②④B.①④⑥C.②③⑤D.③⑤⑥
【命题立意】本题以化学平衡为考查对象。
主要考查外界条件对化学平衡的影响。
【思路点拨】利用勒夏特列原理分析外界条件对化学平衡的影响。
①该反应的正反应是吸热反应,升温平衡向正反应方向移动,故可提高COCl2
的转化率。
②恒容通入惰性气体,由于与反应有关的物质的浓度未改变,所以对反应无影响,平衡不移动,故COCl2的转化率不变。
③增加CO浓度,平衡逆向移动,故COCl2的转化率变小。
④减压平衡向正反应方向移动,所以COCl2的转化率变大。
⑤使用催化剂只能影响化学反应速率,对化学平衡无影响。
⑥相当于减压,同④。
综上所述,能提高COCl2的转化率的有①④⑥,故B正确。
【类题拓展】
影响平衡移动的因素只有浓度、压强和温度三个。
1.浓度对化学平衡的影响
在其他条件不变时,增大反应物浓度或减小生成物浓度,平衡向正反应方向移动。
2.压强对化学平衡的影响
在有气体参加或生成的反应中,在其他条件不变时,增大压强(指压缩气体体积使压强增大),平衡向气体体积减小的方向移动。
注意:
恒容时,充入不反应的气体如稀有气体导致的压强增大不能影响平衡.
3.温度对化学平衡的影响
在其他条件不变时,升高温度平衡向吸热反应方向移动。
以上三种因素综合起来就得到了勒夏特列原理(平衡移动原理):
如果改变影响平衡的一个条件(如浓度、压强、温度),平衡就向能够减弱这种改变的方向移动。
说明:
催化剂只能改变达到平衡所需时间,而不能改变平衡移动
6.(2010·
上海高考·
T17·
3分)据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实:
2CO2(g)+6H2(g)
CH3CH2OH(g)+3H2O(g)下列叙述错误的是
A.使用Cu-Zn-Fe催化剂可大大提高生产效率
B.反应需在300℃进行可推测该反应是吸热反应
C.充入大量CO2气体可提高H2的转化率
D.从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率
【命题立意】此题考查化学反应速率和化学平衡知识。
【思路点拨】利用化学平衡知识判断反应吸热还是放热时,一定要注意温度的变化使反应正向移动还是逆向移动。
催化剂能提高化学反应速率,缩短反应时间,也就是提高了生产效率,A正确;
反应需在300℃进行是为了获得较快的反应速率及达到反应所需的温度,不能说明反应是吸热还是放热,B错误;
充入大量CO2气体,能使平衡正向移动,提高H2的转化率,C正确;
从平衡混合物中及时分离出产物,使平衡正向移动,可提高CO2和H2的转化率,D正确。
7.(2010·
T25·
8分)接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
(1)该反应所用的催化剂是(填写化合物名称),该反应450℃时的平衡常数.500℃时的平衡常数(填“大于”、“小于”或“等于”)。
(2)该热化学反应方程式的意义是。
(3)下列描述中能说明上述反应已达平衡的是()
a.
b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
(4)在一个固定容积为5L的密闭容器中充入0.20molSO2和0.10molO2,半分
钟后达到平衡,测得容器中含SO30.18mol,则
=mol·
min-1:
若继续通入0.20molSO2和0.10molO2,则平衡移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,mol<
n(SO3)<
mol。
【命题立意】此题考查了工业制硫酸、化学平衡常数、热化学方程式、化学平衡状态、有关化学平衡的计算等知识。
【思路点拨】化学平衡常数只与温度有关,其随温度变化而变化。
若正反应为吸热反应,温度升高K值增大;
若正反应为放热反应,温度升高K值减小。
(1)工业制硫酸时二氧化硫催化氧化使用的催化剂是五氧化二钒;
该反应正反应为放热反应,故温度越高化学平衡常数越小;
(2)热化学方程式表示的是450℃时,2molSO2气体和1molO2气体完全反应生成2molSO3气体时放出的热量为190kJ;
(3)根据化学平衡状态的特征,容器中气体的平均相对分子质量不随时间变化、分子总数不随时间变化时,说明反应达到平衡状态;
(4)当达到平衡时,容器中SO3的物质的量为0.18mol,则v(SO3)=0.072mol·
min-1,则v(O2)=0.036mol·
min-1;
再继续通入0.20molSO2和0.10molO2时,平衡向正反应方向移动,在此达到平衡时,SO3的物质的量介于0.36和0.40之间。
(1)五氧化二钒(或V2O5)大于
(2)在450℃时,2molSO2气体和1molO2气体完全反应生成2molSO3气体时放出的热量为190kJ(3)bd(4)0.036向正反应方向0.360.40
关闭Word文档返回原板块。