高中化学 142 元素分析和相对分子质量的测定课时作业 新人教版选修5Word文档格式.docx
《高中化学 142 元素分析和相对分子质量的测定课时作业 新人教版选修5Word文档格式.docx》由会员分享,可在线阅读,更多相关《高中化学 142 元素分析和相对分子质量的测定课时作业 新人教版选修5Word文档格式.docx(11页珍藏版)》请在冰豆网上搜索。
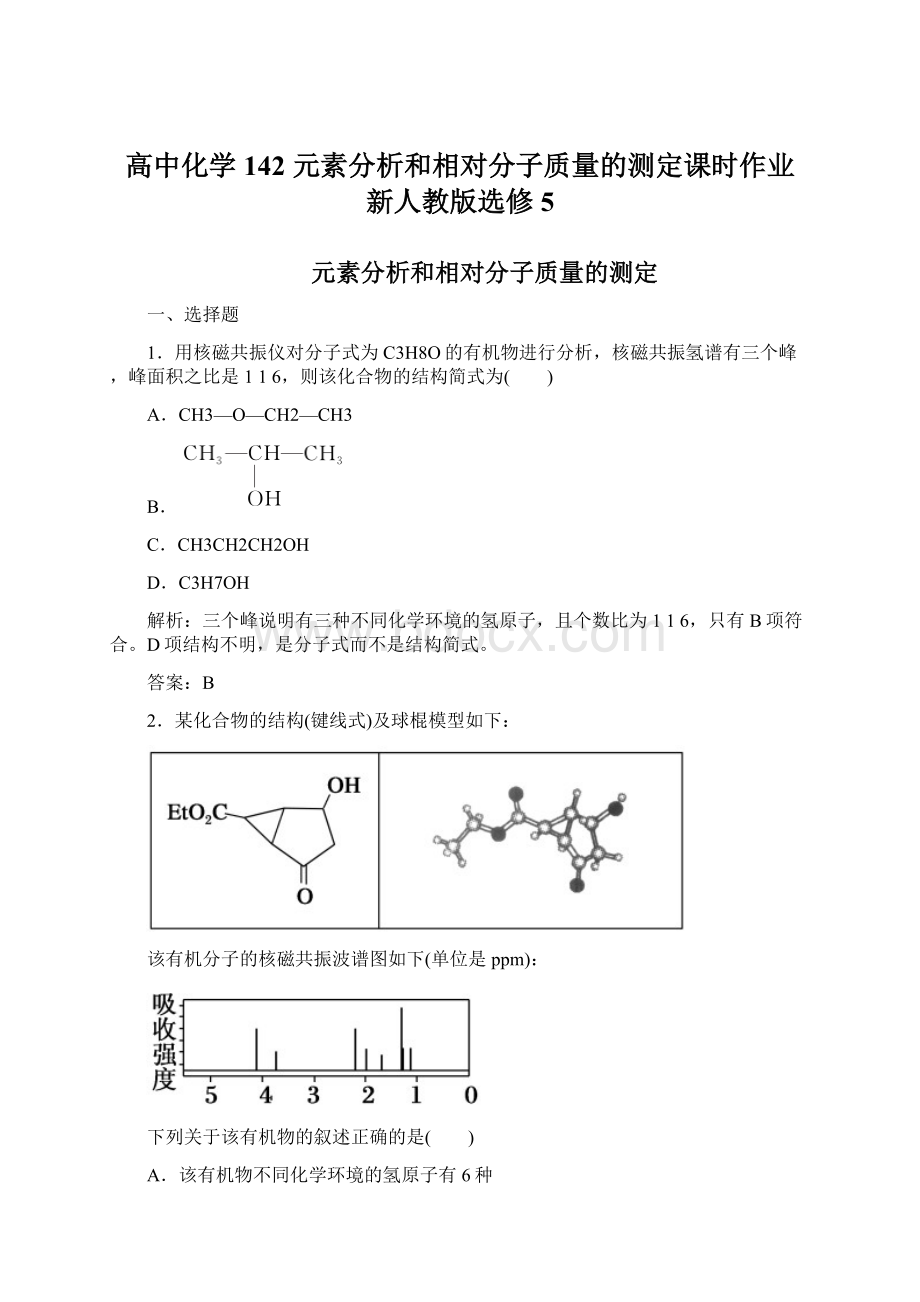
A.该有机物不同化学环境的氢原子有6种
B.该有机物属于芳香化合物
C.键线式中的Et代表的基团为—CH3
D.该有机物在一定条件下能够发生消去反应
A项,由谱图可知有8种不同环境的氢原子,A错;
B项,由键线式可看出,该物质中无苯环,不属于芳香化合物,B错;
C项,Et为—CH2CH3,C错。
D
3.已知某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法不正确的是( )
A.由红外光谱可知,该有机物中至少有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子
C.仅由核磁共振氢谱无法得知其分子中的氢原子总数
D.若A的化学式为C2H6O,则其结构简式为CH3—O—CH3
由A的红外光谱知A中有—OH,由A的核磁共振氢谱知A中有3种氢原子,故若A的化学式为C2H6O,则其结构简式为CH3CH2OH。
4.已知某有机物A的核磁共振氢谱如下图所示,下列说法中,错误的是( )
A.若A的分子式为C3H6O2,则其结构简式为CH3COOCH3
B.由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子,且个数之比为123
C.仅由其核磁共振氢谱无法得知其分子中的氢原子总数
D.若A的化学式为C3H6O2,则其同分异构体有三种
由核磁共振氢谱可知,其分子中含有三种不同化学环境的氢原子,峰的面积之比等于其原子个数之比,但不能确定具体个数,故B、C正确;
由A的分子式C3H6O2可知,其同分异构体有3种:
CH3COOCH3、CH3CH2COOH、HCOOCH2CH3。
其中有三种不同化学环境的氢原子且个数之比为123的有机物的结构简式为CH3CH2COOH或HCOOCH2CH3。
故正确答案为A。
A
5.验证某有机物属于烃,应完成的实验内容是( )
A.只测定它的C、H比
B.只要证明它完全燃烧后产物只有H2O和CO2
C.只测定其燃烧产物中H2O与CO2的物质的量的比值
D.测定该试样的质量及试样完全燃烧后生成CO2和H2O的质量
当CO2和H2O中m(C)+m(H)=m(有机物)时,说明有机物中没有氧元素。
6.某混合气体由两种气态烃组成2.24L该混合气体完全燃烧后,得到4.48L二氧化碳(气体已折算为标准状况)和3.6g水,则这两种气体可能是( )
A.CH4和C3H8B.CH4和C3H4
C.C2H4和C3H4D.C2H4和C2H6
n(C)=
=0.2mol,
n(H)=
×
2=0.4mol,
n(混合物)n(C)n(H)=124。
所以该混合气体的平均分子式为C2H4。
符合题意的组合只有B选项。
7.某有机物样品3.1g完全燃烧,燃烧后的混合气体通入过量的澄清石灰水中,石灰水共增重7.1g,经过滤、干燥得到10g沉淀。
该有机物样品可能是( )
A.乙烯B.乙醛
C.乙酸D.乙二醇
根据题意,10g沉淀为CaCO3,则产生的二氧化碳为0.1mol,即4.4g,其中碳元素质量为0.1mol×
12g/mol=1.2g,石灰水增重7.1g,所以有机物燃烧生成的水的质量为7.1g-4.4g=2.7g,即n(C)=0.1mol,n(H)=
2=0.3mol,氢元素质量为0.3mol×
1g/mol=0.3g,有机物样品共3.1g,所以氧元素的质量=3.1g-1.2g-0.3g=1.6g,物质的量为
=0.1mol,碳、氢、氧原子的物质的量之比为131,即最简式为CH3O,只有D符合。
8.在120℃条件下,3.7g某有机物(只含C、H、O三种元素中的两种或三种)在足量O2中燃烧后,将所得气体先通过浓H2SO4,浓H2SO4增重2.7g,再通过碱石灰,碱石灰增重6.6g,对该有机物进行核磁共振分析,谱图如下图所示:
则该有机物可能是( )
A.HCOOCH2CH3B.CH3CH2C≡CH
C.CH3CH2OHD.CH2===CHCH3
浓H2SO4吸水,增重的质量即为H2O的质量为2.7g,计算得m(H)=0.3g,n(H)=0.3mol;
碱石灰吸收CO2,则CO2的质量为6.6g,计算得m(C)=1.8g,n(C)=0.15mol;
根据以上数据可计算得m(O)=3.7g-0.3g-1.8g=1.6g,n(O)=0.1mol。
此有机物中C、H、O原子个数之比为0.150.30.1,即362,只有A选项正确,且A选项中氢原子共有三类,对应核磁共振氢谱中有三个峰。
9.由E(金属铁)制备的E(C5H5)2的结构如图甲所示,其中氢原子的化学环境完全相同。
但早期人们却错误地认为它的结构如图乙所示。
核磁共振法能区分这两种结构。
甲和乙的核磁共振氢谱中,分别有几种吸收峰( )
A.1种 1种B.1种 2种
C.1种 3种D.2种 3种
甲中氢原子的化学环境完全相同,其核磁共振氢谱中只有1种吸收峰;
乙中与铁相连的2个五元环结构全等,每个五元环中有3种不同化学环境的氢原子,则其核磁共振氢谱中有3种吸收峰。
C
10.某化合物6.4g在氧气中完全燃烧,只生成8.8gCO2和7.2gH2O。
下列说法正确的是( )
A.该化合物仅含碳、氢两种元素
B.该化合物中碳、氢原子个数比为14
C.无法确定该化合物是否含有氧元素
D.该化合物一定是C2H8O2
n(CO2)=
=0.2mol,n(H2O)=
=0.4mol。
m(C)+m(H)=0.2mol×
12g·
mol-1+0.4mol×
2×
1g·
mol-1=3.2g<
6.4g,故n(O)=
=0.2mol。
则n(C)n(H)n(O)=0.2mol(0.4mol×
2)0.2mol=141,该化合物的实验式为CH4O。
由于CH4O中氢原子已饱和,故实验式即化学式。
11.下图是A、B两种物质的核磁共振氢谱。
已知A、B两种物质都是烃类,都含有6个氢原子。
请根据下图两种物质的核磁共振氢谱谱图选择出可能属于下图的两种物质( )
A.A是C3H6;
B是C6H6B.A是C2H6;
B是C3H6
C.A是C2H6;
B是C6H6D.A是C3H6;
B是C2H6
核磁共振氢谱是记录不同氢原子核对电磁波的吸收情况来推知氢原子种类的谱图。
根据题目所示的谱图,图1中只有一种氢原子,且是稳定的氢原子,所以图1中C2H6。
在图2中,氢原子中有3种,且比例为213,符合此情况的物质分子是C3H6。
C3H6的结构简式为CH3—CH===CH2,其中氢原子有三种,这三种氢原子的原子核吸收的电磁波的强度不相同,且是312的,因此图2是C3H6的核磁共振氢谱谱图。
12.某气态化合物X含C、H、O三种元素,现已知下列条件:
①X中C的质量分数;
②X中H的质量分数;
③X在标准状况下的体积;
④X对氢气的相对密度;
⑤X的质量。
欲确定X的分子式,所需的最少条件是( )
A.①②④ B.②③④ C.①③⑤ D.①②
由①②可确定该气态化合物的最简式,若要确定X的分子式,还需要知道X的相对分子质量,即需要知道X对H2的相对密度。
二、填空题
13.有机物A满足下列条件:
①A在空气中完全燃烧的产物是CO2和H2O,且燃烧过程中产生CO2的物质的量等于消耗O2的物质的量,也恰好和生成H2O的物质的量相等;
②质谱法测定A的相对分子质量为180,分子中含有六元环;
③碳原子和氧原子在分子结构中都有两种不同的化学环境,且A的核磁共振氢谱中有3个吸收峰。
回答下列问题:
(1)A的实验式(最简式)是________________________________。
(2)A的分子式是_______________________________________。
(3)A的结构简式是_____________________________________。
(4)A有一种同分异构体B,其分子中也有六元环,所有碳原子都处于相同的化学环境中,其结构简式是_________________________
__________________________________________________________。
燃烧时n(CO2)=n(O2),说明有机物的分子式可表示成Cx(H2O)y,n(CO2)=n(H2O),说明有机物分子中碳原子数与氢原子数之比为12,故其最简式为CH2O,结合A的相对分子质量为180可知,A的分子式为C6H12O6。
由该有机物分子中碳原子和氧原子都有两种不同的化学环境且分子中含有六元环知,该六元环必是由3个碳原子和3个氧原子交替连接形成。
剩下的3个碳原子和3个氧原子有两种组合方式,1种是CH3O—,1种是HOCH2—,再结合分子中氢原子处于3种不同的化学环境可得出正确结论。
若所有碳原子均处于相同的化学环境,则必是由6个碳原子形成六元环。
(1)CH2O
(2)C6H12O6
14.有机物分子式的确定常采用燃烧法,其操作如下:
在电炉加热下用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。
如图所示是用燃烧法测定有机物分子式常用的装置,其中A管装碱石灰,B管装无水CaCl2。
现准确称取1.80g有机物样品(含C、H元素,还可能含有O元素),经燃烧被吸收后A管质量增加1.76g,B管质量增加0.36g。
请按要求填空:
(1)此法适宜于测定固体有机物的分子式,此有机物的组成元素可能是________。
(2)产生的气体按从左到右的流向,所选各装置导管口的连接顺序是________。
(3)E和D中应分别装有何种药品________。
(4)如果将CuO网去掉,A管增加的质量将________(填“增大”“减小”或“不变”)。
(5)该有机物的最简式是______________________________。
(6)要确定该有机物的分子式,还必须知道的数据是______。
A.消耗E中液体的质量
B.样品的摩尔质量
C.CuO固体减少的质量
D.C装置增加的质量
E.燃烧消耗氧气的物质的量
(7)在整个实验开始之前,需先让D产生的气体通过整套装置一段时间,其目的是___________________________________________
_________________________________________________________。
(1)B管质量增加为所吸收的水的质量,A管质量增加为所吸收CO2的质量。
m(H2O)=0.36g,m(H)=0.36g×
2/18=0.04g。
m(CO2)=1.76g,m(C)=1.76g×
12/44=0.48g。
1.80g-0.04g-0.48g=1.