GMP对制药厂房设计地要求aWord文档下载推荐.docx
《GMP对制药厂房设计地要求aWord文档下载推荐.docx》由会员分享,可在线阅读,更多相关《GMP对制药厂房设计地要求aWord文档下载推荐.docx(29页珍藏版)》请在冰豆网上搜索。
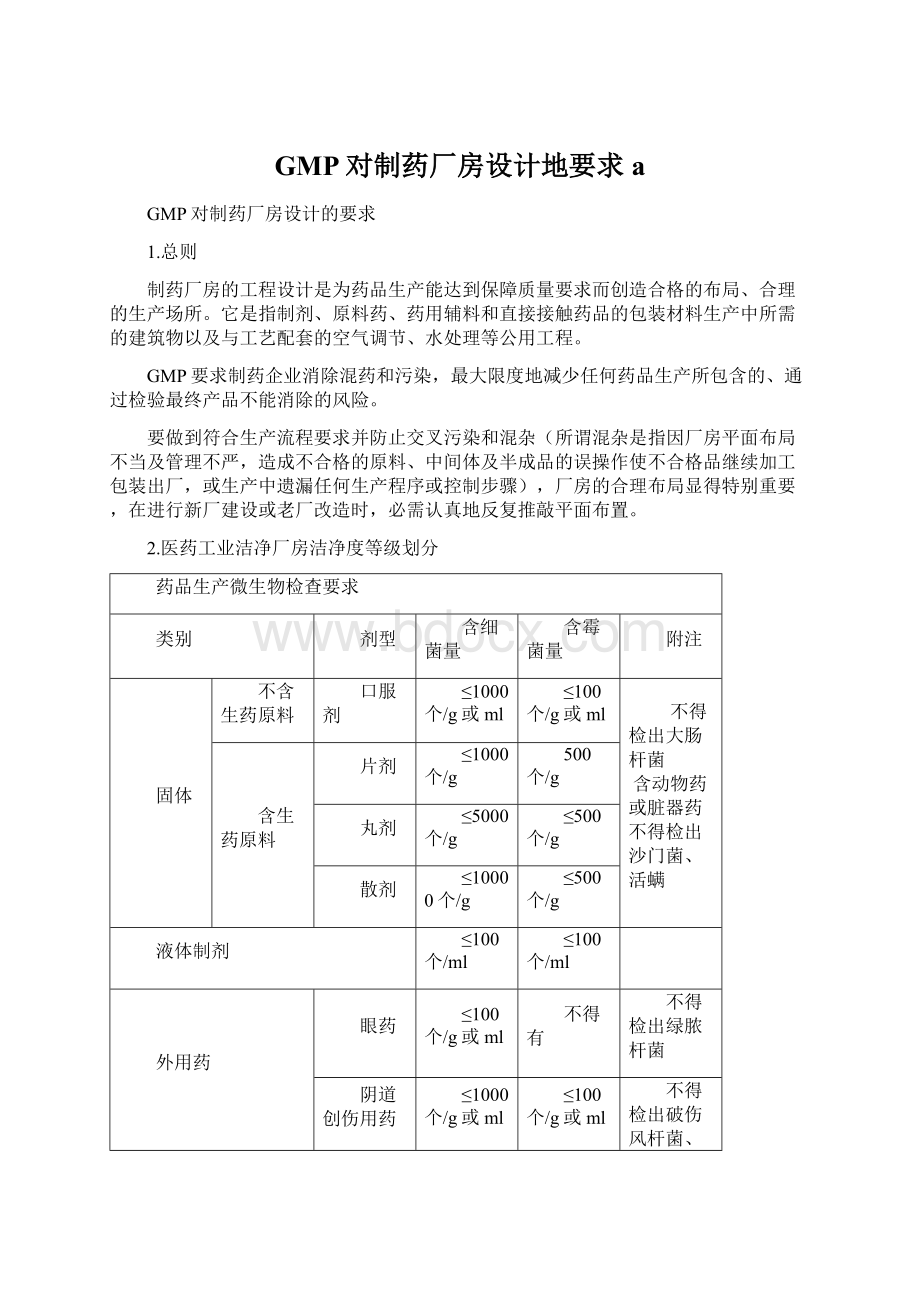
散剂
≤10000个/g
液体制剂
≤100个/ml
外用药
眼药
不得有
不得检出绿脓杆菌
阴道创伤用药
不得检出破伤风杆菌、绿脓杆菌。
药品生产洁净室(区)空气洁净度级别
洁净度级别
尘粒最大允许数/个.m-3
微生物最大允许数
≤0.5μm
≥5μm
浮游菌/个.m-3
沉降菌/个.皿-1
100级
3500
5
1
10000级
35000
2000
100
3
100000级
3500000
20000
500
10
300000级
10500000
60000
15
注:
①300000级是参考美国联邦标准洁净室和洁净区内空气浮游粒子洁净等级。
②空气洁净度的测试以静态条件为依据,测试方法应符合国家医药管理局《医药工业洁净室和洁净区悬浮粒子的测试方法》的规定。
③对于空气洁净度为100级的洁净室,室内100尘粒的计数,应进行多次采样,当其多次出现时,方可认为该测试数据是可靠的。
3.药品生产洁净区划分
药品生产洁净区的划分
原料药
洁净等级
百级及万级背景下的百级
万级
10万级
>
法定药品标准中列有无菌检查项目的原料药
其他原料药的生产暴露环境
无菌药品:
指有无菌检查项目(不存在活的生物)的药品。
最终灭菌药品
大容量注射剂(≥50ml)的灌装加塞;
①注射剂的稀配、过滤;
②小容量注射剂的灌封;
③直接接触药品的包装材料的最终处理
注射剂浓配或采用密闭系统的稀配。
非灭菌
药品
①罐装前不需过滤的药液配置;
②注射剂的灌封、分装和压塞;
③直接接触药品的包装材料最终处理后的暴露环境。
罐装前需除菌过滤的药液配置
轧盖,直接接触药品的包装材料最后一次精洗的最低要求
非无菌药品:
法定药品标准中未列无菌检查项目的制剂
①非最终灭菌口服液药品的暴露工序:
●片剂、硬胶囊剂、颗粒剂中的称量、配料、制粒、干燥、混合、压片包衣;
●颗粒式胶囊灌装;
●内包装及相应中间开口工序;
●粉针剂的清洗瓶工序、干燥灭菌室、无菌服配备和轧盖工序;
②深部组织创伤外用药品、眼用药品的暴露工序;
③除直肠用药外的腔道用药的暴露工序。
①最终灭菌口服液体药品的暴露工序;
②口服固体药品的暴露工序;
③表皮外用药品的暴露工序。
生物制品
罐装前不经除菌过滤的制品及其配置、合并、灌封、冻干、加塞、添加稳定剂、佐剂、灭活剂等;
①罐装前需经除菌过滤的制品及其配置、合并、精制、添加稳定剂、佐剂、灭活剂除菌过滤、超滤等;
②体外免疫诊断试剂的阳性血清的分装、抗原-抗体分装;
③粉针剂中的灭菌瓶胶塞冷却储存室、分装室、无菌更衣室、无菌缓冲走廊。
①原料血浆的合并、非低温提取、分装前的巴士消毒、轧盖及制品最终容器的清洗等;
②口服制剂其发酵培养密闭系统环境(暴露部分需无菌操作);
③酶联免疫吸附试剂的包装、配液、分装、干燥;
胶体金试剂(PCR)、纸片法试剂等体外免疫试剂;
④深部组织创伤用制品和大面积体表创面用制品的配制、灌装。
4.制药生产简介及洁净区的划分
●无菌原料药精制、干燥、包装生产流程及环境划分
用于口服剂生产的生产流程示意及环境划分
粗品或
浓缩液活性炭溶剂
包装桶过筛结晶分离干燥
清洁贮存包装混粉过筛
内包装材料清理入库
注:
10万级洁净区域
用于灌装前需经除菌过滤的生物制品
抗生素粗活性溶玻璃瓶瓶纯注射
浓缩液品炭剂或铝瓶塞水用水
过滤
无菌过滤结晶粗洗过滤过滤
喷雾干燥干燥分离清洗
过筛混粉精洗
装瓶装瓶干燥灭菌
标签贴签冷却
纸箱装箱入库
注:
局部100级环境;
万级环境;
10万级环境
口服液生产布置方案
成品
成品库包装材料
成品包装包装材料库
中
间灌洗洗
品装瓶瓶
库更衣
人员原
配药材
存外衣男更料
女更溶媒处理室库
原料
●粉针剂生产、包装流程及洁净环境划分
粉针剂生产:
以青霉素制剂为例。
1粉剂制作:
为了取得纯菌种,必须在没有其他杂菌的试管中保存单一的细菌孢子。
从试管中取出少许孢子后,把它涂布在斜面培养基上,再从斜面上选种,置入母瓶摇动发芽。
待种子量扩大后,置入冰库备用。
接种时,先将母瓶中的种子投入小罐生长,再从管道进入中罐而后过渡到大发酵罐。
利用细菌的尸体溶液反复多次提炼,从溶液中分离出结晶,再进行过滤提纯、烘干。
①细菌的培养虽然在密封罐里进行,但选种与接种等大都暴露在
细菌接种选种室内容气中,使用敞开的容器进行提取结晶、真空烘干和粉剂研磨
也并非流水作业,不断接触室内
①生物细菌培养西林瓶胶基空气,故需要环境净化条件。
化验②提炼工作往往使用大量的有
机溶剂如乙醇、丁醇、乙酸乙酯
②溶液的过滤、丙酮、酒精等等。
不可避免局
提炼精制洗瓶清洗处理部泄漏。
针剂灌封与接种时使
用煤气或液化石油气火头,厂
结晶房需考虑
干燥灭菌干燥灭菌抽检铝盖防火与防
烘干爆。
磨细分装加橡皮塞轧盖
外送装箱包装贴签封蜡视检
成品化验
注局部100级净化区域;
万级净化区域;
10万级净化区域。
粉针剂制作车间,发酵部分因设备尺寸大并且成组布置,需要安排在较大的空间内,适合用局部净化气流装置等加强其炉口操作环境的净化。
其余各工序对平面尺寸和净空都没有特殊要求。
一般需在洁净工作台配合下进行全室空气净化。
房间之间流水关系不强,布置较为灵活。
2.粉剂分装:
粉针剂装在西林瓶内再封胶塞和轧盖。
瓶与塞都要事先清洗与干燥灭菌。
从清洗分装
直到轧盖前,仍容易混入尘埃和微生物。
一旦混入,则粉剂制作阶段的净化工作将前功尽弃。
因而瓶与塞的清洗用水/清洗与干燥的环境/分装设备及其操作环境都需要高洁净度。
为了确保药品质量,后工序的抽检/轧盖也需要较高的净化条件。
粉剂分装车间的工艺流水性极强,用分装线顺序串通各有关房间。
容器与药品从传递窗进入。
分装间尺寸取决于分装线的设备数量与组合,但单台设备尺寸不大。
厂房净高一般在2.5-3.0之间。
因此制药工业厂房往往布置成多层的形式。
粉针布置示意
无菌药粉包材
100
加
瓶子灭菌隧道分装轧盖成品
塞
10万洗瓶1万分装10万
●无菌分装注射剂生产流程及环境区域划分
冻干用分装用空安瓶胶塞
原料原料
割园酸或碱处理
擦洗消毒擦洗消毒洗瓶饮用水洗饮用水
配料纯水洗纯水
灭菌干燥
检查注射用水洗注射用水
无菌过滤冷却
硅化
灌装分装
铝盖
冻干加塞轧盖灭菌
热源试验
灭菌检漏无菌试验
轧盖灯检封蜡白蜡
入库装箱装盒贴签
纸箱纸盒标签
胶塞冷却贮藏室、分装室、无菌更衣室、无菌缓冲走廊均为万级净化区域。
局部100级净化区域;
●可灭菌大容量注射剂的生产流程及净化区域划分
饮用水胶塞隔离膜输液瓶原辅料
离子交换酸碱处理乙醇浸泡瓶外清洗称量
浓配
纯水粗洗清洗清洗剂处理过滤
煮沸粗洗稀配
过滤清洗清洗清洗粗滤
蒸馏精滤
精洗灌装
注射用水
放膜
精洗
精洗上塞
过滤翻塞
入库包装贴签灯检灭菌轧口加盖
纸箱标签铝盖
水针剂布置示意
药液包材
洗瓶100
安瓶万级灭菌灯检成品
干燥灭菌灌封检漏印包
万级
●可灭菌小容量注射剂工艺流程示意及净化区域划分
粉剂加注射用水配制注射液,将注射液进行配药过滤后即可进行灌封.安瓶在清洗前要先进行割园.从安瓶清洗干燥灭菌到灌封都需要环境净化.水针剂在灌封之后还有无菌检漏工序,故在灭菌方面较之粉针剂条件有利一些,但是水针剂对非生物粒子的控制更为严格。
平面布置的情况与粉针剂分装车间类似。
饮用水安瓶原料
离子交换切割配制
纯水过滤粗洗粗滤
蒸馏精洗精滤
干燥灭菌灌装
注射用水冷却封口灭菌检漏
入库包装印字灯检
纸盒纸箱
●胶囊剂生产流程及环境区域划分
制剂原辅料
化验
配料黏合剂/湿润剂
混合
制软材
空胶囊内包装玻璃瓶
制粒
干燥整粒消毒干燥洗瓶
检囊装囊装瓶冷却
打光外包装
FVC片
铝塑包装检片包装成品
10万级净化区域
局部100级净化区域
●片剂的生产
原料药的粉碎、制粒与干燥工段会产生大量粉尘(根据生产情况不同可能达到空气浓度
5mg/m3左右),一方面需要加强排风,一方面还要净化。
压片工作既不能吸收水分又不能混进灰尘。
片剂生产还要注意的一条就是要对生产区的粉尘进行有效的控制,防止粉尘通过空气系
统发生混药