复分解反应的条件离子反应方程式Word格式文档下载.docx
《复分解反应的条件离子反应方程式Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《复分解反应的条件离子反应方程式Word格式文档下载.docx(18页珍藏版)》请在冰豆网上搜索。
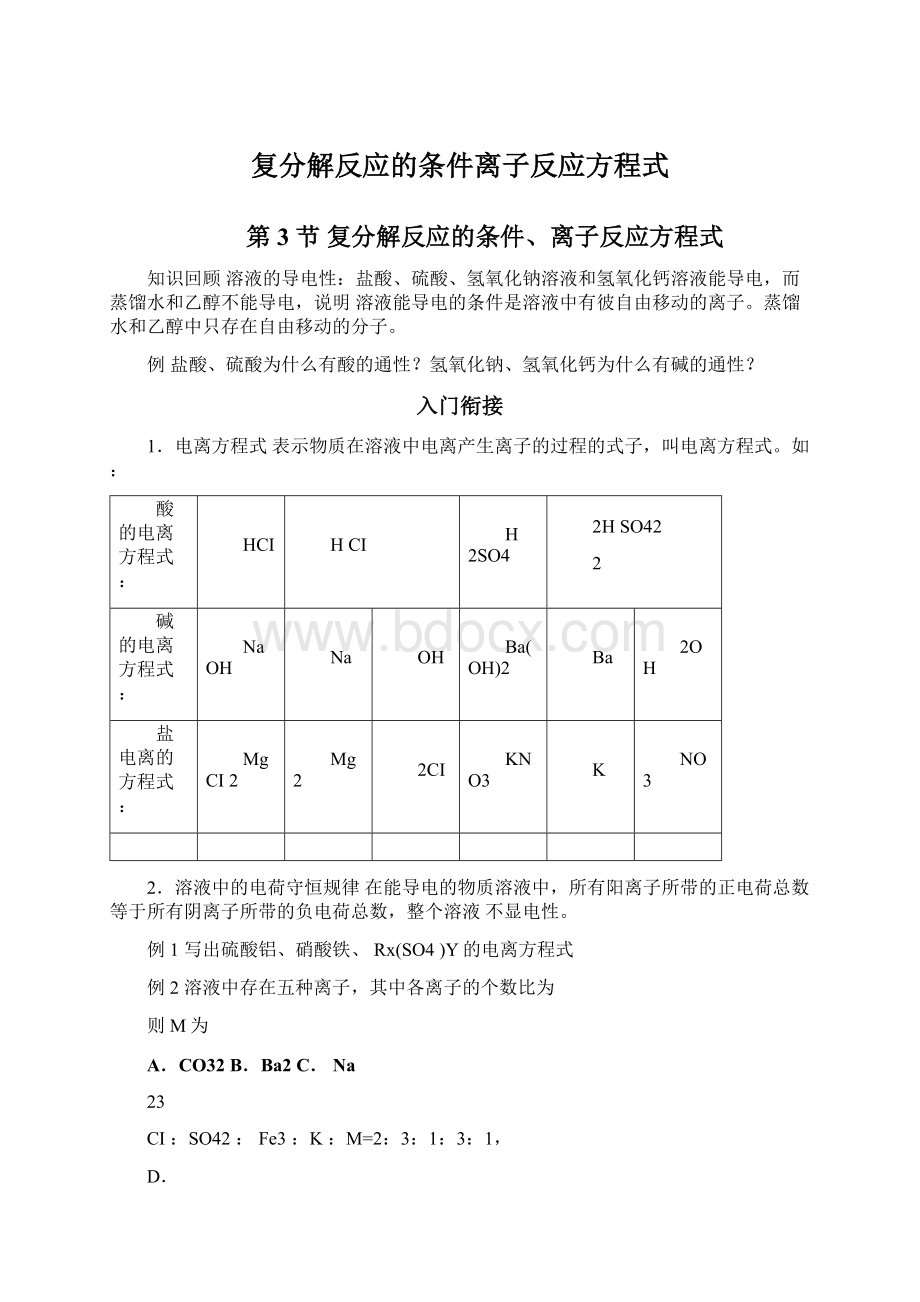
盐电离的方程式:
MgCI2
Mg2
2CI
KNO3
K
NO3
2.溶液中的电荷守恒规律在能导电的物质溶液中,所有阳离子所带的正电荷总数等于所有阴离子所带的负电荷总数,整个溶液不显电性。
例1写出硫酸铝、硝酸铁、Rx(SO4)Y的电离方程式
例2溶液中存在五种离子,其中各离子的个数比为
则M为
A.CO32B.Ba2C.Na
23
CI:
SO42:
Fe3:
K:
M=2:
3:
1:
1,
D.
Mg
3.电解质和非电解质电解质:
在水溶液中或熔融状态下能导电的化合物。
如氯化钠、硝酸钾。
非电解质:
在水溶液中和熔融状态下都不能导电的化合物。
如酒精、葡萄糖。
酸、碱、盐在水溶液中能够导电,是因为它们在溶液中发生电离,产生了能够自由移动的离子,酸、碱、盐属于电解质。
我们知道氯化钠、硝酸钾、氢氧化钠等固体不导电,而它们的水溶液能够导电。
原因是它们在水溶液里发生了电离,产生了能够自由移动离子。
如果我们将氯化钠、硝酸钾、氢氧化钠等固体分别加热至熔化,它们也能导电。
这些在水溶液里或熔化状态下能够导电的化合物叫做电解质。
蔗糖、酒精等化合物,无论是在水溶液或熔化状态都不导电,这些化合物叫做非电解质。
练习:
请填下表。
电解质
非电解质
定义
物质种类
大多数酸碱盐、部分氧化物
大多数有机化合物、CO、SO2、NH3等
能否电离
在溶液中存在形态
离子或
实例
H2SO4、NaOH、
C2H5OH、CO2、
4.强电解质与弱电解质
按下图装置把仪器连接好,然后把相同条件下的HCI、CH3COOH、CH3COOH、NaOH、NaCI溶液和氨水分别倒入五个烧杯中,接通电源,观察灯泡发光的明亮程度。
实验结果表明:
连接插入CH3COOH溶液和氨水的电极上的灯泡比其他三个灯泡暗。
可见它们在同样条件下的导电能力是不相同的。
HCI、NaOH和NaCI溶液的导电能力比CH3COOH溶液和氨水强。
这是为什么呢?
我们可以从这些物质的结构和它们在水溶液中所发生的变化来进行分析。
从物质结构的观点来看,NaCI、NaOH等是由阴离子和阳离子构成的离子化合物。
当这类物质溶解于水时,在水分子的作用下,阴、阳离子脱离晶体表面,全部电离成为能够自由移动的水合阴离子和水合阳离子(如图)。
为了简便起见,通常仍用离子符号来表示水合离子。
例如,NaCI和NaOH的电离方
程式为:
NaCI
NaCI
NaOH
不仅是离子化合物,像HCI这样的共价化合物在液态时虽不导电,但溶于水后,在水分子的作用下,也能全部电离成水合氢离子和水合氯离子。
HCIHCI实验证明,在大多数盐类、强酸和强碱的水溶液里,只有水合离子,没有溶质分子,它们是全部电离的。
在水溶液里全部电离成离子的电解质叫做强电解质。
例如,NaOH、KOH、HCI、HNO3、H2SO4、
NaCI、KNO3等都是强电解质。
在水溶液里只有一部分分子电离成离子的电解质叫做弱电解质。
弱酸、弱碱是弱电解质,如CH3COOH、NH3·
H2O等,水也是弱电解质。
请填写下表
强电解质
弱电解质
化合物种类
离子化合物、
电离条件
溶液里的粒子
物质类别实例
强酸:
等强碱:
等
弱酸:
绝大多数盐等
5.离子反应
由于电解质溶于水后就电离成为离子,所以,电解质在溶液里所起的反应实质上是离子之间的反应,这样的反应属于离子反应。
在试管里加入少量CuSO4溶液,再加入少量NaCI溶液,观察有无变化。
在另一支试管里加入5mLCuSO4溶液,再加入5mLCuSO4溶液,过滤。
观察沉淀和滤液的颜色。
在第三支试管里加入少量上述滤液,并滴加AgNO3溶液,观察沉淀的生成。
再滴加稀硝酸,观察沉淀是否溶解。
将有关的实验现象列表如下:
通过对上述实验现象的分析,我们可以得出这样的结论:
当CuSO4溶液与NaCI溶液混合时,没有发生化学反应,只是CuSO4电离出来的Cu2、SO42与NaCI电离出来的Na、CI的混合;
当CuSO4
溶液与BaCI2溶液混合时,CuSO4电离出来的Cu2和BaCI2电离出来的CI都没有发生化学反应,而
CuSO4电离出来的SO42与BaCI2电离出来的Ba2发生化学反应,生成了难溶的BaSO4白色沉淀。
CuSO4+BaCI2===CuCI2BaSO4也就是说,这个反应的实质是:
SO42+Ba2==BaSO4这种用实质参加反应的离子的符号表示离子反应的式子叫做离子方程式。
怎样书写离子方程式呢?
我们仍以CuSO4溶液与BaCI2溶液的反应为例,说明书写离子方程式步骤。
第一步,写出反应的化学方程式:
CuSO4+BaCI2===CuCI2BaSO4第二步,易溶于水、易电离的物质写成离子形式,难溶的物质或难电离的物质以及气体等仍用化学式表示。
上述化学方程式可改写成:
CuSO42Ba22CICu22CIBaSO4
第三步,删去方程式两边不参加反应的离子:
Ba2SO42BaSO4
第四步,检查离子方程式两边各元素的原子个数和电荷总数是否相等。
经检查,上述离子方程式两边各元素的原子个数和电荷总数都相等,所写的离子方程式正确。
我们学过的复分解反应,实质上就是两种电解质在溶液中相互交换离子的反应。
这类离子反应发生的
条件就是复分解反应发生的条件,即有难溶的物质(如BaSO4、AgCI)或难电离的物质(如H2O)或
挥发性的物质(如CO2)生成,只要具备上述条件之一,这类离子反应就能发生。
表是几种不同的酸与不同的碱发生反应的化学方程式和离子方程式。
化学方程式
离子方程式
NaOHHCI
NaCIH2O
H
H2O
KOHHCI
KCIH2O
2NaOHH2SO
4Na2SO42H2O
2KOHH2SO4
K2SO42H2O
上面的四个反应都是中和反应,虽然每一个反应的化学方程式不同,但它们的
离子方程式却是相同的。
这表明:
酸与碱发生中和反应的实质是由酸电离出来的
H与由碱电离出来的OH结合生成了H2O。
离子方程跟一般的化学方程式不同,它不仅可以表示某一个具体的化学反应,而且还可以表示同一类型的离子反应。
在九年级化学中我们已经学过,可以利用盐酸和澄清的石灰水来检验某物质是不是碳酸盐。
如果在某物质中滴加盐酸后,有能使澄清石灰水变浑浊的无色、无味
气体产生,就可以证明该物质是碳酸盐。
在书写CO3检验的离子方程式时需要考虑两种情况:
1.如果被检物是可溶性的碳酸盐,如
Na2CO3、K2CO3、(NH4)2CO3等,则这类碳酸盐检验的离
子方程式为:
CO322HH2OCO2
CO2Ca22OHCaCO3H2O
2.如果被检物是不溶性的碳酸盐,如
CaCO3等,则该物质检验的离子方程式为:
CaCO32HCa2H2OCO2CO2Ca22OHCaCO3H2O
书写离子方程式应注意下面几个问题:
(1)离子反应是在水溶液中或熔化状态下进行的,除此以外均无离子方程式。
(2)强酸、强碱和易溶性的盐改写成离子形式,难溶物、难电离的物质(如弱酸、弱碱、水等)、易
挥发性物质、单质、氧化物、非电解质等均不能拆,要写化学式。
(3)微溶性物质如作生成物,一律视为沉淀,写化学式,标“”;
如作反应物,若是澄清溶液应改写成离子符号,若是悬浊液应写化学式。
(4)多元弱酸的酸式酸根离子,不能改写或拆开,如HCO3不能拆成H和CO3
5)要保持原物质的组成比例,如H2SO4与Ba(OH)2的反应的离子方程式为:
2H
22
SO422OHBa2BaSO4
而不是HSO42
Ba2BaSO4
(6)要符合反应物的质量之比。
例如:
NaHCO3与Ca(OH)2溶液反应。
①当NaHCO3过量时,Ca22OH
2HCO3
CaCO
32H2
OCO32
②当Ca(OH)2过量时,Ca2OH
HCO3
CaCO3
例1下列离子方程式,正确的是
(
)
A.NaHCO3溶液与NaOH溶液反应:
OHCO32H
2O
B.少量二氧化碳通入足量的NaOH溶液:
CO2
C.Fe与盐酸反应产生H2:
2Fe6H
2Fe
33H2
D.氨水和醋酸溶液混合:
NH3·
H2OCH3COOHNH4CH3COOH2O
例2离子方程式HOHH2O可表示的化学反应是()
A.盐酸和氢氧化钡溶液的反应B.硝酸溶液和氢氧化镁的反应
C.硫酸溶液和氢氧化钡溶液的反应D.盐酸和氨水的反应
例3下列各组离子中,能在强酸溶液里大量共存,并且溶液呈无色透明的是(
A.MnO4、K、Na、SO42B.Na、K、HCO3、CI
2222
C.Mg2、NH4、CI、NO3D.Ba2、K、S2、SO42
例4某地有甲、乙两工厂排放污水,污水中存在下列8种离子中的4种(两厂不含大量相同离子)
Fe3、OH、Ba2、SO42、Ag、NO3、CI、Na。
两厂的污水单独排放都会造成严重的水污染,如将两厂的污水按一定比例混合,沉淀后污水便只含硝酸钠而变成无色澄清,污染程度会大大降低,关于
污染源的分析,你认为正确的是()
A.SO42和NO3可能来自同一工厂
B.CI和NO3一
定不在同一工厂
C.Ag和Na可能来自同一工厂
D.Na和NO3
来自同一工厂
D.NaCI
1.下列物质中,不属于电解质的是()
A.NaOHB.H2SO4C.蔗糖
2.下列物质中,能够导电的是()
A.CO2B.稀盐酸C.蔗糖
D.CuSO4·
5H2O
3.下列叙述中正确的是()
A.固体氯化钠不导电,所以氯化钠不是电解质B