新人教版高中化学必修2第三章有机化合物复习提纲Word文件下载.docx
《新人教版高中化学必修2第三章有机化合物复习提纲Word文件下载.docx》由会员分享,可在线阅读,更多相关《新人教版高中化学必修2第三章有机化合物复习提纲Word文件下载.docx(15页珍藏版)》请在冰豆网上搜索。
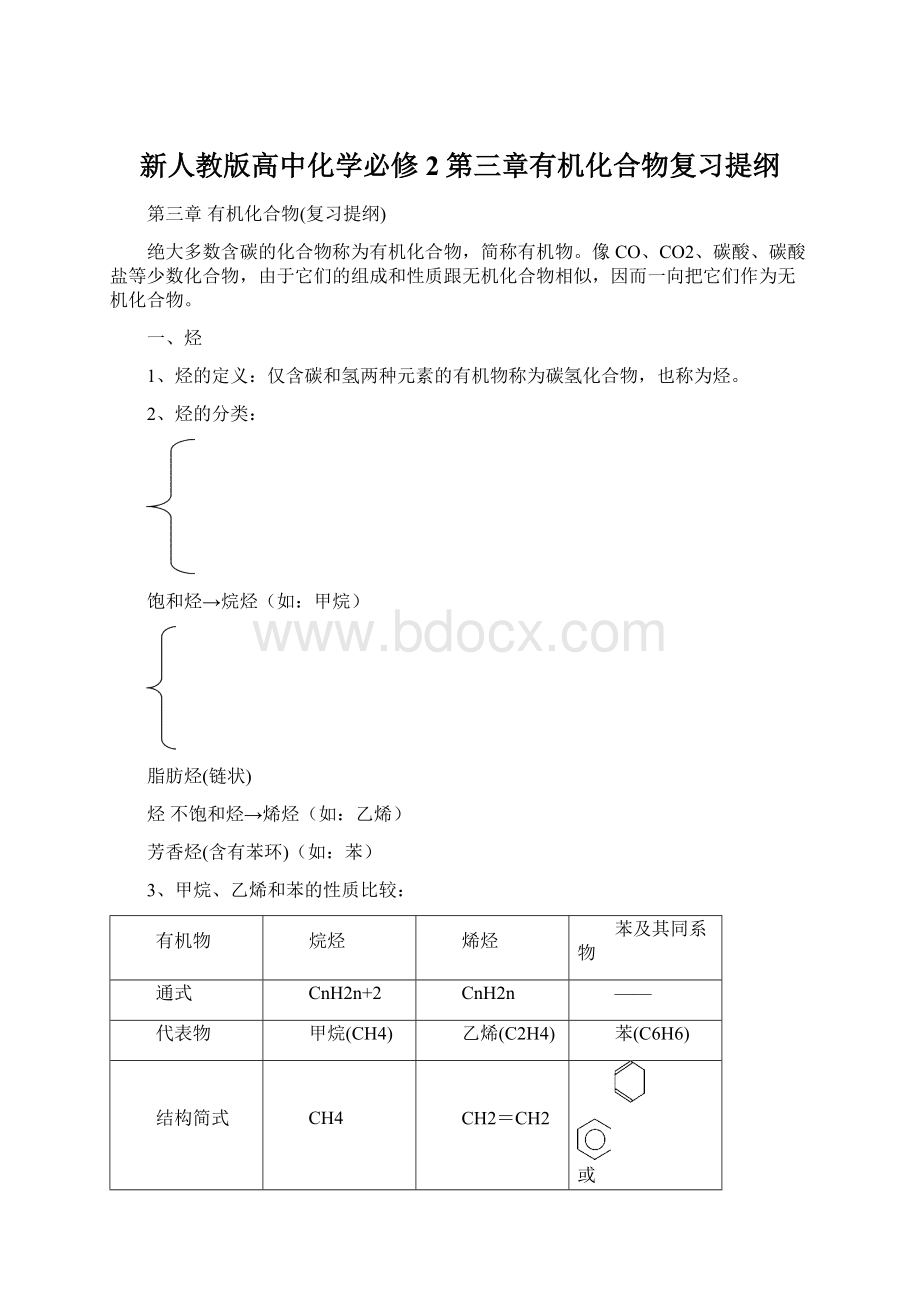
甲烷(CH4)
乙烯(C2H4)
苯(C6H6)
结构简式
CH4
CH2=CH2
或
(官能团)
结构特点
C-C单键,
链状,饱和烃
C=C双键,
链状,不饱和烃
一种介于单键和双键之间的独特的键,环状
空间结构
正四面体
六原子共平面
平面正六边形
物理性质
无色无味的气体,比空气轻,难溶于水
无色稍有气味的气体,比空气略轻,难溶于水
无色有特殊气味的液体,比水轻,难溶于水
用途
优良燃料,化工原料
石化工业原料,植物生长调节剂,催熟剂
溶剂,化工原料
[练习]1.在人类已知的化合物中,品种最多的是()
A.过渡元素的化合物B.第二主族元素的化合物
C.第三主族元素的化合物D.第四主族元素的化合物
2.下列物质属于有机物的是()
A.COB.NaHCO3C.NH4CO3D.CH4
3.下列物质中,属于有机物但不属于烃的是()
A.CO2B.CH3COOHC.Na2CO3D.CH4
4.下列物质不属于饱和链烃的是()
A.CH4B.C3H8C.C4H8D.C5H12
5.以下关于甲烷的说法中错误的是()
A.甲烷分子是由极性键构成的分子B.甲烷分子具有正四面体结构
C.甲烷分子中四个C-H键是完全等价的键D.甲烷分子中具有非极性键
6.下列气体的主要成分不是甲烷的是()
A.沼气B.煤气C.天然气D.坑道气
7.衡量石油化工发展水平的标志是()
A.乙烯产量B.丙烯产量C.汽油产量D.丁二烯产量
主要化学性质
烷烃:
甲烷
①氧化反应(燃烧)
CH4+2O2――→CO2+2H2O(淡蓝色火焰,无黑烟)
②取代反应(注意光是反应发生的主要原因,产物有5种)
CH4+Cl2―→CH3Cl+HClCH3Cl+Cl2―→CH2Cl2+HCl
CH2Cl2+Cl2―→CHCl3+HClCHCl3+Cl2―→CCl4+HCl
在光照条件下甲烷还可以跟溴蒸气发生取代反应,
甲烷不能使酸性KMnO4溶液、溴水或溴的四氯化碳溶液褪色。
烯烃:
乙烯
①氧化反应(ⅰ)燃烧
C2H4+3O2――→2CO2+2H2O(火焰明亮,有黑烟)
(ⅱ)被酸性KMnO4溶液氧化,能使酸性KMnO4溶液褪色。
②加成反应
CH2=CH2+Br2-→CH2Br-CH2Br(能使溴水或溴的四氯化碳溶液褪色)
在一定条件下,乙烯还可以与H2、Cl2、HCl、H2O等发生加成反应
CH2=CH2+H2――→CH3CH3
CH2=CH2+HCl-→CH3CH2Cl(氯乙烷)
CH2=CH2+H2O――→CH3CH2OH(制乙醇)
③加聚反应nCH2=CH2――→-CH2-CH2-n(聚乙烯)
乙烯能使酸性KMnO4溶液、溴水或溴的四氯化碳溶液褪色。
常利用该反应鉴别烷烃和烯烃,如鉴别甲烷和乙烯。
苯
2C6H6+15O2―→12CO2+6H2O(火焰明亮,有浓烟)
②取代反应
苯环上的氢原子被溴原子、硝基取代。
+Br2――→+HBr
+HNO3――→+H2O
③加成反应
+3H2――→
苯不能使酸性KMnO4溶液、溴水或溴的四氯化碳溶液褪色。
[练习]8.不可以用于区别乙烯和乙烷的气体是()
A.苯B.溴水C.酸性高锰酸钾溶液D.溴的四氯化碳溶液
9.在光照条件下,甲烷与氯气反应得到的产物是()
①CH3Cl②CH2Cl2③CHCl3④CCl4
A.只有①B.只有②C.①和②的混合物D.①②③④的混合物
10.聚乙烯是由乙烯(CH2=CH2)通过聚合反应形成的。
下列说法中错误的是()
A.乙烯是不饱和烃B.聚乙烯分子中含有双键
C.聚乙烯中碳的质量分数是85.7%D.聚乙烯制品在自然环境中很难降解
11.等物质的量的甲烷和氯气混合后,在漫射光的照射下充分反应,生成物中的物质的量最大的是()
A.HClB.CH2Cl2C.CH3ClD.CCl4
12.甲烷中混有乙烯,欲除去乙烯得到纯净的甲烷,最好依次通过盛有()试剂的洗气瓶
A.澄清石灰水,浓H2SO4B.酸性KMnO4溶液、浓H2SO4
C.溴水,浓H2SO4D.浓H2SO4,酸性KMnO4溶液
13.1molCH4完全和Cl2发生取代反应,并生成等物质的量的四种氯代物,则需要Cl2的物质的量为()
A.4mol B.3mol C.2.5mol D.0.5mol
14.下列关于苯的性质的叙述中,不正确的是()
A.苯是无色带有特殊气味的液体
B.常温下苯是一种不溶于水且密度比水小的液体
C.苯在一定条件下能与溴发生取代反应
D.苯不具有典型的双键所具有的加成反应的性能,故不可能发生加成反应
15.制取一氯乙烷最好的方法是()
A.乙烷与Cl2反应B.乙烯与Cl2反应
C.乙烯与HCl反应D.乙烯与H2、Cl2反应
16.利用下列反应不能制得括号中的纯净物质的是()
A.乙烯和氯气加成(1,2-二氯乙烷)B.乙烯与水加成(乙醇)
C.等物质的量的氯气与乙烷在光照条件下反应(氯乙烷)
D.氯气与苯用氯化铁作催化剂反应(氯苯)
4、同系物、同分异构体、同素异形体、同位素比较。
概念
同系物
同分异构体
同素异形体
同位素
定义
结构相似,在分子组成上相差一个或若干个CH2原子团的物质
分子式相同而结构式不同的化合物的互称
由同种元素组成的不同单质的互称
质子数相同而中子数不同的同一元素的不同原子的互称
分子式
不同
相同
元素符号表示相同,分子式可不同
结构
相似
研究对象
化合物
单质
原子
[练习]17.有下列几种物质A.金刚石和石墨B.C2H6和C5H12C.C2H4和C2H6
D.CH3CH2CH2CH3和CH3CH(CH3)2F.35Cl和37ClE.
属于同分异构体的是();
属于同素异形体的是();
属于同系物的是();
属于同位素的是();
属于同种物质的是()。
18.下列说法正确的是()
A.C8H16与甲烷互为同系物
B.乙烯只能加成、不能取代,苯只能取代、不能加成
C.CH3CH2CH2CH3和CH3CHCH3互为同分异构体
D.CH3CH2CHCH3和CH3CHCH2CH3互为同分异构体
19.关于烷烃性质的叙述中,不正确的是()
A.烷烃同系物随相对分子质量增大,熔点、沸点逐渐升高;
常温下的状态由气态递变到液态,相对分子质量大的则为固态
B.烷烃同系物的密度随相对分子质量增大逐渐增大
C.烷烃跟卤素单质在光照条件下能发生取代反应
D.烷烃同系物都能使溴水、KMnO4溶液褪色
5、烷烃同分异构体的书写:
(每个碳只能四价)
甲烷、乙烷、丙烷没有同分异构体。
丁烷(有2种同分异构体)戊烷(有3种同分异构体)
[练习]20.某饱和链烃CnH2n+2有同分异构体时的最小值为()
A.5B.4C.3D.2
21.下列化学式只能表示一种物质的是()
A.C3H8B.C4H10C.C5H10D.C7H12
6、烷烃的命名:
(1)普通命名法:
把烷烃泛称为“某烷”,某是指烷烃中碳原子的数目。
1-10用甲,乙,丙,丁,戊,已,庚,辛,壬,癸;
11起汉文数字表示。
区别同分异构体,用“正”,“异”,“新”。
正丁烷,异丁烷;
正戊烷,异戊烷,新戊烷。
(2)系统命名法:
①命名步骤:
(1)找主链-最长的碳链(确定母体名称);
(2)编号-靠近支链(小、多)的一端;
(3)写名称-先简后繁,相同基请合并.
②名称组成:
取代基位置-取代基名称母体名称
③阿拉伯数字表示取代基位置,汉字数字表示相同取代基的个数
CH3-CH-CH2-CH3CH3-CH-CH-CH3
2-甲基丁烷2,3-二甲基丁烷
7、比较同类烃的沸点:
①一看:
碳原子数多沸点高。
②碳原子数相同,二看:
支链多沸点低。
常温下,碳原子数1-4的烃都为气体。
[练习]22.下列物质沸点最低的是()
A.庚烷B.2-甲基丁烷C.正戊烷D.新戊烷
23.城市居民用石油液化气的主要成分是丁烷,在使用过程中常有一些杂质的液态沉积于钢瓶内,这些杂质是()
A.丙烷和丁烷B.乙烷和丙烷C.乙烷和戊烷D.戊烷和己烷
8、烃燃烧通式:
[练习]24.在标准状况下,取等物质的量下列各烃,分别在足量O2中燃烧,消耗O2最多是()
A.CH4B.C2H6C.C2H4D.C3H6
25.某气态烃在密闭容器中与足量的O2混合,用电火花点燃,完全燃烧后,
容器内保持压强不变(120℃),则该烃是()
A.CH4B.C2H6C.C2H4D.C3H6
26.2-甲基丁烷和氯气发生取代反应得到的一氯代物有()
A.3种B.4种C.5种D.6种
二、烃的衍生物
1、乙醇和乙酸的性质比较
饱和一元醇
饱和一元醛
饱和一元羧酸
CnH2n+1OH
CnH2n+1COOH
乙醇
乙醛
乙酸
CH3CH2OH
或C2H5OH
CH3CHO
CH3COOH
官能团
羟基:
-OH
醛基:
-CHO
羧基:
-COOH
无色、有特殊香味的液体,俗名酒精,与水互溶,易挥发
(非电解质)
有强烈刺激性气味的无色液体,俗称醋酸,易溶于水和乙醇,无水醋酸又称冰醋酸。
作燃料、饮料、化工原料;
用于医疗消毒,乙醇溶液的质量分数为75%
有机化工原料,可制得醋酸纤维、合成纤维、香料、燃料等,是食醋的主要成分
①与Na的反应
2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑
乙醇与Na的反应(与水比较):
①相同点:
都生成氢气,反应都放热
②不同点:
比钠与水的反应要缓慢
结论:
乙醇分子羟基中的氢原子比烷烃分子中的氢原子活泼,但没有水分子中的氢原子活泼。
②氧化反应(ⅰ)燃烧
CH3CH2OH+3O2―→2CO2+3H2O
(ⅱ)在