中考化学模拟探究题Word下载.docx
《中考化学模拟探究题Word下载.docx》由会员分享,可在线阅读,更多相关《中考化学模拟探究题Word下载.docx(11页珍藏版)》请在冰豆网上搜索。
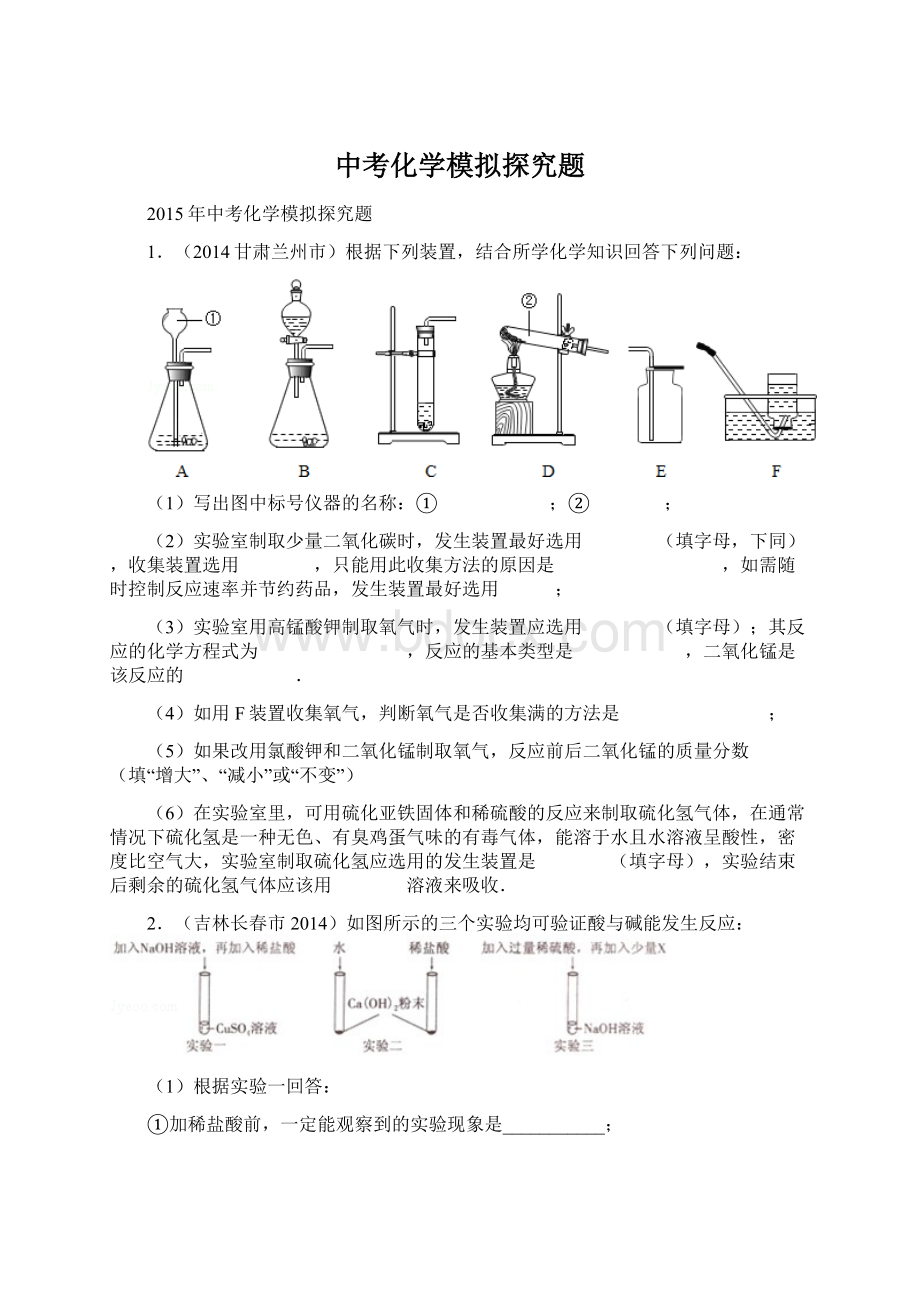
(2)实验二通过两只试管中的现象对比,可以判断稀盐酸与Ca(OH)2能反应,该实验除需控制所加水和稀盐酸的温度、体积相同外,还需控制________________________相同.
(3)实验三中,加入X可验证稀硫酸与碱能发生反应,符合此条件的X是下列物质中的______
A.酚酞B.CuOC.Na2CO3D.Ba(NO3)2.
3.(2014天津市)(9分)某钢铁厂高炉炼铁的主要原料是焦炭、赤铁矿石(主要含Fe2O3)、空气等,主要反应过程如下:
请回答:
(1)A的化学式___________。
(2)反应②的化学方程式。
(3)反应③的化学方程式。
(4)向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,反应停止后过滤,得到滤渣和滤液。
向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有_________(填化学式),滤液中一定含有的溶质是_________(填化学式)。
(5)用含杂质的铁10g(杂质不溶于水,也不参加反应)与100g稀硫酸恰好完全反应,滤去杂质,得到滤液质量为108.1g,则含杂质的铁中铁的质量分数为_________________。
4.(2014北京市)(7分)碳酸钠和碳酸氢钠是生活中常见的盐,通过实验验证、探究它们的化学性质。
【查阅资料】
Na2CO3+CaCO3===CaCO3↓+2NaCl
2NaHCO3Na2CO3+CO2↑+H2O
③Ca(HCO3)2易溶于水。
④CaCl2溶液分别与NaHCO3、Na2CO3溶液等体积混合现象(表中的百分数为溶液中溶质的质量分数):
NaHCO3
Na2CO3
0.1%
1%
5%
CaCl2
无明显现象
有浑浊
xk.Com]
有浑浊,有微小气泡
有沉淀
有浑浊,有大量气泡
【进行实验】
序号
实验装置
主要实验步骤
实验现象
实验1
向2支试管中分别加入少量Na2CO3和NaHCO3溶液,再分别滴加盐酸
2支试管中均有气泡产生
实验2
向Ⅱ中加入试剂a,向Ⅰ中加入少量Na2CO3或NaHCO3固体,分别加热一段时间
Na2CO3受热时Ⅱ中无明显现象
NaHCO3受热时Ⅱ中出现
浑浊
实验3
向Ⅱ中加入试剂a,向Ⅰ中加入少量5%的NaHCO3溶液,再滴加5%的CaCl2溶液
Ⅰ中出现浑浊,有气泡产生Ⅱ中出现浑浊
【解释与结论】
(1)实验1中,NaHCO3与盐酸反应的化学方程式为__________________。
(2)实验2中,试剂a为___________。
(3)实验3中,NaHCO3与CaCl2反应的化学方程式为:
2NaHCO3+CaCl2___________+___________+H2O。
【反思与评价】
(1)实验2中,加热NaHCO3后,试管Ⅰ中残留固体成分可能为______________(写出所有可能)。
(2)资料④中,NaHCO3溶液与CaCl2溶液混合的现象中,有些只观察到浑浊、未观察到气泡,原因可能是______________________。
(3)用2种不同的方法鉴别Na2CO3和NaHCO3固体,实验方案分别为:
①_________________________________。
②_________________________________。
5.(山东烟台2014)(10分)科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环(如图所示)。
某化学小组的同学对此非常感兴趣,在老师的指导下,设计如下装置探究上述设想的反应原理是否可行。
(1)能证明装置A“释放CO2”的现象是;
(2)装置B在实验结束撤掉酒精喷灯时的作用是;
(3)上述反应结束后,小组同学对D中固体的成分进行探究,以证明是否“捕捉”到CO2。
【猜想与假设】
D中的固体可能为:
I.只有氧化钙;
Ⅱ.氧化钙与碳酸钙;
Ⅲ.只有碳酸钙
①甲同学从D中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物。
甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅲ成立。
乙同学认为上述实验不足以证明猜想Ⅲ成立,其理由是。
②乙同学从D中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;
继续向试管中加入几滴稀盐酸,没有发现气泡产生。
乙同学据此认为试管中的固体只有氧化钙,即猜想I成立。
丙同学认为乙的实验不足以证明猜想I成立,理由是_________________________________________________。
③丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和
稀盐酸证明了猜想Ⅱ成立,请完成他的实验报告。
实验步骤
实验结论
猜想Ⅱ成立
(4)通过以上探究,小组同学认为科学家的设想在反应原理上是可行的。
该设想的优点
有(填字母序号)。
A.原料易得B.充分利用太阳能C.释放出的CO2可作为资源加以利用
6.(陕西2013)(4分)
海边盛产贝壳,其主要成分为CaCO3,以贝壳和纯碱为原料,生产烧碱的简要工艺流程如下:
请回答下列问题:
(1)A的化学式是____________。
(2)写出步骤③发生反应的化学方程式________________________。
(3)在工业上,熟石灰可用于生产烧碱。
在农业上,它的一种用途是____________________。
7.(成都市2013中考)(13分)
通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分得到粗盐。
粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。
[提出问题]如何才能将粗盐中难溶性杂质和可溶性杂质(氯化镁、氯化钙)除去,从而获得较纯的食盐晶体?
[资料准备]
[实验方案]某同学为了提纯粗盐,设计了如下实验方案并进行实验。
[交流与表达]
(1)实验步骤①和②的目的是_____________;
实验步骤③和④的目的是_____________。
(2)实验操作X的名称是_____________,该操作中要用到的玻璃仪器有烧杯、玻璃棒和_____________。
(3)实验步骤③的主要目的是_____________(用化学方程式回答);
判断氢氧化钠溶液已过量的方法是__________________________。
(4)实验步骤④中生成的沉淀D是_____________。
(5)实验步骤⑤用蒸发溶剂的方法而不用降低溶液温度的方法获取食盐晶体,原因是__________________________;
在蒸发食盐溶液的过程中要使用玻璃棒,作用是__________________________。
[反思与评价]
(6)有同学认为只需要用氢氧化钠溶液和碳酸钠溶液中任意一种试剂就能将两种可溶性杂质除去,你认为这种方法__________________________(选填“可行”或“不可行”),理由是_______________________________________。
(7)有同学认为原实验方案不完善,做出这种评价的依据是__________________________。
[实验方案设计]
(8)为了完善原实验方案,你设计的实验是_______________________________________
______________________________________(仅写出补充部分的实验操作和现象)
8.(2013黄冈)(7分)
小东、小林和小雨同学对氢氧化钠溶液使酚酞溶液变红的现象很感兴趣,决定做实验进行探究:
氢氧化钠溶液中到底是哪一种粒子使酚酞溶液变红?
实验中可供使用的用品有盐酸、氯化钠溶液、氯化钙溶液、氢氧化钠溶液、碳酸钠溶液、酚酞溶液及若干支试管。
【提出假设】假设
(1):
使酚酞溶液变红的是H2O。
假设
(2):
使酚酞溶液变红的是Na+。
假设(3):
使酚酞溶液变红的是________。
小东认为不做实验即可说明假设
(1)不成立,原因是___________________。
【实验验证】
(完成下列实验操作、实验现象及实验结论)
小雨认为向实验步骤
(1)后的试管中加入盐酸也可得出正确结论,你同意她的观点吗?
_________(填“同意”或“不同意”)。
【实验拓展】
小林将酚酞溶液滴入碳酸钠溶液中,发现溶液也变红。
他们经过分析、讨论、归纳,得出的结论是_______________________。
9、(四川雅安中学2015诊断)(本题7分)某校化学兴趣小组经查阅资料得知:
铝是重要的轻金属,广泛应用于航空、电讯和建筑等领域。
铝也有其特殊的性质:
①铝的熔点是660℃,氧化铝的熔点高达2054℃。
②铝虽比锌活泼,但是将铝和锌分别投入稀硫酸中,铝比锌反应慢得多。
③尽管铝表面致密的氧化膜能使铝与其周围的介质(空气、水)隔绝,但“奇怪”的是铝制容器仍不能用来盛放和腌制咸菜。
为此该小组进行了“铝表面氧化膜”的探究实验,其过程如下,请完成填空:
【实验1】用坩埚钳夹住一块擦去氧化膜的铝片,放在酒精灯火焰上灼烧,铝片表面接触火焰的部分变暗片刻后变软;
轻轻摇动,会左右摇晃,却不像蜡烛那样滴落。
问题:
(1)请写出在空气中灼烧铝片的化学方程式;
(2)铝片接触火焰的部分不像蜡烛那样滴落的原因是
。
【实验2】取2条未用砂纸打磨过的铝片,一片浸入CuCl2稀溶液中,其表面很快析出较多红色粉末状固体;
而另一片浸入CuSO4稀溶液中现象一直不明显。
试猜测产生这种现象差异的因素是
【实验3】用砂纸打磨一铝片使其表面较粗糙,再将其放入CuSO4稀溶液中,直到2-3分钟后,铝片表面才有少量红色固体附着。
试写出铝片表面附着红色固体的化学方程式:
;
【实验4】向实验2的CuSO4稀溶液中滴入3-5滴NaCl稀溶液,铝片表面逐渐有红色固体析出。
【实验5】向实验2的CuSO4稀溶液中滴入3-5滴Na2SO4稀溶液,铝片表面现象一