2 第30讲 生活中两种常见的有机物和基本营养物质Word文件下载.docx
《2 第30讲 生活中两种常见的有机物和基本营养物质Word文件下载.docx》由会员分享,可在线阅读,更多相关《2 第30讲 生活中两种常见的有机物和基本营养物质Word文件下载.docx(18页珍藏版)》请在冰豆网上搜索。
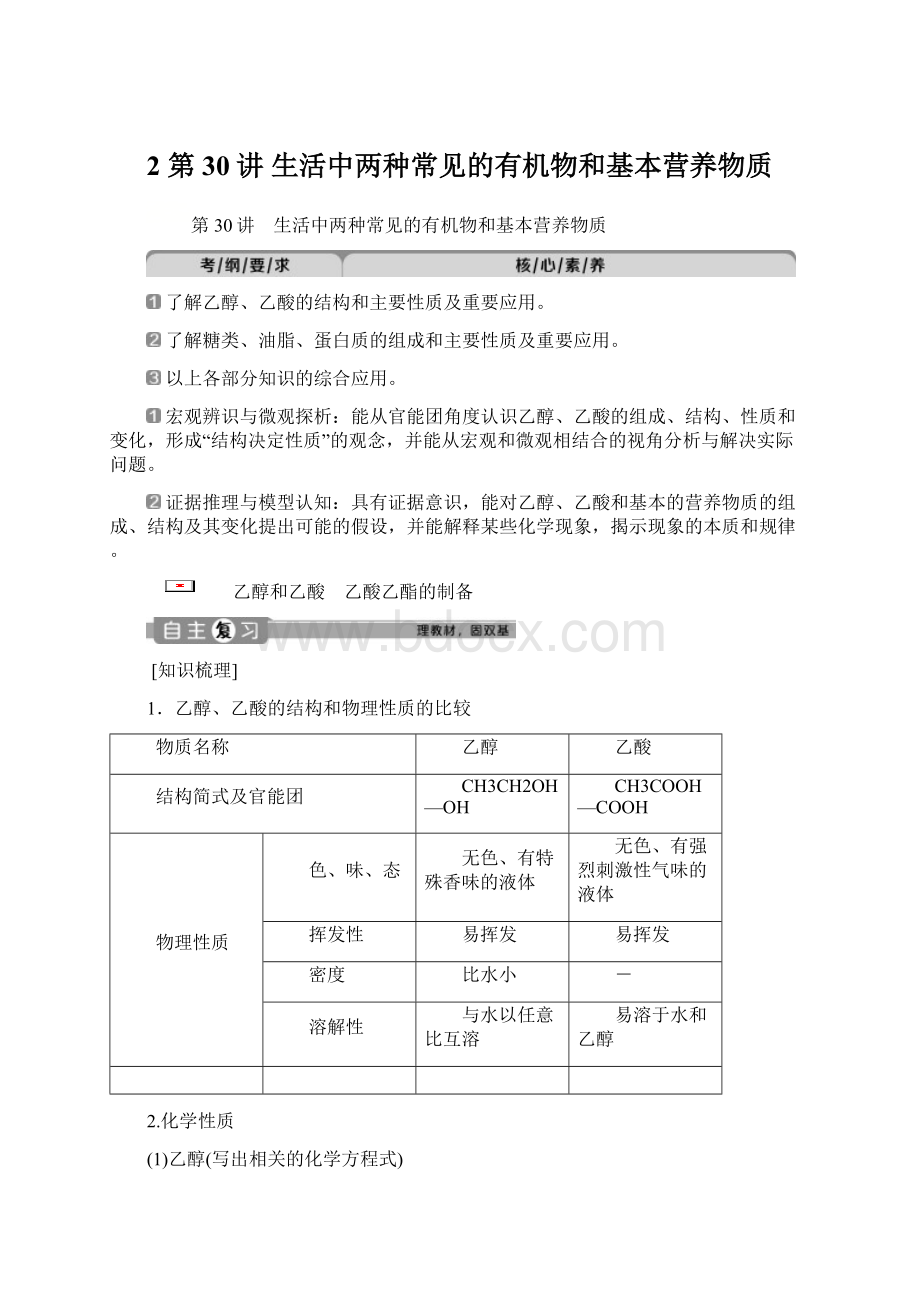
易挥发
密度
比水小
-
溶解性
与水以任意比互溶
易溶于水和乙醇
2.化学性质
(1)乙醇(写出相关的化学方程式)
(2)乙酸(写出相关的化学方程式)
3.乙酸乙酯的制取
(1)实验原理
CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O。
其中浓硫酸的作用为催化剂和吸水剂。
(2)反应特点
(3)装置(液液加热反应)及操作
①试管向上倾斜45°
,试管内加入少量碎瓷片,长导管起冷凝回流和导气的作用。
②试剂的加入顺序为乙醇、浓硫酸、乙酸,不能先加浓硫酸。
③要用酒精灯小火均匀加热,以防止液体剧烈沸腾及乙酸和乙醇大量挥发。
(4)饱和Na2CO3溶液的作用及现象
①作用:
降低乙酸乙酯的溶解度、消耗乙酸、溶解乙醇。
②现象:
在饱和Na2CO3溶液上方出现有香味的油状液体。
(5)提高乙酸乙酯产率的措施
①用浓硫酸吸水;
②加热将酯蒸出;
③适当增加乙醇的用量。
(6)乙酸乙酯的水解反应
在酸性或碱性条件下均可发生水解反应。
CH3COOC2H5+H2OCH3COOH+C2H5OH(可逆)
CH3COOC2H5+NaOHCH3COONa+C2H5OH(完全)
[自我检测]
判断正误(正确的打“√”,错误的打“×
”)。
(1)(2017·
高考全国卷Ⅱ,10B)乙醇和水都可与金属钠反应产生可燃性气体,说明乙醇分子中的氢与水分子中的氢具有相同的活性。
( )
(2)(2017·
高考全国卷Ⅱ,10C)用乙酸浸泡水壶中的水垢,可将其清除,说明乙酸的酸性小于碳酸的酸性。
(3)(2016·
高考全国卷Ⅰ,7D)医用消毒酒精中乙醇的浓度为95%。
(4)(2016·
高考上海卷)CH3COOH溶液与Zn反应放出H2,能证明乙酸是弱酸。
(5)乙醇、乙酸与Na2CO3均能反应产生CO2。
(6)向乙酸溶液中滴入几滴紫色石蕊溶液,溶液变红。
(7)乙醇与乙酸中均含有—OH,所以均能与Na反应生成氢气。
(8)制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸。
(9)可以用分液漏斗分离乙酸乙酯和乙醇。
(10)乙酸和乙酸乙酯可用饱和Na2CO3溶液加以区别。
答案:
(1)×
(2)×
(3)×
(4)×
(5)×
(6)√ (7)√ (8)×
(9)×
(10)√
演练一 乙醇和乙酸的性质
1.(2019·
哈尔滨高三模拟)下列关于乙醇和乙酸的说法错误的是( )
A.乙醇和乙酸均可发生取代反应
B.乙醇和乙酸均可与钠反应,二者水溶液均呈酸性
C.乙醇在一定条件下可直接氧化生成乙酸
D.可用新制氢氧化铜悬浊液鉴别乙醇和乙酸
解析:
选B。
乙醇和乙酸可发生酯化反应,该反应属于取代反应,A说法正确;
乙醇的水溶液呈中性,B说法错误;
乙醇可被强氧化剂如酸性KMnO4溶液直接氧化生成乙酸,C说法正确;
Cu(OH)2可溶于乙酸生成蓝色溶液,与乙醇不反应,因此可用新制氢氧化铜悬浊液鉴别乙醇和乙酸,D说法正确。
2.(2019·
南宁模拟)山西老陈醋素有“天下第一醋”的盛誉。
食醋中含有乙酸,下列关于乙酸的说法中错误的是( )
A.乙酸分子中含有4个氢原子,但乙酸是一元酸
B.往食醋溶液中滴入紫色石蕊溶液,溶液将变红
C.往热水瓶内胆中加入适量的食醋,可去除水垢
D.制取乙酸乙酯时,乙酸分子中的氢原子被乙基(—C2H5)取代
选D。
酯化反应原理是羧酸分子中的羟基被醇中的烃基取代,D错误。
3.乳酸的结构简式为,下列有关乳酸的说法不正确的是( )
A.乳酸中能发生酯化反应的官能团有2种
B.1mol乳酸可与2molNaOH发生中和反应
C.1mol乳酸与足量金属Na反应生成1molH2
D.有机物与乳酸互为同分异构体
乳酸中含有的官能团是羟基和羧基,都能发生酯化反应,所以A正确;
1mol乳酸只含有1mol羧基,只能和1molNaOH发生中和反应,而羟基不参加反应,所以B错误;
羧基和羟基都可以和Na反应生成氢气,所以C正确;
与乳酸分子式相同,结构不同,二者互为同分异构体,所以D正确。
1.乙酸、水、乙醇、碳酸分子中羟基氢的活泼性比较
物质类别
水
碳酸
分子结构
CH3COOH
H—OH
C2H5OH
与羟基直接相连的原子或原子团
H—
C2H5—
遇石蕊溶液
变红
不变红
变浅红
与Na
反应
与Na2CO3溶液
水解
不反应
羟基氢的活泼性强弱
CH3COOH>
H2CO3>
H2O>
CH3CH2OH
2.乙醇的化学性质与羟基的关系
(1)与Na反应时,只断裂a处键。
(2)乙醇催化氧化时,断裂a和c两处键,形成碳氧双键。
(3)乙醇和乙酸发生酯化反应时,只断裂a处键。
演练二 乙酸乙酯的制备与酯化反应的拓展
4.(2016·
高考上海卷)乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用a装置来制备。
完成下列填空:
(1)实验时,通常加入过量的乙醇,原因是______________________________________
________________________________________________________________________。
加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是__________________
________________________________;
浓硫酸用量又不能过多,原因是________________________________________________________________________
(2)饱和Na2CO3溶液的作用是____________、____________、________________________。
(3)反应结束后,将试管中收集到的产品倒入分液漏斗中,________、________,然后分液。
(4)若用b装置制备乙酸乙酯,其缺点有____________、________________。
由b装置制得的乙酸乙酯粗产品经饱和碳酸钠溶液和饱和食盐水洗涤后,还可能含有的有机杂质是________,分离乙酸乙酯与该杂质的方法是______________。
(1)由于浓硫酸具有强氧化性和脱水性,会使有机物碳化,降低酯的产率,所以浓硫酸用量不能过多。
(2)由于生成的乙酸乙酯中含有乙醇和乙酸,所以饱和Na2CO3溶液的作用是中和乙酸、溶解乙醇、减少乙酸乙酯在水中的溶解。
(3)乙酸乙酯不溶于饱和碳酸钠溶液,因此反应结束后,将试管中收集到的产品倒入分液漏斗中,振荡、静置,然后分液即可。
(4)根据b装置可知由于不是水浴加热,温度不易控制,因此用b装置制备乙酸乙酯的缺点是原料损失较大、容易发生副反应。
由于乙醇发生分子间脱水生成乙醚,所以由b装置制得的乙酸乙酯产品经饱和碳酸钠溶液和饱和食盐水洗涤后,还可能含有的有机杂质是乙醚,乙醚与乙酸乙酯的沸点相差较大,则分离乙酸乙酯与乙醚的方法是蒸馏。
(1)增大反应物浓度,使平衡向生成酯的方向移动,提高酯的产率(答案合理即可) 浓H2SO4能吸收生成的水,使平衡向生成酯的方向移动,提高酯的产率 浓硫酸具有强氧化性和脱水性,会使有机物碳化,降低酯的产率
(2)中和乙酸 溶解乙醇 减少乙酸乙酯在水中的溶解
(3)振荡 静置
(4)原料损失较大 易发生副反应 乙醚 蒸馏
5.(教材改编)某课外兴趣小组欲在实验室里制备少量乙酸乙酯,该小组的同学设计了以下四个制取乙酸乙酯的装置,其中正确的是( )
选A。
B和D中导管插入试管b内液面以下,会引起倒吸,C和D中试管b中的NaOH溶液会与生成的乙酸乙酯反应。
6.1丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如下图,下列对该实验的描述错误的是( )
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.加入过量乙酸可以提高1丁醇的转化率
选C。
该酯化反应需要的温度为115~125℃,水浴的最高温度为100℃,A项正确;
长导管可以起到冷凝回流酸和醇的作用,B项正确;
乙酸丁酯在氢氧化钠溶液中容易发生水解,C项错误;
在可逆反应中,增加一种反应物的用量可以提高另一种反应物的转化率,D项正确。
有机实验中应注意的问题
(1)加热方面
①用酒精灯加热:
教材中的实验需要用酒精灯加热的有乙烯的制备、乙酸乙酯的制备、蒸馏石油的实验、石蜡的催化裂化实验。
②水浴加热:
银镜反应(温水浴)、乙酸乙酯的水解(70~80℃水浴)、蔗糖的水解(热水浴)。
(2)蒸馏操作中应注意的事项
温度计的水银球位于蒸馏烧瓶的支管口处;
烧瓶中加碎瓷片防暴沸;
冷凝管一般选用直形冷凝管,冷凝剂的流动方向与被冷凝的液体的流动方向应相反。
(3)冷凝回流问题
当需要使被汽化的物质重新流回到反应容器中时,可通过在反应容器的上方添加一个长导管达到此目的(此时空气是冷凝剂);
若需要冷凝的试剂沸点较低,则需要在容器的上方安装冷凝管,常选用球形冷凝管,此时冷凝剂的方向是下进上出。
(4)在有机制备实验中利用平衡移动原理,提高产品的产率常用的方法:
①及时蒸出或分离出产品;
②用吸收剂吸收其他产物,如水;
③利用回流装置,提高反应物的利用率;
④增加其中一种反应物的用量。
基本营养物质——糖类、油脂、蛋白质
1.糖类、油脂、蛋白质的化学组成
有机物
元素组成
代表物
代表物分子式或分子组成
水溶性
糖类
单糖
C、H、O
葡萄糖、果糖
C6H12O6
易溶于水
双糖
麦芽糖、蔗糖
C12H22O11
多糖
淀粉、纤维素
(C6H10O5)n
油脂
油
植物油
不饱和高级脂肪酸甘油酯
不溶
脂肪
动物脂肪
饱和高级脂肪酸甘油酯
蛋白质
C、H、O、N、S、P等
酶、肌肉、毛发等
氨基酸连接成的高分子
淀粉和纤维素尽管可用一个化学式表示,但其中的n值不定,所以淀粉和纤维素不是同分异构体。
2.糖类、油脂、蛋白质的性质
特征反应
水解反应
葡萄糖
葡萄糖有银镜产生
有砖红色沉淀产生