高考化学铝及其化合物推断题综合题Word文档格式.docx
《高考化学铝及其化合物推断题综合题Word文档格式.docx》由会员分享,可在线阅读,更多相关《高考化学铝及其化合物推断题综合题Word文档格式.docx(15页珍藏版)》请在冰豆网上搜索。
【解析】
【分析】
铝土矿中含有氧化铝和氧化铁,向铝土矿中加入NaOH溶液,发生反应Al2O3+2OH-═2AlO2-+H2O,氧化铁不溶,然后过滤,得到溶液B为NaOH、NaAlO2混合溶液,沉淀C为Fe2O3;
向溶液B中通入CO2,发生反应2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-、2OH-+CO2=CO32-+H2O,然后过滤得到沉淀Al(OH)3和Na2CO3溶液,向溶液中加入CaO,发生反应Na2CO3+CaO+H2O═2NaOH+CaCO3↓,然后过滤,将NaOH循环利用;
将Al(OH)3加热得到Al2O3,电解熔融Al2O3得到Al,据此分析解答。
【详解】
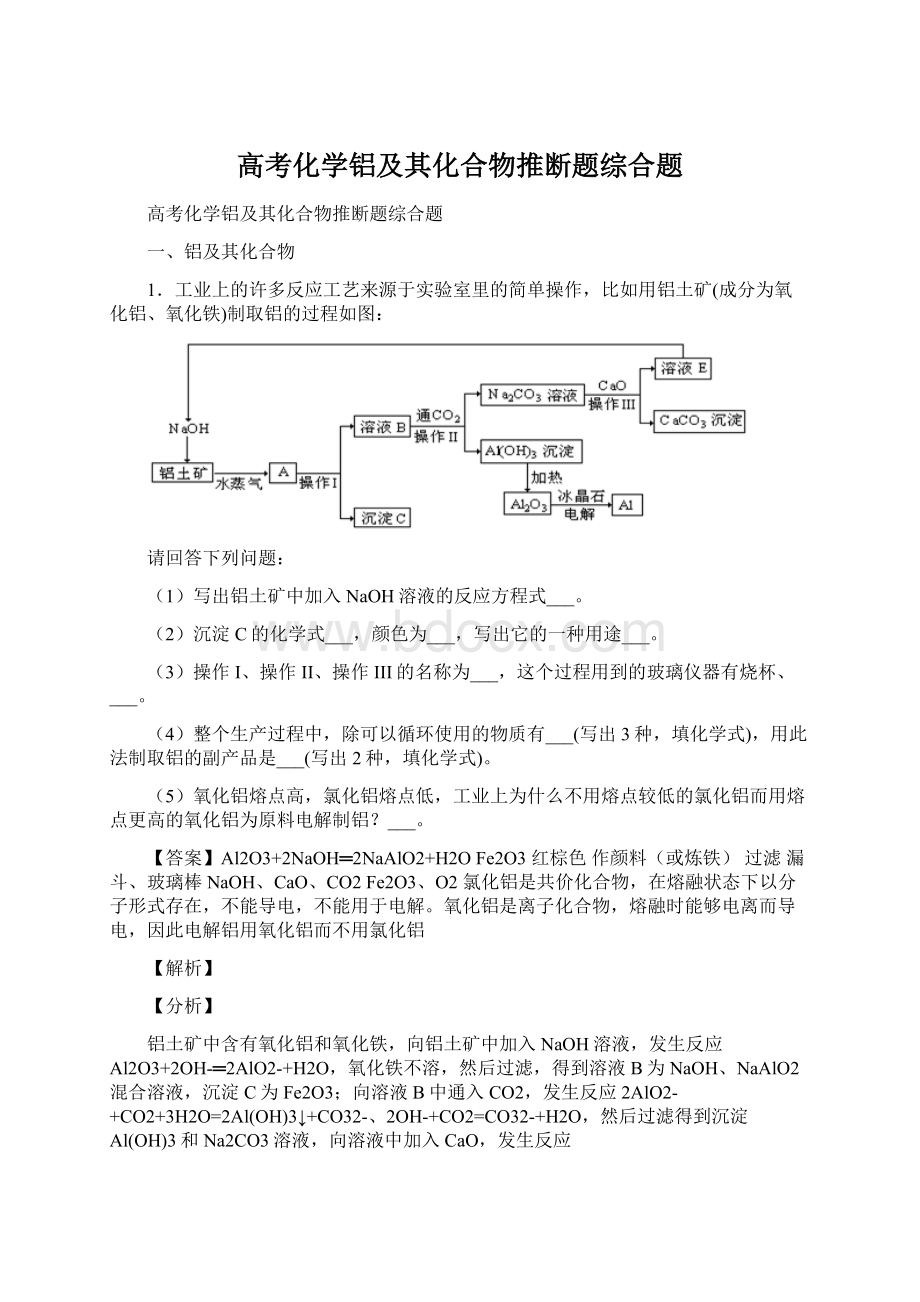
(1)根据上面的分析,铝土矿中加入NaOH溶液,氧化铝与氢氧化钠反应生成偏铝酸钠,反应的化学方程式为Al2O3+2NaOH═2NaAlO2+H2O,故答案为:
Al2O3+2NaOH═2NaAlO2+H2O;
(2)根据上述分析,沉淀C为Fe2O3,氧化铁为红棕色粉末,俗称铁红,除了用于金属冶炼以外,还可用作顔料,故答案为:
Fe2O3;
红棕色、作颜料(或炼铁);
(3)实现固体和液体的分离采用过滤法,操作Ⅰ、操作Ⅱ和操作Ⅲ都是过滤操作,过滤时需要制作过滤器的漏斗、固定仪器的铁架台、引流用的玻璃棒、承接滤液的烧杯,故答案为:
过滤;
漏斗、玻璃棒;
(4)煅烧碳酸钙得到CaO和CO2,B生成沉淀需要二氧化碳、碳酸钠转化为碳酸钙需要CaO,所以CaO和CO2能循环利用,溶液E中的氢氧化钠也能循环利用;
根据流程图和上述分析,操作Ⅰ所得的Fe2O3和电解熔融Al2O3得到的O2为副产品,故答案为:
NaOH、CaO和CO2;
Fe2O3和O2;
(5)氯化铝是共价化合物,在熔融状态下以分子形式存在,不能导电,不能用于电解。
氧化铝是离子化合物,熔融时能够电离而导电,因此尽管氧化铝熔点高,氯化铝熔点低,工业上电解铝时选用氧化铝而不用氯化铝,故答案为:
氯化铝是共价化合物,在熔融状态下以分子形式存在,不能导电,不能用于电解。
氧化铝是离子化合物,熔融时能够电离而导电,因此电解铝用氧化铝而不用氯化铝。
2.下列物质A-F是我们熟悉的单质或化合物,其中A、B均是常见的金属,且B的合金用量最大;
E在常温下是黄绿色气体;
适当的条件下,它们之间可以发生如图所示的转化。
(1)G溶液中溶质的化学式为_____________。
(2)请写出反应D→F的化学方程式:
_________。
(3)检验F中金属阳离子的常用试剂是______________(填物质的化学式);
现象是____________。
(4)E物质可与石灰乳反应制取漂白粉,写出漂白粉的有效成分_________。
(5)写出C与过量氢氧化钠溶液反应的离子方程式_______________。
(6)若向D溶液中滴加氢氧化钠溶液,现象是:
____,反应过程中的化学方程式为:
____,______。
【答案】NaAlO22FeCl2+Cl2=2FeCl3KSCN溶液呈血红色Ca(ClO)2Al3++4OH-=AlO2-+2H2O先产生白色沉淀,后白色沉淀变为灰绿色,最后变为红褐色FeCl2+2NaOH=Fe(OH)2↓+2NaCl4Fe(OH)2+O2+2H2O=4Fe(OH)3
B的合金用量最大,所以B为Fe;
E在常温下是黄绿色气体,所以E为Cl2;
盐酸与铁反应生成FeCl2,FeCl2与Cl2反应生成的F为FeCl3;
金属A与盐酸反应后生成的盐,与适量的NaOH溶液反应能生成白色沉淀,白色沉淀还能溶于NaOH,所以A为Al单质,C为AlCl3溶液,G为NaAlO2溶液。
(1)根据分析可知,G即为偏铝酸钠溶液,溶质的化学式为NaAlO2;
(2)根据分析可知,D为FeCl2,与E即Cl2反应后生成FeCl3,方程式为:
;
(3)检验Fe3+常用硫氰化钾溶液,Fe3+遇SCN-生成血红色物质;
(4)漂白粉中的有效物质为次氯酸钙;
(5)通过分析可知,C为AlCl3溶液,与过量的NaOH溶液反应,生成偏铝酸钠和水,离子方程式为:
(6)通过分析可知,D的溶液为FeCl2溶液,FeCl2会与NaOH溶液反应生成很不稳定的白色Fe(OH)2沉淀,沉淀会迅速的被氧化为Fe(OH)3,转化的现象为:
白色沉淀先转变为灰绿色,最终变为红褐色;
相关的方程式还有:
3.回答下列问题:
(1)锂和镁在元素周期表中有特殊“对角线”关系,它们的性质相似。
下列有关锂及其化合物的叙述正确的是________。
ALi2SO4难溶于水
BLi与N2反应产物是Li3N
CLiOH易溶于水
DLiOH与Li2CO3受热都难分解
(2)与铝位于对角线位置的第二周期元素是________,能区别Be(OH)2和Mg(OH)2的一种试剂是________,反应的化学方程式是_________。
(3)门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下空位。
例如,他预测在铝的下方有一个与铝类似的元素“类铝”,后来被法国化学家于1875年发现,命名为镓。
镓的元素符号是________,它在周期表中的位置是___________。
(4)关于与镓同主族的第6周期元素性质的推测中不正确的是________。
A单质是银白色较软的金属
B其氢氧化物是两性氢氧化物
C在化合物中显+3价
D单质与盐酸的反应比铝剧烈
【答案】B铍(Be)NaOH溶液Be(OH)2+2NaOH=Na2BeO2+2H2OGa第四周期ⅢA族B
(1)A.锂和镁在元素周期表中有特殊“对角线”关系,它们的性质非常相似,硫酸镁易溶于水,所以硫酸锂易溶于水,故A错误;
B.锂和镁在元素周期表中有特殊“对角线”关系,它们的性质非常相似,镁和氮气反应生成氮化镁,所以锂和氮气反应生成Li3N,故B正确;
C.氢氧化镁难溶于水,所以氢氧化锂属于难溶物质,故C错误;
D.锂和镁在元素周期表中有特殊“对角线”关系,它们的性质非常相似,氢氧化镁和碳酸镁受热易分解,则氢氧化锂和碳酸锂受热也易分解,故D错误;
故答案为B;
(2)根据对角线规则,与铝位于对角线位置的第二周期元素是铍,有相似的化学性质,氢氧化铝具有两性,Be(OH)2也具有两性,可以与氢氧化钠反应,Mg(OH)2不可以与氢氧化钠反应,故可以用氢氧化钠来鉴别,类比氢氧化铝与氢氧化钠反应的化学方程式,则氢氧化铍与氢氧化钠反应的化学方程式为:
Be(OH)2+2NaOH=Na2BeO2+2H2O;
(3)同主族元素性质相似,铝下方的元素为镓,其元素符号为Ga,位于元素周期表中第四周期ⅢA族;
(4)A.与镓同主族的第六周期元素为铊,单质为银白色,质软,故A正确;
B.氢氧化物为两性的物质位于金属和非金属的临界处,如硼铝硅锗砷等,铊不是两性物质,其氢氧化物也不是两性氢氧化物,故B错误;
C.铊与铝同主族,具有相同的最外层电子数,所以铊在化合物中也显+3价,故C正确;
D.同主族元素自上到下金属性递增,该元素金属性大于铝,其单质与盐酸的反应比铝剧烈,故D正确;
故答案为B。
【点睛】
考查位置结构性质的相互关系应用,明确同主族元素性质的递变规律为解答关键,注意掌握对角线规则内容,结合Mg、Al单质及其化合物的性质,类推未知物的性质,试题侧重培养学生的分析、理解能力及知识的迁移能力。
4.有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。
E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;
E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:
(1)五种元素的名称:
A________,B________,C________,D________,E________。
(2)画出C原子、A离子的结构示意图:
__________________、__________________。
(3)B单质在D单质中燃烧,反应现象是_______________________,生成物的化学式为_____________________。
(4)A与E形成化合物的化学式为______________,它的性质决定了它在物质的分类中应属于__________________。
(5)向D与E形成的化合物的水溶液中滴入烧碱溶液直至无明显现象发生时,观察到的现象是先有白色胶状沉淀产生并逐渐增多,随NaOH加入又逐渐溶解最终澄清,请写出有关反应的离子方程式为_______________________、___________________________________________。
【答案】氧磷硫氯铝白色烟雾PCl3、PCl5Al2O3两性氧化物Al3++3OH-=Al(OH)3↓Al(OH)3+OH-=AlO2-+2H2O
A、B、C、D、E五种短周期元素,由位置图可知,A在第二周期,B、C、D处于第三周期,设C的质子数为x,则A的质子数为x-8,B的质子数为x-1,D的质子数为x+1,A、B、C、D四种元素原子核外共有56个电子,则x+(x-8)+(x-1)+(x+1)=56,解得x=16,即A为O,B为P,C为S,D为Cl;
1molE单质与足量酸作用,在标准状况下能产生33.6LH2,设E的化合价为y,根据电子转移守恒:
1mol×
y=×
2×
1,解得y=3,E的阳离子与A的阴离子核外电子层结构完全相同,则E为Al,据此解答。
(1)由上述分析,可知A为氧、B为磷、C为硫、D为氯、E为铝;
(2)C为硫,S原子核外有16个电子,三个电子层,各层电子数为2、8、6,原子结构示意图为:
A为氧,O2-离子核外电子数为10,有2个电子层,各层电子数为2、8,离子结构示意图为:
(3)磷单质在氯气中燃烧三氯化磷和五氯化磷,生成物的化学式为:
PCl3是液体、PCl5是固体,反应现象是:
有白色烟雾生成;
(4)A与E形成的化合物为氧化铝,化学式为Al2O3,能与酸、碱反应生成盐与水,属于两性氧化物;
(5)D与E形成的化合物为AlCl3,向AlCl3的水溶液中逐渐滴入烧碱溶液直至过量,发生Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O,则可观察到先有白色胶状沉淀产生并逐渐增多,随NaOH加入又逐渐溶解最终澄清。
5.某混合溶液中可能大量含有的离子如下表所示:
阳离子
H+、K+、