中考化学酸碱盐专题复习学生版梁+薛Word下载.docx
《中考化学酸碱盐专题复习学生版梁+薛Word下载.docx》由会员分享,可在线阅读,更多相关《中考化学酸碱盐专题复习学生版梁+薛Word下载.docx(23页珍藏版)》请在冰豆网上搜索。
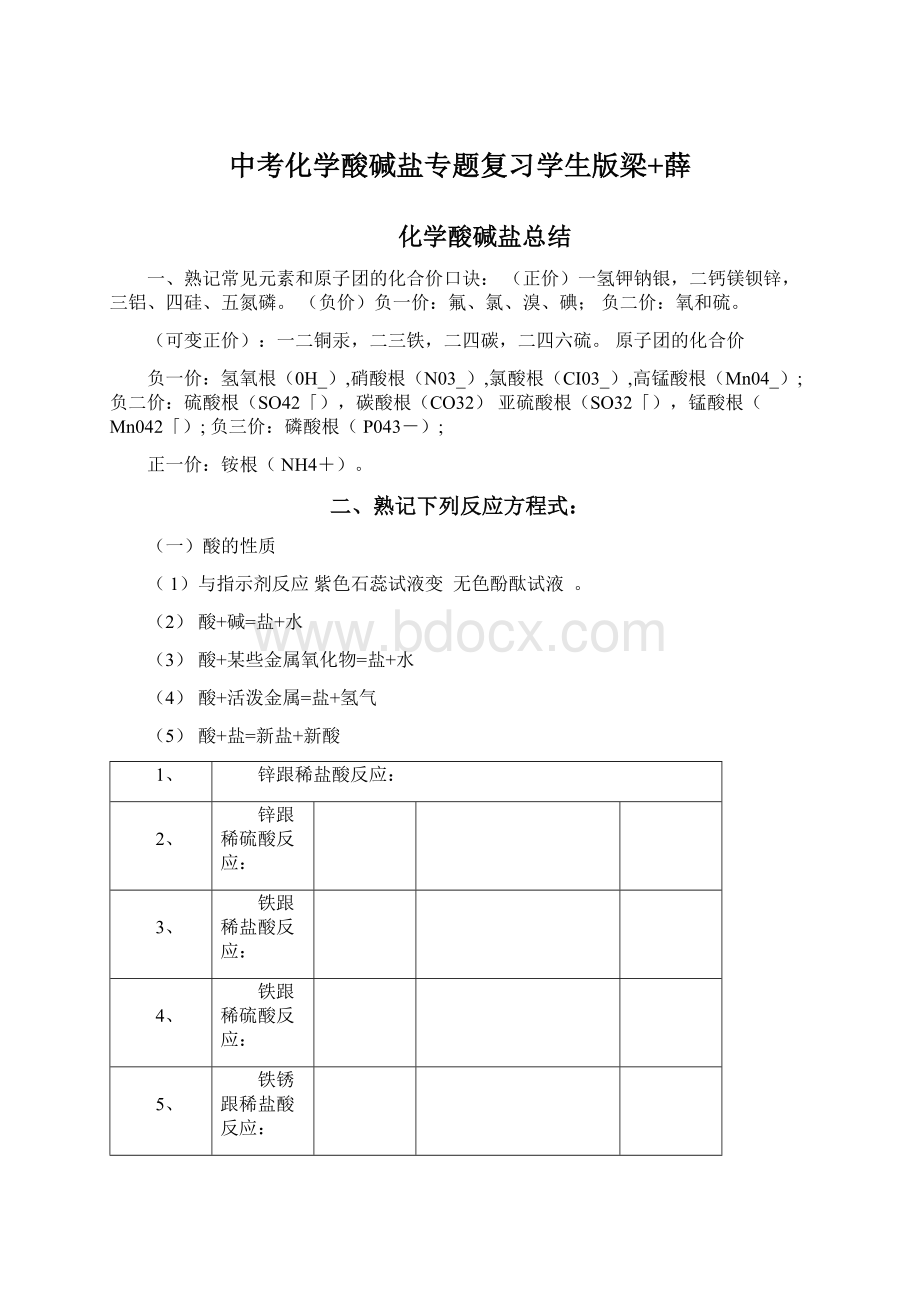
(4)酸+活泼金属=盐+氢气
(5)酸+盐=新盐+新酸
1、
锌跟稀盐酸反应:
2、
锌跟稀硫酸反应:
3、
铁跟稀盐酸反应:
4、
铁跟稀硫酸反应:
5、
铁锈跟稀盐酸反应:
6、
铁锈跟稀硫酸反应:
7、
氧化铜跟稀盐酸反应:
8、
氧化铜跟稀硫酸反应:
(二
)碱的性质:
(1)
碱溶液能使紫色石蕊试液变_
___无色酚酞试液
。
(2)
碱+多数非金属氧化物=
盐+水
(3)
碱+酸=盐+水
(4)
碱+某些盐=另一种盐+
另一种碱
氢氧化钠跟二氧化碳反应:
氢氧化钠跟稀硫酸反应:
氢氧化钠跟二氧化硫反应:
氢氧化钠跟稀盐酸反应:
氢氧化钠跟三氧化硫反应:
生石灰跟水反应:
氢氧化钙跟二氧化碳反应:
(三)盐的性质:
(1)盐+某些金属二另一种盐+另一种金属
(2)盐+某些酸=另一种盐+另一种酸。
(3)盐+某些碱=另一种盐+另一种碱
(4)盐+某些盐=另一种盐+另一种盐
1、硫酸铜溶液跟铁反应:
2、碳酸钠跟盐酸反应:
3、碳酸氢钠跟盐酸反应:
4、石灰石跟稀盐酸反应:
5、硝酸银跟稀盐酸反应:
6、氯化钡跟稀硫酸反应:
7、氢氧化钙根碳酸钠溶液反应:
8、硝酸银溶液跟氢氧化钠溶液反应:
9、氯化钡溶液跟硫酸钠溶液反应:
三、金属活动性顺序表:
KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu
四、溶解性表:
(1)大多数酸可溶(HCl、HNO3、H2CO3有挥发性、浓H2SO4有吸水性。
)
(2)碱的溶解性:
钾、钠、钡、铵溶、钙微溶,其余碱全不溶。
(3)盐的溶解性:
钾、钠、铵、硝四盐溶。
氯化物除AgCl不溶外,其余全溶。
硫酸盐除BaS04不溶,Ag2SO4、CaSCh微溶外,其余全溶。
碳酸盐除钾、钠、铵盐全溶、MgCO3微外,其余全不溶。
五、反应条件:
1、复分解反应的条件——生成物中有沉淀析出,或有气体放出,或有水生成
2、金属跟酸反应的条件——
(1)在金属活动性顺序表中,金属要排在氢前。
(2)浓硫酸、硝酸跟金属反应不能生成氢气。
(3)铁发生置换反应时,生成+2价的铁的化合物。
3、金属跟盐反应的条件——
(1)在金属活动性顺序表中,单质的金属要比盐中金属活泼。
(2)反应物中的盐要可溶。
(3)K、Ca、Na、Ba等金属跟盐反应不能生成另一种盐和另一种金属。
4、盐跟盐反应的条件——反应物都要可溶,生成物要有沉淀。
5、盐跟碱反应的条件——反应物都要可溶,生成物要有沉淀或气体。
六、熟记常见物质的俗称和化学式:
熟石灰——Ca(OH)2纯碱、苏打——Na2CO3赤铁矿——Fe3O4冰——H2O醋酸(乙酸)
食盐——NaCl
小苏打——NaHCO3金刚石、石墨——C天然气(甲烷)——CH4
红色的固体——Cu、Fe2O3、P(红磷)黑色的固体——C、CuO、FesO4、FeO、MnO2
白色的固体——KCIO3、P2O5、P(白磷)、CuSO4(无水硫酸铜)、KCl、NaCl等暗紫色的固体——KMnO4黄色的固体——S
蓝色的固体——CuSO4•5H2O蓝色絮状沉淀——Cu(OH)2
红褐色絮状沉淀——Fe(OH)3常见不溶于酸的白色沉淀——BaSO4、AgCI
溶于酸并放出使澄清石灰水变浑浊的气体的白色沉淀一一BaCO3、CaCO3等不溶性碳酸盐沉淀
溶于酸但不产生气体的白色沉淀——Mg(OH)2、AI(OH)3等不溶性碱的沉淀
蓝色的溶液——CuSC4、CuCl2、Cu(NO3)2等含Cu2+溶液
浅绿色的溶液一一FeSC4、FeCl2等含Fe2十溶液
黄色的溶液——FeC3、Fe2(SO4)3、Fe(NO3)3等含Fe3*溶液
八、物质的检验和鉴别:
1、检验稀盐酸(或C「)一一取少量待检液体于洁净的试管中,滴入几滴AgNO3溶液和稀HNO3,有白色沉淀产生。
2、检验稀硫酸(或SO42「)一一取少量待检液体于洁净的试管中,滴入几滴BaCl2溶液和稀HNO3,有白色沉淀产生。
3、检验CO32-――取少量待检液体于洁净的试管中,滴入几滴稀HCI,有使澄清石灰水变浑浊的气体产生。
4、检验NH4+――取少量待检物于洁净的试管中,滴入适量NaOH溶液并加热,有使湿的红色石蕊试纸变成蓝色的气体产生。
5、鉴别稀盐酸和稀硫酸一一分别取少量待检液体于两支洁净的试管中,各滴入几滴BaCl2溶液,有白色沉淀产生的原溶液是稀硫酸,无现象产生的原溶液是稀盐酸。
6鉴别Ca(OH)2和NaOH溶液一一分别取少量待检液体于两支洁净的试管中,分别通入CO2
气体(或各滴入几滴Na2CO3溶液),有白色沉淀产生的原溶液是Ca(OH)2,无现象产生的原溶液是NaOH。
◎补充下列反应方程式:
1、氢氧化铜跟稀盐酸反应:
Cu(OH)2+2HCl=CuCl2+2H2O蓝色沉淀消失
2、氢氧化铜跟稀硫酸反应:
Cu(OH)2+H2SO4=CuSO4+2H2O变成蓝色溶液
3、氢氧化钠跟硫酸铜溶液反应:
2NaOH+CuSO4=Na2SO4+Cu(OH)2J有蓝色沉淀产生
4、氢氧化钠跟氯化铁溶液反应:
3NaOH+FeCb=Fe(OH)3;
+3NaCl有红褐色沉淀产生
◎判断溶液的酸碱性
用指示剂,溶液的酸碱度用pH来表示。
I£
3456T8yJu111J14
1111111
j1e11a1
中性k
豔性増强瑕性増強
紫色石蕊无色酚酞
pH<
7为酸性显红色显无色
pH=7为中性显紫色显红色
pH>
7为碱性显蓝色显红色
◎干燥剂的选择:
1、浓硫酸可干燥:
酸性气体(如:
C02、S02、SO3、N02、HCl、)中性气体(如:
H2、02、N2、C0)
※不能干燥碱性气体(如:
NH3)
2、氢氧化钠固体、生石灰、碱石灰可干燥:
碱性气体(如:
NH3)中性气体(如:
※不能干燥酸性气体(如:
C02、S02、S03、N02、HCl、)
3、无水硫酸铜固体遇水由白色变蓝色,可检验水的存在,并吸收水蒸气
酸碱盐中考试题
1.分类是学习化学的方法之一,下列物质是按单质、盐、混合物的顺序排列的是
A.氧气、碳酸钙、空气
溶液
盐酸
CuCl2溶液
Na2SO4溶液
水
Na2CO3溶液
NaOH溶液
pH「
<
7
=7
>
2.某同学在实验室测定了几种溶液的
pH,其结果如下表:
该同学由此得出的结论正确的是
(
)
4.下列物质露置于空气中,没有发生化学变化而质量增大的是(
A.浓硫酸B.浓盐酸C.生石灰D.氢氧化钠
段时间后,质量减小的是()
C.浓盐酸D.氢氧化钠
C.稀硫酸与氯化钡溶液混合得白色沉淀
D.浓硫酸倒入水中,溶液温度会降低
9.根据学科实验现象,可以判断其溶液一定呈酸性的是()
A.滴加酚酞试液显红色的溶液B.滴加石蕊试液显蓝色的溶液
C.能够与碱发生反应的溶液
D.常温下,pH<
7的溶液
10.稀盐酸和稀硫酸具有相似的化学性质,其本质原因是()
A.都能与指示剂作用B.都能解离出酸根离子
C.都能解离出氢离子
D.都含有氢元素
11.下面是某同学进行碱的化学性质实验时记录的实验现象,其中与事实不相符的是
A.在Ca(OH)2溶液中加入稀盐酸,无明显变化
B.在NaOH溶液中通入CO2气体,有白色沉淀生成
C.在Ca(OH)2溶液中加入几滴石蕊溶液,溶液呈蓝色
D.在NaOH溶液中加入CuSO4溶液,有蓝色沉淀生成
12.物质的性质决定其用途。
下列物质的用途与性质对应关系错误的是(
A.氢氧化钙可用来改良酸性土壤----氢氧化钙溶液呈碱性
B•氮气常用作保护气----氮气化学性质稳定
C•固体二氧化碳可用人工降雨----二氧化碳能与碱反应
D.氧化钙可做食品干燥剂----氧化钙能与水反应
13•下列实验方法无法.达到实验目的的是()
A•用肥皂水鉴别硬水和软水B•用燃着的木条鉴别氮气与二氧化碳
14.推理是化学学习中常用的思维方法,下列推理正确的是()
A.分子是构成物质的微粒,物质都是由分子构成的
B.氧化物一定含氧元素,含氧元素的物质一定是氧化物
C.中和反应生成盐和水,生成盐和水的反应一定是中和反应
D.碱性较强的溶液能使酚酞溶液变红,能使酚酞溶液变红的溶液一定呈碱性
15.逻辑推理是化学学习中常用的思维方法。
下列推理正确的是()
A.中和反应生成盐和水,则生成盐和水的反应一定是中和反应
B•化合物是由不同种元素组成的纯净物。
所以由不同种元素组成的纯净物一定是化合物
C.单质中只含有一种元素,所以只含有一种元素的物质一定是单质
D•活泼金属能与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属
16•观察和实验是学习科学的重要方式,下列实验中观察到的颜色正确的是()
A.铁锈放入稀盐酸中溶液变黄色
B.酚酞试液滴入硫酸溶液中变红色
C.硫在氧气中燃烧发出微弱的淡蓝色火焰
D.硫酸铜溶液中滴加氢氧化钠溶液出现红褐色絮状沉淀
17•某NaOH固体样品,可能含有固体KOH和不溶于酸的杂质A,取5.6g该样品与100g一定质量分数的稀盐酸反应,两者恰好完全反应,生成mg水。
下列说法正确的是()
A.若样品不含任何杂质,则m<
1.8
B.若m=1.8,则样品中一定含有杂质A,可能含有固体KOH
C.若m=1.8,则样品中至少含有杂质A或固体KOH的一种
D•若样品中不含A,则盐酸的溶质质量分数不小于7.3%
18.对于复分解反应:
X+2NaOH—2Y+Cu(OH)2j,下列分析中正确的是()
A.X一定是CuCl2B.相对分子质量大小:
X>
Y
C.Y可能是H20
D.Y可能是Na2SO4