高考化学一轮复习 镁铝铁铜 金属的冶炼Word格式文档下载.docx
《高考化学一轮复习 镁铝铁铜 金属的冶炼Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《高考化学一轮复习 镁铝铁铜 金属的冶炼Word格式文档下载.docx(13页珍藏版)》请在冰豆网上搜索。
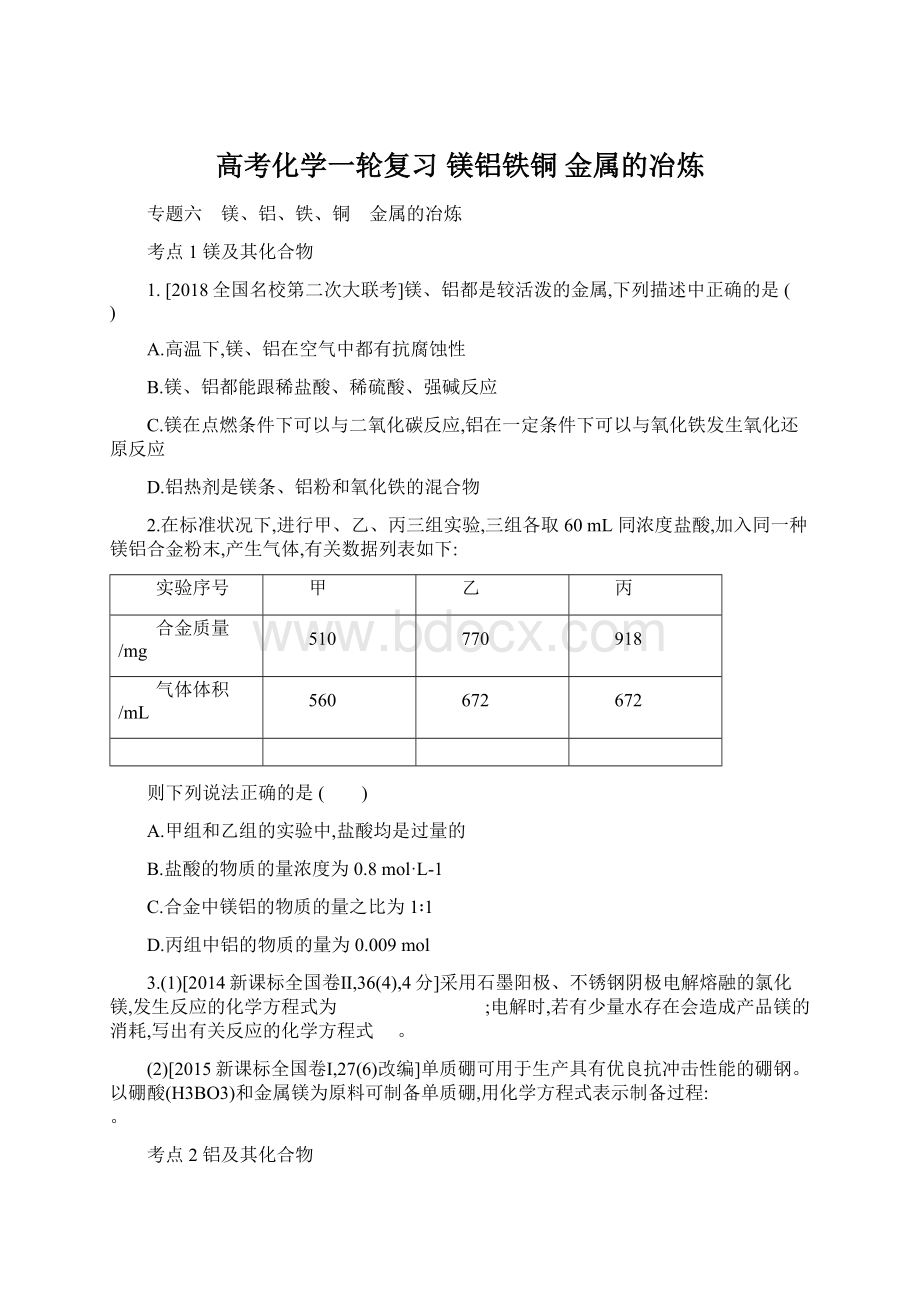
560
672
则下列说法正确的是( )
A.甲组和乙组的实验中,盐酸均是过量的
B.盐酸的物质的量浓度为0.8mol·
L-1
C.合金中镁铝的物质的量之比为1∶1
D.丙组中铝的物质的量为0.009mol
3.
(1)[2014新课标全国卷Ⅱ,36(4),4分]采用石墨阳极、不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为 ;
电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式 。
(2)[2015新课标全国卷Ⅰ,27(6)改编]单质硼可用于生产具有优良抗冲击性能的硼钢。
以硼酸(H3BO3)和金属镁为原料可制备单质硼,用化学方程式表示制备过程:
。
考点2铝及其化合物
4.下列关于铝的说法中正确的有( )
①铝制容器可盛装热的浓硫酸 ②工业上电解熔融状态AlCl3制备Al ③常温下将Al片放入浓硝酸中无明显变化,说明Al与浓硝酸不反应④铝镁合金可完全溶解于烧碱溶液中 ⑤氧化铝和氧化镁都可以作耐火材料
A.1个 B.2个 C.3个 D.4个
5.[2016上海,20,4分]已知NaOH+Al(OH)3Na[Al(OH)4]。
向集满CO2的铝制易拉罐中加入过量NaOH浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;
再过一段时间,罐壁又重新凸起。
上述实验过程中没有发生的离子反应是( )
A.CO2+2OH-C+H2O
B.Al2O3+2OH-+3H2O2[Al(OH)4]-
C.2Al+2OH-+6H2O2[Al(OH)4]-+3H2↑
D.Al3++4OH-[Al(OH)4]-
6.铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的HCl和NaOH的物质的量之比为( )
A.3∶1 B.2∶1 C.1∶1 D.1∶3
7.[2014北京理综,7,6分]下列金属中,表面自然形成的氧化层能保护内层金属不被空气氧化的是( )
A.KB.NaC.FeD.Al
8.向MgSO4、(NH4)2SO4和Al2(SO4)3的混合溶液中,逐滴加入NaOH溶液。
下列图像中,能正确表示上述反应的是(x轴表示加入NaOH溶液的体积,y轴表示反应生成沉淀的质量)( )
A B
CD
9.利用铝热反应可以焊接钢轨。
下列说法正确的是( )
A.铝、氧化铝中铝原子、铝离子的半径r(Al)>
r(Al3+)
B.工业上可用铝热反应的方法制取镁
C.在铝热反应中,化学能全部转化为光能
D.在铝热反应中,铁的还原性大于铝的还原性
10.[2015广东理综,32,16分]七铝十二钙(12CaO·
7Al2O3)是新型的超导材料和发光材料。
用白云石(主要含CaCO3和MgCO3)和废Al片制备七铝十二钙的工艺如下:
(1)煅粉主要含MgO和 。
用适量NH4NO3溶液浸取煅粉后,镁化合物几乎不
溶,若滤液Ⅰ中c(Mg2+)小于5×
10-6mol·
L-1,则溶液pH大于 [Mg(OH)2的Ksp=5×
10-12];
该工艺中不能用(NH4)2SO4代替NH4NO3,原因是 。
(2)滤液Ⅰ中的阴离子有 (忽略杂质成分的影响);
若滤液Ⅰ中仅通入CO2,会生成 ,从而导致CaCO3产率降低。
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为 。
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,电解总反应方程式为 。
(5)一种可超快充电的新型铝电池,充放电时AlC和Al2C两种离子在Al电极上相互转化,其他离子不参与电极反应。
放电时负极Al的电极反应式为 。
11.[2018合肥调研检测]在给定条件下,下列物质的转化不能实现的是( )
A.Fe2O3FeCl3溶液无水FeCl3
B.饱和NaCl溶液NaHCO3Na2CO3
C.Al2O3NaAlO2溶液Al(OH)3
D.MgCl2溶液Mg(OH)2MgO
12.[2016海南,14,8分]KAl(SO4)2·
12H2O(明矾)是一种复盐,在造纸等方面应用广泛。
实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如图所示。
回答下列问题:
(1)为尽量少引入杂质,试剂①应选用 (填标号)。
a.HCl溶液b.H2SO4溶液c.氨水d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为 。
(3)沉淀B的化学式为 ;
将少量明矾溶于水,溶液呈弱酸性,其原因是
。
(4)已知:
Kw=1.0×
10-14,Al(OH)3Al+H++H2O K=2.0×
10-13。
Al(OH)3溶于NaOH溶液反应的平衡常数等于 。
考点3铁及其化合物
13.向FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是( )
A.加入KSCN溶液可能变红色
B.溶液中一定含Fe2+
C.溶液中可能含有Cu2+
D.剩余固体中一定含Cu
14.[2016全国卷Ⅱ,28,15分]某班同学用如下实验探究Fe2+、Fe3+的性质。
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol·
L-1的溶液。
在FeCl2溶液中需加入少量铁屑,其目的是 。
(2)甲组同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。
FeCl2溶液与氯水反应的离子方程式为 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是 。
(4)丙组同学取10mL0.1mol·
L-1KI溶液,加入6mL0.1mol·
L-1FeCl3溶液混合。
分别取2mL此溶液于3支试管中进行如下实验:
①第一支试管中加入1mLCCl4充分振荡、静置,CCl4层显紫色;
②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是 (填离子符号);
实验①和③说明:
在I-过量的情况下,溶液中仍含有 (填离子符号),由此可以证明该氧化还原反应为 。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为 ;
一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。
产生气泡的原因是 ;
生成沉淀的原因是
(用平衡移动原理解释)。
15.用下面两种方法可以制得白色的Fe(OH)2沉淀。
Ⅰ.方法一:
用FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)除去蒸馏水中溶解的O2常采用 的方法。
(2)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。
这样操作的理由是 。
Ⅱ.方法二:
在如图所示装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。
(1)在试管Ⅰ里加入的试剂是 。
(2)在试管Ⅱ里加入的试剂是 。
(3)为了制得白色Fe(OH)2沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是 。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是 。
16.甲、乙、丙三位同学欲分别完成“铁与水蒸气反应”的实验。
Ⅰ.甲同学的方案如图1:
试管中依次放入湿棉花和还原性铁粉,加热。
把生成的气体通入蒸发皿中的肥皂液中,用坩埚钳夹取燃着的火柴在蒸发皿中点火,观察到的现象是 ;
发生反应的化学方程式为 。
Ⅱ.乙同学所采用的装置如图2:
分别用灯1和灯2加热反应器中的水和还原性铁粉,当水蒸气将空气排出后用排水法收集一试管气体。
乙同学所采用的装置与甲同学的装置相比较,优点是 ;
结束实验的操作是 。
Ⅲ.丙同学将甲、乙两位同学所用装置进行改进,如图3所示:
在硬质玻璃管Ⅰ中放入还原性铁粉和石棉绒的混合物,硬质玻璃管Ⅱ中加入CuO。
干燥管Ⅰ中盛装的物质是碱石灰,干燥管Ⅱ中盛装的物质是无水硫酸铜和石棉绒的混合物。
(1)丙同学所采用的装置与乙同学的装置相比较,优点是
。
(2)实验开始时应先点燃a处的酒精灯,然后才点燃b处的酒精喷灯,原因是 。
(3)能证明铁与水蒸气反应的现象是 。
考点4铜及其化合物
17.[2018湖南师大附中模拟]CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。
下列说法不正确的是( )
A.相对于途径①,途径②更好地体现了绿色化学思想
B.Y可以是葡萄糖溶液
C.CuSO4在1100℃分解所得气体X是SO2和SO3的混合气体
D.将CuSO4溶液蒸发浓缩、冷却结晶可制得胆矾晶体
18.[2013广东理综,32,15分]银铜合金广泛用于航空工业。
从切割废料中回收银并制备铜化工产品的工艺如下:
[注:
Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃]
(1)电解精炼银时,阴极反应为 ;
滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学反应方程式为 。
(2)固体混合物B的组成为 ;
在生成固体B的过程中,需控制NaOH的加入量。
若NaOH过量,则因过量引起的反应的离子方程式为 。
(3)完成煅烧过程中一个反应的化学方程式:
CuO+ Al2O3 CuAlO2+ ↑。
(4)若银铜合金中铜的质量分数为63.5%,理论上5.0kg废料中的铜可完全转化为 molCuAlO2,至少需要1.0mol·
L-1的Al2(SO4)3溶液 L。
(5)CuSO4溶液也可用于制备胆矾,其基本操作是 、过滤、洗涤和干燥。
考点5金属材料与金属矿物的开发利用合金
19.下列有关合金的说法正确的是( )
A.合金中至少含有两种金属
B.合金的熔点比成分金属的高
C.合金的硬度比成分金属的小
D.青铜器所用材料属于合金
20.[2013重庆理综,8,14分]合金是建造航空母舰的主体材料。
(1)航母升降机可由铝合金制造。
①铝元素在周期表中的位置为 。
工业炼铝的原料由铝土矿提取而得,提取过程中通入的气体为 。
②Al-Mg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为 。
焊接过程中使用的保护气为 (填化学式)。
(2)航母舰体材料为合金钢。
①舰体在海水中发生的电化学腐蚀主要为