中考化学沪教版专题复习图表线类试题Word下载.doc
《中考化学沪教版专题复习图表线类试题Word下载.doc》由会员分享,可在线阅读,更多相关《中考化学沪教版专题复习图表线类试题Word下载.doc(7页珍藏版)》请在冰豆网上搜索。
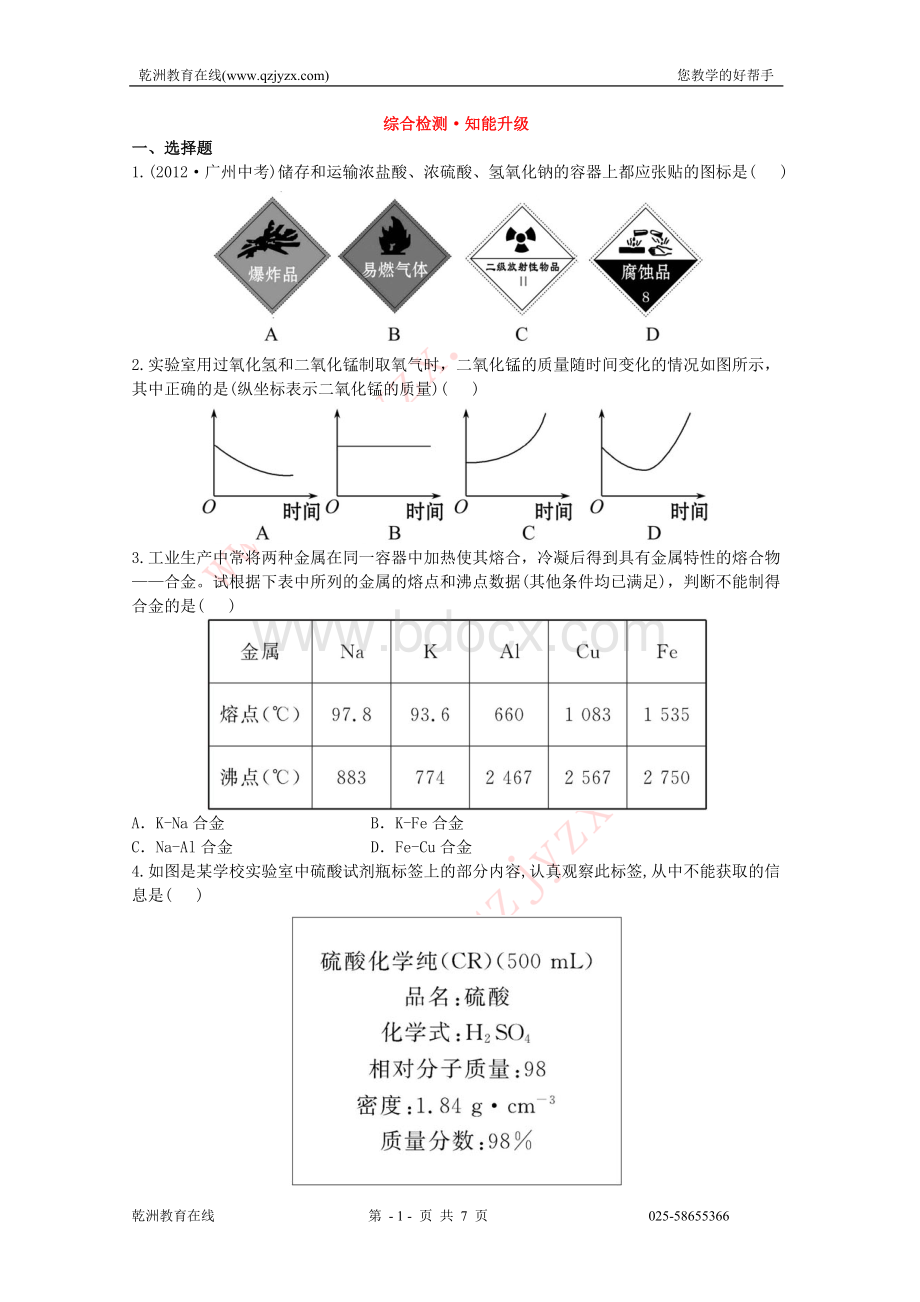
D.硫酸中硫元素的质量分数
5.(2012·
潍坊中考)在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。
则关于此反应的认识正确的是()
A.该反应用化学方程式表示为:
3X+Y====2Z+W
B.该反应的基本类型为复分解反应
C.m=1
D.反应后容器中Z与Y的质量比为1∶6
6.(2011·
江西中考)有等质量的A、B两种金属,相对原子质量Ar(A)<
Ar(B)。
将A放入质量分数为15%的稀硫酸中,B放入质量分数为15%的稀盐酸中,在反应中A、B均显正二价,产生氢气的质量随时间变化曲线如图所示。
下列说法正确的是()
A.产生氢气的速率A<
B
B.反应后A、B一定都有剩余
C.消耗的稀硫酸和稀盐酸质量一定不相等
D.消耗B的质量一定小于消耗A的质量
7.氯化铵和硝酸钾溶解度曲线如图所示,下列叙述正确的是()
A.60℃时,硝酸钾的溶解度小于氯化铵的溶解度
B.40℃的硝酸钾饱和溶液降低温度会变为不饱和溶液
C.t℃时,氯化铵饱和溶液与硝酸钾饱和溶液的溶质的质量分数相等
D.60℃时,100g水中加入120g硝酸钾,充分搅拌,得到的是硝酸钾不饱和溶液
8.(2012·
连云港中考)下列图像与对应的叙述相符合的是()
A.等质量的铁片、铝片分别与足量且质量分数相同的稀硫酸反应
B.向H2SO4和MgSO4的混合溶液中滴加NaOH溶液
C.向pH=13的氢氧化钠溶液中不断加水稀释
D.化学反应中,原子总数随时间的变化
二、非选择题
9.根据如图衣服标签回答下列问题:
(1)面料中的棉属于_______(填“天然”或“合成”,下同)有机高分子材料,面料中的涤纶属于_________有机高分子材料。
(2)合成纤维有下列哪三个优点________(填字母)。
A.强度高、弹性好
B.耐磨
C.吸水性、透气性较好
D.耐化学腐蚀
10.(2011·
眉山中考)如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。
据图回答:
(1)P点的含义是___________________________________________。
(2)t1℃时30g的a物质加入到50g水中不断搅拌,能形成80g溶液吗?
__________(填“能”或“不能”)。
(3)t2℃时,a、b、c三种物质的溶解度按由小到大的顺序排列的是__________
(填物质序号)。
11.(2012·
怀化中考)未成年人和老年人是需要补钙的主要人群,目前市面上有许多补钙的钙片出售。
如图是盖中盖高钙片的部分说明,某课外兴趣小组欲检验说明的真伪,进行了如下实验:
①取1片片剂研碎
②将其加入足量稀盐酸中
③完全反应后收集到0.55g二氧化碳
试分析:
(1)未成年人缺钙会得_________(填序号)。
A.坏血症B.贫血
C.佝偻病D.甲状腺肿大
(2)通过计算判断此钙片中钙含量与标注是否属实。
(假定钙片中其他成分不与盐酸反应,1g=1000mg)
12.(2011·
金华中考)氢气还原氧化铜实验得到的固体粉末为氧化铜和铜的混合物,科学兴趣小组的同学对该粉末中单质铜的含量进行测定。
三组同学各取10克粉末样品置于烧杯中,然后加入不同质量的同浓度的稀硫酸,充分反应后,对烧杯中剩余固体进行称量,实验数据记录如下:
(1)分析表中数据可知,第2组实验中的剩余固体是_________(写出物质名称或符号)。
(2)样品中单质铜的质量分数为_________。
(3)加入的稀硫酸的溶质质量分数是多少?
(写出计算过程)
答案解析
1.【解析】选D。
本题考查一些与安全相关的常见图标。
关键是要弄清浓盐酸、浓硫酸、氢氧化钠所具有的共性。
三种物质都不是爆炸品,不是易燃气体,不具有放射性,但都具有腐蚀性,故选D。
2.【解析】选B。
二氧化锰的质量在反应前后没有变化,不会减少或增多。
3.【解析】选B。
合金是两种或两种以上的金属或金属跟非金属熔合而成的具有金属特性的物质,在合金中一种金属的熔点应低于另一种金属的沸点才能使两种金属熔合在一起。
由表中的各金属的熔点、沸点可知A、C、D项的两种金属均可制得合金,B选项中铁的熔点(1535℃)比钾的沸点(774℃)还高,所以当铁熔化时,钾已经气化,无法熔合,因此B选项中铁和钾不能制得合金。
4.【解析】选A。
由题中商标信息可知,该硫酸溶液的密度(即其物理性质)是
1.84g·
cm-3;
根据硫酸的化学式(H2SO4)可以计算出其中各元素的质量比及硫酸中硫元素的质量分数,但其中没有给出化学性质的信息。
5.【解析】选C。
本题以表格数据为信息考查质量守恒定律的相关内容。
根据容器中反应前后的质量可判断生成X的质量是15g,参加反应的Z的质量是10g,参加反应的W的质量是5g,根据质量守恒定律推出Y反应后质量为1g,所以Y既不是反应物又不是生成物,因此,选项A、B不正确,C正确,反应后容器中Z与Y的质量比为6∶1,D不正确。
6.【解析】选C。
本题通过坐标图考查金属与酸反应时,生成氢气量的多少及反应速率知识。
(1)识标:
图中横坐标表示的是反应时间,纵坐标表示的是生成氢气的质量,即表示等质量的A、B两种金属与相同质量分数的硫酸、盐酸反应时生成氢气的质量随反应时间的变化而变化的关系;
(2)明点:
图像中A的转折点在B前,说明反应结束时A需要的时间短,产生氢气的速率A>
B;
(3)析线:
反应结束时,A、B两金属的转折点在同一水平线上,说明反应结束时,两金属生成氢气质量相等,由于相对原子质量Ar(A)<
Ar(B),并且化合价一样,要生成相同质量的氢气,消耗金属的质量B应大于A,故两种金属不一定都有剩余;
相同质量,相同浓度的盐酸与硫酸完全反应生成氢气的量是不同的,而题中生成氢气的质量相等,故只有C是正确的。
7.【解析】选C。
观察溶解度曲线可知,60℃时硝酸钾的溶解度为110g,大于氯化铵的溶解度,A、D错误;
因硝酸钾的溶解度随温度的升高而增大,故对其饱和溶液降温时将析出晶体,剩余的液体仍是饱和溶液,B错;
t℃时硝酸钾与氯化铵的溶解度曲线相交于一点,所以此时二者的溶解度相等,此温度下二者的饱和溶液的溶质质量分数也一定相等,C正确。
8.【解析】选D。
铝的活泼性大于铁,所以单位时间内铝产生的氢气质量大于铁,故A错;
向H2SO4和MgSO4的混合溶液中滴加NaOH溶液时,NaOH溶液先和H2SO4反应,只有溶液变成中性时,NaOH溶液才和MgSO4反应生成沉淀,故B错;
向碱溶液中加水,碱性减弱,pH会减小,但只能是接近于7,不会小于7,C错;
根据质量守恒定律,在化学反应中,原子的种类、数目、质量都不会改变,故D正确。
9.【解析】
(1)棉是没有经过人工合成加工、能直接从自然界获取的高分子材料,属于天然有机高分子材料。
涤纶是以石油为原料,经过化学加工而得,因此属于合成有机高分子材料;
(2)有机合成材料强度高、耐磨、抗腐蚀性能好,但透气性差,吸水性差,且不易溶于水。
答案:
(1)天然合成
(2)A、B、D
10.【解析】溶解度曲线中交点的意义为:
相应温度下,两者的溶解度相等;
t1℃时,a物质的溶解度是20g,即该温度下,100g水中最多能溶解20g的a物质;
由三种物质的溶解度曲线可知,t2℃时,a、b、c三种物质的溶解度按由小到大的顺序排列的是c<b<a。
(1)在t1℃时,a、c的溶解度相等
(2)不能(3)c、b、a
11.【解析】本题属于信息题,通过对题目信息的分析,考查化学元素与人体健康的关系及化学方程式的有关计算。
(1)未成年人缺钙会导致佝偻病。
(2)向钙片中加入稀盐酸,钙片中的碳酸钙会和盐酸反应生成二氧化碳,根据化学方程式,代入二氧化碳的质量可以求出碳酸钙的质量,然后用碳酸钙的质量×
碳酸钙中钙元素的质量分数便可求出钙元素的质量。
(1)C
(2)解:
设碳酸钙的质量为x
CaCO3+2HCl====CaCl2+H2O+CO2↑
10044
x0.55g
100/x=44/0.55gx=1.25g
钙元素的质量=1.25g×
40/100=0.5g=500mg
所以钙元素的含量与标注相符。
12.【解析】本题考查的是表格数据分析能力和根据化学方程式计算的能力,因铜与稀硫酸不反应,因此铜和氧化铜的混合物与稀硫酸反应时,固体质量减少量是氧化铜的质量。
比较实验1、2可知,实验1中硫酸完全反应,比较实验2、3知,实验2中氧化铜完全反应,由此可知,样品中铜的质量为8g,则样品中铜的质量分数为
设实验1中20g稀硫酸中溶质质量为x
CuO+H2SO4====CuSO4+H2O
8098
10g-8.4gx
=1.6g
80∶98=1.6g∶xx=1.96g
稀硫酸中溶质的质量分数
(1)铜(或Cu)
(2)80%
(3)9.8%(计算过程见解析)
乾洲教育在线第-7-页共7页025-58655366