2016年初三化学复习重点知识点分类总结Word格式.doc
《2016年初三化学复习重点知识点分类总结Word格式.doc》由会员分享,可在线阅读,更多相关《2016年初三化学复习重点知识点分类总结Word格式.doc(7页珍藏版)》请在冰豆网上搜索。
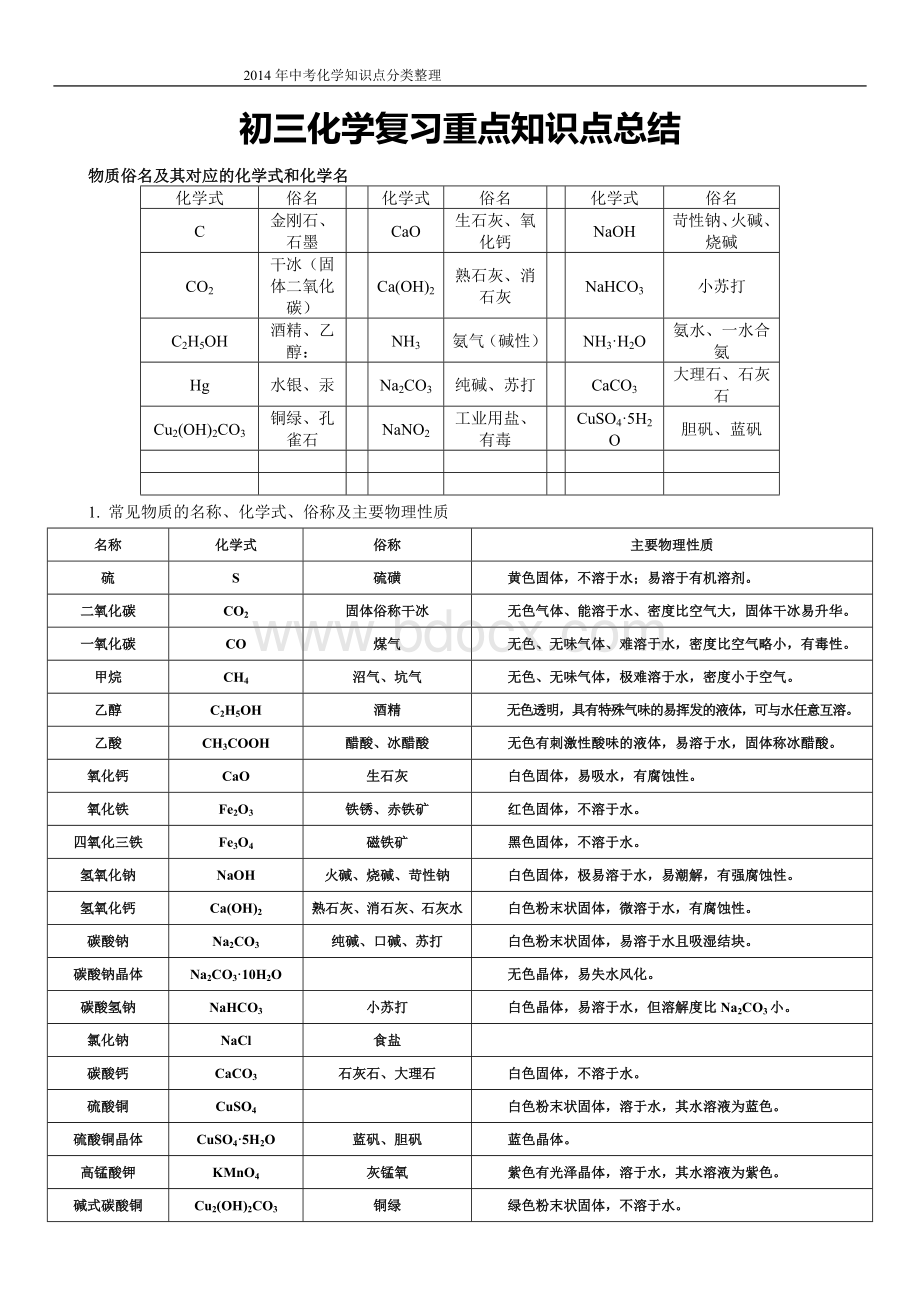
工业用盐、有毒
CuSO4·
5H2O
胆矾、蓝矾
1.常见物质的名称、化学式、俗称及主要物理性质
名称
俗称
主要物理性质
硫
S
硫磺
黄色固体,不溶于水;
易溶于有机溶剂。
二氧化碳
固体俗称干冰
无色气体、能溶于水、密度比空气大,固体干冰易升华。
一氧化碳
CO
煤气
无色、无味气体、难溶于水,密度比空气略小,有毒性。
甲烷
CH4
沼气、坑气
无色、无味气体,极难溶于水,密度小于空气。
乙醇
酒精
无色透明,具有特殊气味的易挥发的液体,可与水任意互溶。
乙酸
CH3COOH
醋酸、冰醋酸
无色有刺激性酸味的液体,易溶于水,固体称冰醋酸。
氧化钙
生石灰
白色固体,易吸水,有腐蚀性。
氧化铁
Fe2O3
铁锈、赤铁矿
红色固体,不溶于水。
四氧化三铁
Fe3O4
磁铁矿
黑色固体,不溶于水。
氢氧化钠
火碱、烧碱、苛性钠
白色固体,极易溶于水,易潮解,有强腐蚀性。
氢氧化钙
熟石灰、消石灰、石灰水
白色粉末状固体,微溶于水,有腐蚀性。
碳酸钠
纯碱、口碱、苏打
白色粉末状固体,易溶于水且吸湿结块。
碳酸钠晶体
Na2CO3·
10H2O
无色晶体,易失水风化。
碳酸氢钠
白色晶体,易溶于水,但溶解度比Na2CO3小。
氯化钠
NaCl
食盐
碳酸钙
石灰石、大理石
白色固体,不溶于水。
硫酸铜
CuSO4
白色粉末状固体,溶于水,其水溶液为蓝色。
硫酸铜晶体
蓝矾、胆矾
蓝色晶体。
高锰酸钾
KMnO4
灰锰氧
紫色有光泽晶体,溶于水,其水溶液为紫色。
碱式碳酸铜
铜绿
绿色粉末状固体,不溶于水。
氯化银
AgCl
新制得为白色凝乳状沉淀,不溶于稀硝酸。
硫酸钡
BaSO4
天然产称重晶石
白色固体,不溶于水,不溶于稀硝酸。
氢氧化铁
Fe(OH)3
新制得为红褐色沉淀。
氢氧化铜
Cu(OH)2
新制得为蓝色沉淀。
2.几种常见药品的存放
药品
性质
保存方法
白磷
着火点低,易自燃,不跟水反应
放入冷水中
浓硫酸
易吸收空气中的水分(吸水性)
放入玻璃瓶内,瓶塞要严
浓盐酸
易挥发
浓硝酸
易吸水,易与空气中二氧化碳反应而变质
密封于干燥试剂瓶中
固体氢氧化钠
易潮解,易与空气中二氧化碳反应而变质
1.地壳中含量最多的金属元素是铝(Al)。
2.地壳中含量最多的非金属元素是氧(O2)。
3.空气中含量最多的物质是氮气(N2)
4.天然存在最硬的物质是金刚石(C)。
5.最简单的有机物是甲烷。
(CH4)
6.金属活动顺序表中活动性最强的金属是钾(K)。
7.相对分子质量最小的氧化物是水(H2O)。
最简单的有机化合物CH4
常见物质的颜色的状态
1.白色固体:
MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;
铁、镁为银白色(汞为银白色液态)
2.黑色固体:
石墨、炭粉、铁粉、CuO、MnO2、Fe3O4
KMnO4为紫黑色。
3.红色固体:
Cu、Fe2O3、HgO、红磷▲硫:
淡黄色▲Cu2(OH)2CO3为绿色
4.溶液的颜色:
凡含Cu2+的溶液呈蓝色;
凡含Fe2+的溶液呈浅绿色;
凡含Fe3+的溶液呈棕黄色,其余溶液一般为无色。
(高锰酸钾溶液为紫红色)
5.沉淀(即不溶于水的盐和碱):
①盐:
白色↓:
CaCO3、BaCO3(溶于酸)AgCl、BaSO4(不溶于稀HNO3)等
②碱:
蓝色↓:
Cu(OH)2红褐色↓:
Fe(OH)3白色↓:
Mg(OH)2。
6.
(1)具有刺激性气体的气体:
NH3、SO2、HCl(皆为无色)
(2)无色无味的气体:
O2、H2、N2、CO2、CH4、CO(剧毒)
▲注意:
具有刺激性气味的液体:
盐酸、硝酸、醋酸。
酒精为有特殊气体的液体。
7.有毒的,气体:
CO液体:
CH3OH;
固体:
NaNO2CuSO4(可作杀菌剂,与熟石灰混合配成天蓝色的粘稠状物质——波尔多液)
解题技巧和说明
推断题解题技巧
看其颜色,观其状态,察其变化,初代验之,验而得之。
黑色:
MnO2、CuO、Fe3O4、C、FeS(硫化亚铁)
蓝色:
CuSO4•5H2O、Cu(OH)2.CuCO3.含Cu2+溶液、液态固态O2(淡蓝色)
红色:
Cu(亮红色)、Fe2O3(红棕色)、红磷(暗红色)
黄色:
硫磺(单质S)、含Fe3+的溶液(棕黄色)
绿色:
FeSO4•7H2O、含Fe2+的溶液(浅绿色)、碱式碳酸铜[Cu2(OH)2CO3]
无色气体:
N2、CO2、CO、O2、H2、CH4
有色气体:
Cl2(黄绿色)、NO2(红棕色)
有刺激性气味的气体:
NH3(此气体可使湿润pH试纸变蓝色)、SO2
有臭鸡蛋气味:
H2S
(二)解实验题
看清题目要求是什么,要做的是什么,这样做的目的是什么。
实验用到的气体要求是比较纯净,除去常见杂质具体方法:
①除水蒸气可用:
浓流酸、CaCl2固体、碱石灰、无水CuSO4(并且可以检验杂质中有无水蒸气,有则颜色由白色→蓝色)、生石灰等;
②除CO2可用:
澄清石灰水(可检验出杂质中有无CO2)、NaOH溶液、KOH溶液、碱石灰等;
③除HCl气体可用:
AgNO3溶液(可检验出杂质中有无HCl)、石灰水、NaOH溶液、KOH溶液;
除气体杂质的原则:
用某物质吸收杂质或跟杂质反应,但不能吸收或跟有效成份反应,或者生成新的杂质。
2.实验注意的地方:
①防爆炸:
点燃可燃性气体(如H2、CO、CH4)前,要检验气体纯度。
②防暴沸:
稀释浓硫酸时,将浓硫酸倒入水中,不能把水倒入浓硫酸中。
③防中毒:
进行有关有毒气体(如:
CO、SO2、NO2)的性质实验时,在通风厨中进行;
并要注意尾气的处理:
CO点燃烧掉;
SO2、NO2用碱液吸收。
④防倒吸:
加热法制取并用排水法收集气体,要注意熄灯顺序
实验室制取三大气体中常见的要除的杂质:
(1)制O2要除的杂质:
水蒸气(H2O)
(2)用盐酸和锌粒制H2要除的杂质:
水蒸气(H2O)、氯化氢气体(HCl,盐酸酸雾)(用稀硫酸没此杂质)
(3)制CO2要除的杂质:
水蒸气(H2O)、氯化氢气体(HCl)
除水蒸气的试剂:
浓流酸、CaCl2固体、碱石灰(主要成份是NaOH和CaO)、生石灰、无水CuSO4(并且可以检验杂质中有无水蒸气,有则颜色由白色→蓝色)等;
除HCl气体的试剂:
AgNO3溶液(并可检验出杂质中有无HCl)、澄清石灰水、NaOH溶液(或固体)、KOH溶液(或固体);
[生石灰、碱石灰也可以跟HCl气体反应]
常见气体的性质
(1)氧气O2(通常状况下)化学性质及用途(O2)无色无味的气体,不易溶于水,密度比空气略大a.供呼吸;
b.炼钢;
c.气焊。
(注:
O2具有助燃性,但不具有可燃性,不能燃烧。
)
(2)氢气(H2)无色无味的气体,难溶于水,密度比空气小,是最轻的气体。
①可燃性:
a.填充气、飞舰(密度比空气小)b.合成氨、制盐酸c.气焊、气割(可燃性)4.提炼金属(还原性)
②还原性:
3H2+Fe2O3△2Fe+3H2O
(3)二氧化碳(CO2)无色无味的气体,密度大于空气,能溶于水,固体的CO2叫“干冰”。
①CO2+H2O==H2CO3(酸性)(H2CO3===H2O+CO2↑)(不稳定)
a.用于灭火(应用其不可燃烧,也不支持燃烧的性质)b.制饮料、化肥和纯碱
CO2+Ca(OH)2==CaCO3↓+H2O(鉴别CO2)CO2+2NaOH==Na2CO3+H2O
②氧化性:
CO2+C==2COCaCO3==CaO+CO2↑(工业制CO2)
(4)一氧化碳(CO)无色无味气体,密度比空气略小,难溶于水,有毒气体。
①可燃性:
2CO+O2==2CO2
(火焰呈蓝色,放出大量的热,可作气体燃料)a.作燃料b.冶炼金属
②还原性:
3CO+Fe2O3高温2Fe+3CO2(跟血液中血红蛋白结合,破坏血液输氧的能力)
基本化学反应
物质反应
化学方程式
伴随现象
化合反应
镁在空气中燃烧
2Mg+O2点燃2MgO
耀眼的白光、放出热量、生成白色粉末
铁在氧气中燃烧
3Fe+2O2点燃Fe3O4
剧烈燃烧,火星四射、放出热量、黑色固体生成
氢气中空气中燃烧
2H2+O2点燃2H2O
淡蓝色火焰、放出热量、烧杯内壁出现水雾
红(白)磷燃烧
4P+5O2点燃2P2O5
发出白光、放出热量、生成大量白烟。
碳在氧气中充分燃烧
C+O2点燃CO2
发出白光、放出热量、澄清石灰水变浑浊
碳不充分燃烧
2C+O2点燃2CO
CO2通过灼热碳层
C+CO2高温2CO
(吸热反应)
氧化钙溶于水
CaO+H2O==Ca(OH)2(放大量热)
白色块状固体变为粉末、生石灰制备石灰浆
二氧化碳溶于水
CO2+H2O===H2CO3
石蕊试液由紫色变成红色。
分解反应
水在通电分解
2H2O通电2H2↑+O2↑
两电极上有气泡产生、(正氧负氢)
加热高锰酸钾
2KMnO4△K2MnO4+MnO2+O2↑
紫色变为黑色、生成使带火星木条复燃的气体
双氧水制氧气
2H2O2MnO22H2O+O2↑
有气泡产生,带火星的木条复燃。
锻烧石灰石
CaCO3高温CaO+CO2↑
(二氧化碳工业制法)工业制备二氧化碳和生石灰
碳酸不稳定而分解
H2CO3===H2O+CO2↑
石蕊试液由红色变成紫色。
小苏打受热分解
2NaHCO3△Na2CO3+H2O+CO2↑
产生使澄清石灰水变浑浊的气体小苏打蒸馒头
置换反应基本形式:
A+BC=AC+B单质和化合物反应生成另一种单质和另一种化合物
酸与金属反应
Zn+H2SO4==ZnSO4+H2↑ Fe+H2SO4==FeSO4+H2↑ Mg+2HCl==MgCl2+H2↑
放出气体
盐与金属反应
2Al+3CuSO4==Al2(SO4)3+3Cu
银白色金属表面覆盖有红色物质
铁溶于稀硫酸
Fe+H2SO4=FeSO4+H2↑
有气体生成