A级医疗器械软件生存周期评估报告标准要求文档格式.docx
《A级医疗器械软件生存周期评估报告标准要求文档格式.docx》由会员分享,可在线阅读,更多相关《A级医疗器械软件生存周期评估报告标准要求文档格式.docx(23页珍藏版)》请在冰豆网上搜索。
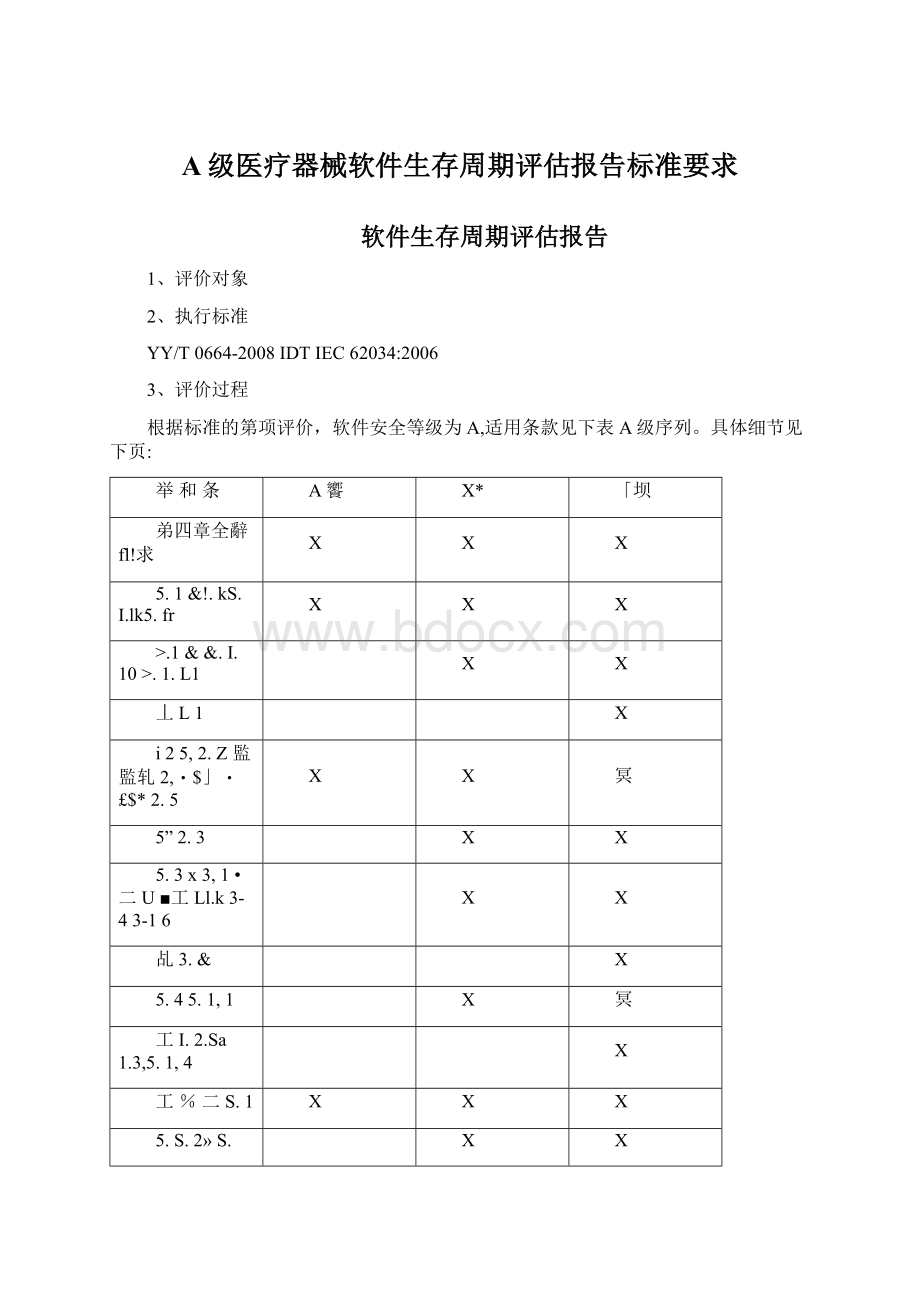
丄L1
i25,2.Z監監轧2,・$」・£
$*2.5
冥
5”2.3
5.3x3,1•二U■工Ll.k3-43-16
乩3.&
5.45.1,1
工I.2.Sa1.3,5.1,4
工%二S.1
5.S.2»
S.
X』・$
乩E仝萍鉴审
S.7金澤吿审
久吕5.S.1
IlS.rS-K.2,5.a1.55.5.ft.15,5.A.Th5.
Ar1R1
tLi?
b.Z.1.6Z.2.62上5
札a.”
瓦X鱼邦監*
7.t令部冬求
x
7-2金邯左求
7.i鱼邦豐*
7,A7,仇1
7.LK^I.5
ifix0个轉亶*
%
永q©
金带疋醸
;
Clause
-V^-f-H
早节
Requirements
标准要求
Result
测试结果
Verdict
判定
4
总要求
质量管理体系
医疗器械软件制造商应证实其有能力提供持续满足顾客和适用的法规要求的医疗器械软
件。
风险管理
制造商应使用符合YY/T0316(ISO14971)的
风险管理过程。
软件的安全性级别
a)
制造商应按照软件系统引起的危害对于患者、操作者或其他人员的可能影响,赋于每个软件
系统一个软件安全性级别(A、B或C)。
b)
制造商应依据风险控制措施所控制的危害的可能影响。
对实施风险控制措施起作用的每个软件系统赋予一个软件安全性级别。
c)
制造商应在风险管理文档中将赋予每个软件系统的软件安全性级别形成文档。
d)
当一个软件系统分解为软件项,及当一个软件项又进一步分解为几个软件项时,此类软件项应继承原软件项(或软件系统)的软件安全性级别,除非制造商以文件形式证明分类为不同的安全性级别的理由。
此类理由说明应解释新的软件项是如何被分开的,以便可对其另行分级。
e)
如果以分解方式产生的软件项的安全级别和其源软件项不同,制造商应对每个软件项的软件安全级别形成文档。
f)
为符合本标准,无论特定级别的软件项是否需要一个过程,此过程是否有必要应用于一组软件项,制造商应使用此组中最高级别的软件项所要求的诸过程和任务,除非制造商在风险管理文档中有使用较低级别的理由的说明文件。
g)
对每个软件系统,在赋予软件安全性级别以前,均应应用C级要求。
5
软件开发过程
软件开发策划
5.1.1
软件开发计划
制造商应制定一项(或多项)软件开发计划,以便实施适合于所开发软件系统的范围、规模和软件安全级别的软件开发过程的活动。
在一个(或多个)计划中应完整地规定或引用软件开发生存周期模型。
计划应说明下列各项:
用于软件系统开发的过程。
各项活动和任务的交付物(包括文件)。
系统需求、软件需求、软件系统测试和软件中实施的风险控制措施之间的可追溯性
软件配置和更改管理,包括未知来源软件配置
项和用于支持开发的软件;
和
在生存周期每个阶段的软件产品、交付物和活动中发现的用于处理问题的软件问题解决方
案。
5.1.2
保持软件开发计划更新
在适当时,制造商应在开发进行的同时更新计
戈叽
5.1.3
引用系统设计和开发的软件开发计划
制造商应在软件开发计划中引用系统需求,作
为软件开发的输入
制造商应在软件开发计划中包括或引用用于协调软件开发和为满足必需的设计开发确认的规程。
5.1.6
软件验证策划
制造商应在软件开发计划中包括或引用下列
验证信息
需要验证的交付物
每个生存周期活动所要求的验证任务
对交付物进行验证的里应碑,和
验证交付物的验收准则
5.1.7
软件风险管理策划
制造商应在软件开发计划中包括或引用实施软件风险管理过程的活动和任务的计划,包
括与未知来源软件有关的风险的管理.
5.1.8
文档策划
制造商应在软件开发计划中包括或引用有关
在软件开发生存周期中所形成文档的信息。
对
每个已识别的文挡或文档类型,应包括或引用
如下信息:
标题、名称或命名约定;
P
目的;
文件的预期阅读者;
开发、评审、批准和修改的程序和职责。
5.1.9
软件配置管理策划
制造商应在软件开发计划中包括或引用软件
配置管理信息。
软件配置管理信息应包括或引
用:
受控项目的级别、型式、类别或清单;
软件配置管理活动和任务;
负责进行软件配置管理和活动的组织;
他们和其他组织的关系,诸如软件开发或维
护;
当将这些项目处于配置控制之下时;
何时应用问题解决过程。
软件需求分析
5.2.1
由系统需求确疋软件需求并形成文档。
对每个医疗器械软件系统,制造商应从系统层
面需求中确疋软件系统需求并形成文档。
5.2.2
软件需求内容
在使用与医疗器械软件,制造商应在软件需求中包括:
功能和能力需求;
软件系统的输入和输出;
软件系统和其他系统之间的接口;
软件控制的报警、警告和操作者信息;
保密安全需求;
对人为错误敏感的适用性工程要求和培训;
数据定义和数据库需求;
h)
对已交付的医疗器械软件在操作和维护的一
个或多个地点的安装和验收要求;
i)
与操作和维护方法有关的要求;
j)
要编制的用户文档;
k)
用户维护要求;
和;
l)
法规要求。
5.2.4
医疗器械风险分析的再评价
制造商应在制疋并适当更新软件需求时,对医疗器械风险分析进行再评价。
5.2.5
更新系统需求
制造商应确保对现有的需求〈包括系统需求)
进行再评价和适当时更新,作为软件需求分析活动的结果。
5.2.6
验证软件需求
制造商应对软件需求进行验证并形成文档。
实施包括有关风险控制在内的系统需求;
需求不互相矛盾;
避免使用含糊不清的术语表示;
用表述的术语来制定测试准则和实施测试,以
确定是否满足测试准则;
可以进行唯一性标识;
对于系统要求或其他来源是可追溯的。
软件单元的实现和验证
5.5.1
制造商应实现每个软件单元。
软件发行
584
将发行的版本形成文档。
6
软件维护过程
制定软件维护计划
制造商应为进行维护过程的活动和任务,制定一项(或多项)软件维护计划,计划应说明以下内容:
用于以下目的的规程:
――接收
――形成文档
――评价
解决过程,和:
――跟踪。
――医疗器械软件发行后引起的反馈;
是否将反馈作为问题加以考虑的准则;
软件风险管理过程的应用;
应用软件冋题解决过程以分析和解决在医疗
器械软件发行后出现的问题;
应用软件配置管理过程(第8章)管理对现有系统的更改:
评价并实施未知来源软件(SOUP下列事项的
规程:
――升级
――缺陷修复
――补丁和;
废弃
问题和修改分析
6.2.1
形成文档并评价反馈
621.1
监控反馈
制造商应从其组织内部和用户两方面监控对对已发行的软件产品的反馈。
621.2
反馈应形成文档并进行评价,以决定其对已发行的软件产品安全性有何种影响,是否有必要对已发行的软件产品进行更改以解决问题。
621.3
评价问题报告对安全性的影响
应对每个问题报告进行评价,以确定已发行的软件产品是否存在问题。
任何这样的问题应以问题报告的形式记录(见第9章)。
问题报告应包括实际的或潜在的不良事件和对规范的偏离。
622
应用软件问题解决过程
制造商应利用软件冋题解决过程(见第9章)
阐明问题报告。
624
更改请求的批准
制造商应评价并批准修改已发行软件产品的经批准的更改请求。
6.2.5
联系用户和