辽宁省阜新二高学年高二化学下学期期末考试试题Word文档格式.docx
《辽宁省阜新二高学年高二化学下学期期末考试试题Word文档格式.docx》由会员分享,可在线阅读,更多相关《辽宁省阜新二高学年高二化学下学期期末考试试题Word文档格式.docx(12页珍藏版)》请在冰豆网上搜索。
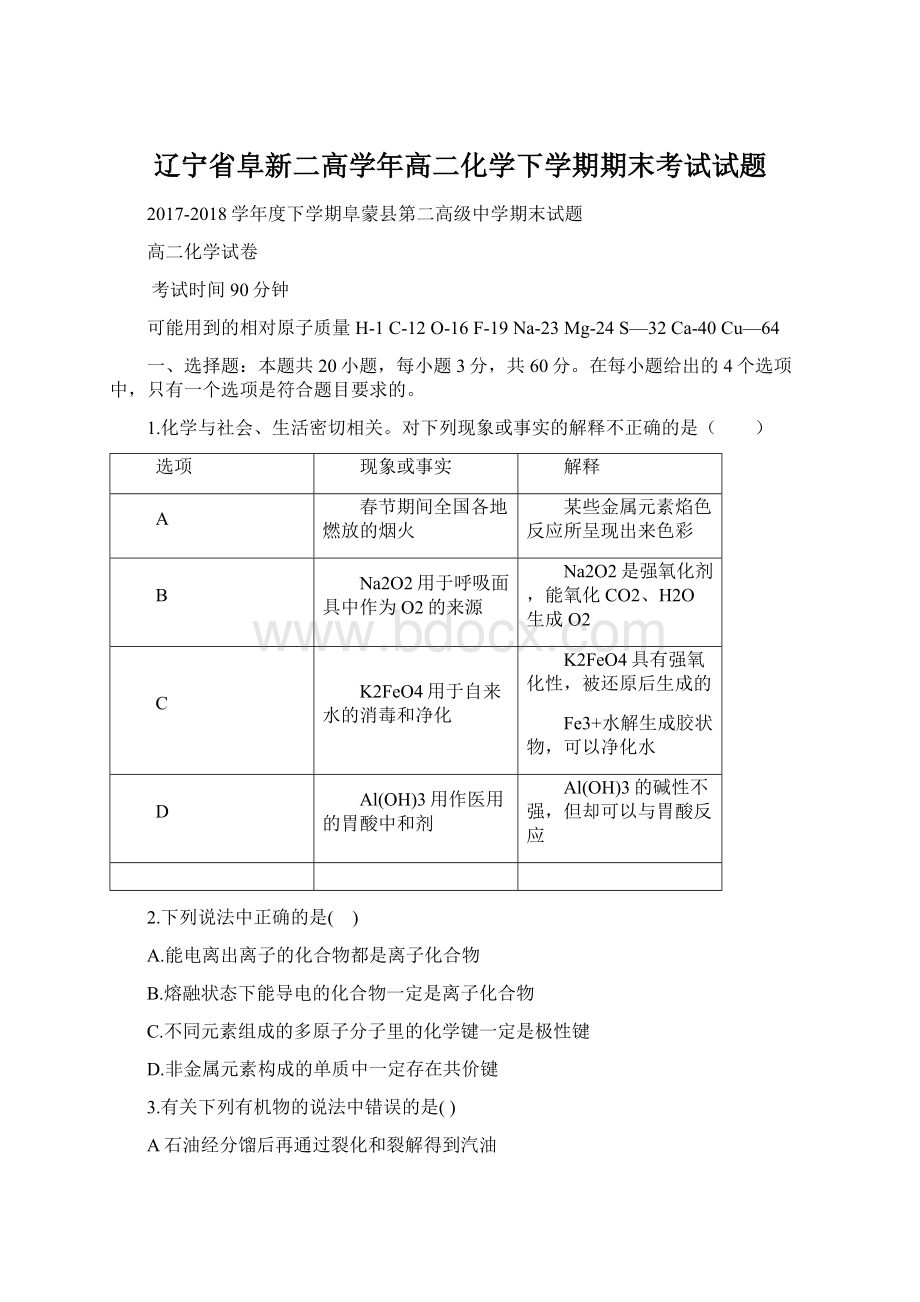
K2FeO4具有强氧化性,被还原后生成的
Fe3+水解生成胶状物,可以净化水
D
Al(OH)3用作医用的胃酸中和剂
Al(OH)3的碱性不强,但却可以与胃酸反应
2.下列说法中正确的是(
)
A.能电离出离子的化合物都是离子化合物
B.熔融状态下能导电的化合物一定是离子化合物
C.不同元素组成的多原子分子里的化学键一定是极性键
D.非金属元素构成的单质中一定存在共价键
3.有关下列有机物的说法中错误的是()
A石油经分馏后再通过裂化和裂解得到汽油
B.植物油通过氢化加成可以变成脂肪
C用灼烧的方法可以区别蚕丝和合成纤维
D.在做淀粉的水解实验时,用碘水检验淀粉是否完全水解
4.下列离子在指定溶液中一定不能大量共存的是()
A弱碱性溶液中:
HCO3-、NO3-、Na+、Cl-
B.常温时pH=7的溶液中:
Fe3+、SO42-、K+、Cl-
C.含NO3-的溶液中:
Fe3+、.SO42-、H+.NH4+
D.与铝反应产生H2的溶液中:
S2-、K+、CO32-、Na+
5.NA代表阿伏加德罗常数的数值,下列说法中错误的是()
A完全燃烧1.5mol乙醇和乙烯的混合物,转移电子数为18NA
B.7.8g由Na2S和Na2O2组成的混合物中含有阴离子的数目为0.1NA
C.0.1mol/LFeCl3溶液中Fe3+的物质的量一定小于0.1NA
D.常温常压下,60g甲醛和乙酸的混合物所含碳原子数为2NA
6.提纯下列物质(括号内为少量杂质),所选用的除杂试剂与分离方法错误的是(
不纯物质
除杂试剂
分离方法
Mg(Al)
NaOH溶液
过滤
乙烷(乙烯)
溴水
洗气
CuCl2(FeCl3)
单质铜
乙酸乙酯(乙酸)
饱和碳酸钠溶液
分液
7.下列试剂的保存方法及解释中错误的是()
A.金属钾在空气中易被氧化,因此少量钾保存在煤油中
B.NaOH与玻璃中的SiO2反应,因此NaOH溶液保存在配有橡胶塞的细口瓶中
C.常温时铝遇浓硫酸钝化,所以可以用铝制容盛装浓硫酸
D.为防止FeSO4水解而变质,常在溶液中加入少量铁粉
8.乙为两种常见的单质,丙、丁为氧化物,它们存在如下转化关系,则不满足条件的甲和乙为(
A.
铝和铁B.镁和碳C.
铁和氢气D.
铜和氢气
9.下列离子方程式书写不正确的是()
A、等体积、等物质的量浓度的NaHCO3和Ca(OH)2两溶液混合:
HCO3-+Ca2++OH-==CaCO3↓+H2O
B、向澄清石灰水中通入过量的CO2:
OH-+CO2==HCO3-
C、在含3amolHNO3的稀溶液中,加入amol铁粉:
4Fe+12H++3NO3-=Fe3++3Fe2++3NO↑+6H2O
D、Al2(SO4)溶液中加入过量氨水:
Al3++4NH3•H2O=AlO2-+4NH4++2H2O
10.向含Al2(SO4)3和AlCl3的混合溶液中逐滴加人1mol/LBa(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所得沉淀的物质的量的关系如图,下列说法不正确的是(
)
A.原混合液中c(SO42-):
c(Cl-)=1:
1
B.向D点溶液中通人C02气体,立即产生白色沉淀
C.图中A点沉淀中含有BaSO4和Al(OH)3
D.AB段反应的离子方程式为:
Al3++3OH-=Al(OH)3↓
11.利用Cu和浓硫酸制备SO2的反应涉及的装置,下列说法正确的是(
A用装置①制备B用装置②检验和收集
C用装置③稀释反应后溶液D用装置④测定反应后溶液中
12.W、X、Y、Z是原子序数依次增大的四种短周期元素,分属于连续的四个主族,电子层数之和为10,四种原子中X原子的半径最大.下列说法不正确的是(
A.Y原子形成的离子是同周期元素所形成的离子中半径最小的
B.Y的最高价氧化物不能与Z的最高价氧化物对应的水化物反应
C.W与同主族元素可以形成离子化合物
D.工业上获得X单质可利用电解其熔融的氧化物的方法
13.对于反应SO2(g)+O2(g)⇌2SO3(g)
△H<
0.达到平衡后,以下分析正确的是( )
A.减小生成物浓度,对正反应的反应速率影响更大
B.扩大容器体积,对正反应的反应速率影响更大
C.降低温度,对正反应的反应速率影响更大
D.加入催化剂,对逆反应的反应速率影响更大
14.如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池放电、充电的化学方程式为:
2K2S2+KI3⇌K2S4+3KI.装置(Ⅱ)为电解池的示意图.当闭合开关K时,电极X附近溶液先变红.则闭合K时,下列说法不正确的是(
K+从左到右通过离子交换膜
B.
电极A上发生的反应为:
I3-+2e-=3I-
C.
电极Y上发生的反应为:
2Cl--2e-=Cl2
D.
当有0.1
mol
K+通过离子交换膜,X电极上产生1.12
L气体(标准状况)
15.某温度下,将1.1molI2加入到氢氧化钾溶液中,反应后得到
KI、KIO、KIO3的混合液。
经测定IO-与IO3-的物质的量之比是2:
3.下列说法错误的是( )
A.I2在该反应中既作氧化剂又做还原剂
B.I2的还原性大于KI的还原性,小于KIO和KIO3的还原性
该反应中转移电子的物质的量为1.7mol
该反应中,被还原的碘元素与被氧化的碘元素的物质的量之比是17:
5
16.室温下,将0.1mol/L的一元酸HA溶液逐滴滴加到10mL0.1mol/LNaOH溶液中,pH的变化曲线如图所示。
下列说法错误的是( )
A.a点所示溶液中c(Na+)>
c(A-)>
c(OH-)>
c(HA)
B.a、b两点所示溶液中水的电离程度a点大于b点
C.pH=7时,c(Na+)=c(A-)+c(HA)
D.一元酸HA为弱酸
17.将一定量的镁和铜组成的混合物加入到过量的稀硝酸中,金属完全溶解(假设反应中还原产物只有NO)。
向反应后的溶液中加入3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g。
则下列叙述中错误的是(
)。
A:
当生成的沉淀量达到最大时,消耗NaOH溶液的体积V=100ml
B:
当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol
C:
参加反应的金属的总质量为9.6g>
m>
3.6g
D:
当金属全部溶解时收集到NO气体的体积在标准状况下一定为2.24L
18.从海水中提取镁的工业流程如图所示,下列说法正确的是(
在实验室进行②的操作需用到坩埚、坩埚钳、玻璃棒、酒精灯
步骤⑥电解MgCl2时,阴极产生H2
步骤⑤应将晶体置于HCl气体氛围中脱水
D.
上述工艺流程中的反应未涉及氧化还原反应
19.将一定量纯净的氨基甲酸铵置于密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
H2NCOONH4(s)⇌2NH3(g)+CO2(g)。
能判断该反应已经达到化学平衡的是()
①v(NH3)正=2v(CO2)逆②密闭容器中总压强不变③密闭容器中混合气体的密度不变④密闭容器中混合气体的平均相对分子质量不变⑤密闭容器混合气体的总物质的量不变密闭容器中CO2的体积分数不变混合气体总质量
A.①②③⑤B.①②⑤C.①⑤D.全部
20.某烃的含氧衍生物的相对分子质量为102,其中氧元素的质量分数约为31.4%,则能与NaOH溶液反应的有机物有(不含立体异构)()
A.11种B.8种C.12种D.13种
二、非选择题:
共40分.
21.随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示.
根据判断出的元素回答问题:
(1)z在周期表中的位置是
.
(2)写出x和d组成的一种四原子共价化合物的电子式
(3)y、g、h的最高价氧化物对应水化物的酸性最强的是.(填化学式)
(4)写出f的最高价氧化物与e的最高价氧化物对应的水化物反应的离子方程式
(5)已知e和g的最高价氧化物对应的水化物的稀溶液反应生成1mol水时所放出的热量为QkJ。
请写出该反应的中和热的热化学方程式
(6)用y元素的单质与f元素的单质可以制成电极浸入由x、d、e三种元素组成的化合物的溶液中构成电池负极反应式为
22.二氧化铈(CeO2)是一种重要的稀土氧化物。
以氟碳铈矿(主要含CeFCO3)为原料制备CeO2的一种工艺流程图如图:
已知:
①Ce4+既能与F-结合成[CeFX](4-x)+,也能与SO42-结合成[CeSO4]2+;
②在硫酸体系中Ce4+能被萃取剂[(HA)2]萃取,而Ce3+不能。
回答下列问题:
(1)“氧化焙烧”前需将矿石粉碎成细颗粒,其目的是
。
(2)“酸浸”中会产生大量黄绿色气体,写出CeO2与盐酸反应的离子方程式
,为避免上述污染,请提出一种解决方案:
(3)“萃取”时存在反应:
Ce4++n(HA)2⇌Ce·
(H2n-4A2n)+4H+。
实验室中萃取时用到的主要玻璃仪器名称为
,
(4)“反萃取”中,在稀硫酸和H2O2的作用下CeO2转化为Ce3+,H2O2在该反应中作
(填“催化剂”、“氧化剂”或“还原剂”),每有1molH2O2参加反应,转移电子物质的量为
(5)“氧化”步骤的化学方程式为
(6)取上述流程得到的CeO2产品0.50g,加硫酸溶解后,用0.10mol/LFeSO4标准溶液滴定至终点时(铈被还原为Ce3+,其他杂质均不参加反应),消耗25.00ml标准溶液。
该产品中CeO2的质量分数为
(Ce的相对原子质量为140)
23.某校化学研究性学习小组的同学在学习了氨的性质后讨论:
运用类比的思想,既然氨气具有还原性,能否像H2那样还原CuO呢?
他们设计实验制取氨气并探究上述问题。
请你参与该小组的活动并完成下列研究:
(一)制取氨气
(1)写出实验制取氨气的化学方程式_______________________________;
(2)有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。
你认为他能否达到目的?
________(填“能”或“否”)。
理由是。
(二)该小组中某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性:
(1)该装置在设计上有一定缺陷,为保证实验结果的准确性,对