苏教版初中化学知识归纳Word格式.docx
《苏教版初中化学知识归纳Word格式.docx》由会员分享,可在线阅读,更多相关《苏教版初中化学知识归纳Word格式.docx(17页珍藏版)》请在冰豆网上搜索。
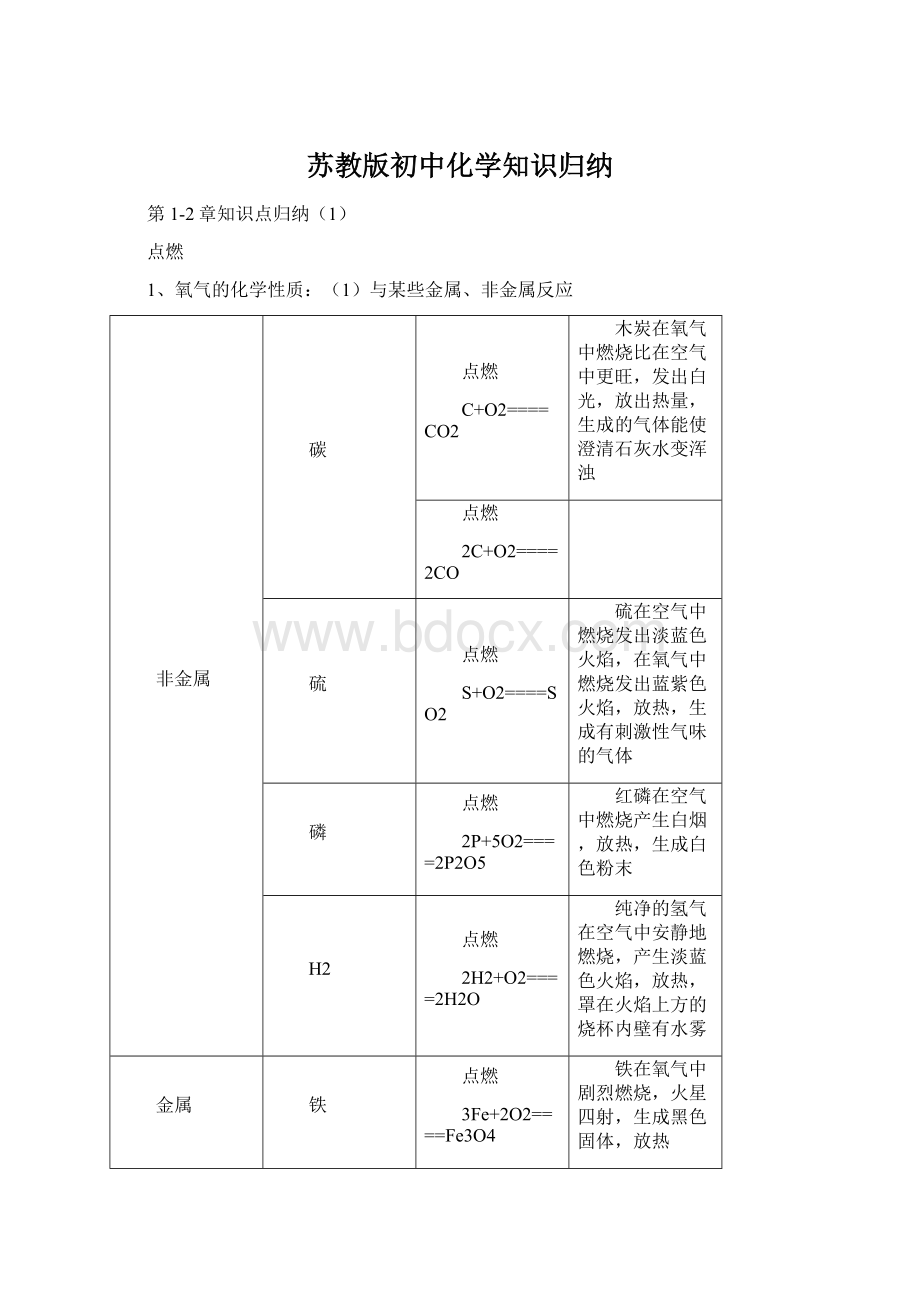
铜丝在空气中灼烧发黑
铝
4Al+3O2====2Al2O3
酶
(3)能与氧气反应的化合物有:
CO、CH4、C6H12O6、SO2、H2SO3,反应方程式:
尘埃
2CO+O2====2CO2、CH4+2O2====2H2O+CO2、C6H12O6+6O2====6H2O+6CO2、2SO2+O2====2SO3、2H2SO3+O2====2H2SO4
2、根据右图回答下列问题:
(1)该实验目的:
测定空气中氧气的含量
(2)该实验现象:
红磷燃烧产生大量白烟、倒吸入集气瓶中的水占集体瓶容积的1/5。
(3)该实验原理:
红磷燃烧消耗了氧气,生成固体,使得集气瓶中的压强变小,在大气压的作用下,烧杯中的水被压入集气瓶中。
(4)若测定结果偏小,可能是:
装置漏气、红磷量不足、没等到冷却就打开止水夹。
(5)若测定结果偏大,可能是:
红磷点燃后没有迅速伸入集气瓶内
3、二氧化碳的化学性质
(1)如右图所示,可观察到下面的蜡烛比上面的蜡烛先熄灭,说明二
氧化碳既不能燃烧也不能支持燃烧,且密度比空气大(灭火原理)
(2)二氧化碳能与可溶性碱反应:
CO2+Ca(OH)2====CaCO3↓+H2O(一般用于检验二氧化碳)
CO2+2NaOH====Na2CO3+H2O(一般用于吸收二氧化碳)
叶绿素
(3)能与水反应,为了证明该反应发生,可先在水中滴加紫色石蕊试液,再通入二氧化碳,可观察到紫色变成红色,说明反应发生,【CO2+H2O====H2CO3】,再加热,红色又变成紫色,说明碳酸不稳定,【H2CO3====CO2↑+H2O】
高温
(4)能与水发生光合作用:
6H2O+6CO2=======C6H12O6+6O2
(5)能与碳反应:
CO2+C====2CO
第1-2章知识点归纳
(2)
1、氧气、二氧化碳的实验室制法
氧气
二氧化碳
药品
高锰酸钾
双氧水、二氧化锰
石灰石(或大理石)、稀盐酸
反应原理
P36
P43
收集方法
向上排空气法(密度比空气大)
只能用向上排空气法
(密度比空气大且能溶于水)
排水法(不易溶于水)
检验方法
用带火星的木条伸入集气瓶中,复燃,证明是氧气
将气体通入澄清石灰水中,变浑浊,证明是二氧化碳
验满方法
用带火星的木条放在集气瓶口,复燃,证明已收集满氧气
将燃着的木条放在集气瓶口,火焰熄灭,证明已收集满
2、高锰酸钾制取氧气(实验中注意事项)
操作步骤
注意事项
目的
1.连接仪器,检查装置气密性
略
防止漏气,收集不到气体
2.加药品
药品平铺在试管底部
反应充分
3.固定装置
a.试管口略向下倾斜
防止水倒流引起试管炸裂
b.试管口塞一小团棉花
防止高锰酸钾随气流进入
导管或水槽
C.伸入试管的导管不能太长
防止气体难以排出
4.加热
先预热再集中加热
防止试管受热不均匀炸裂
5.收集
向上排空气法
导管伸到集气瓶底部
有利于排出空气
排水法
等到气泡连续均匀冒出时才收集
防止收集的氧气不纯
实验结束时,先将导管移出水面再停止加热
防止水倒吸进试管
引起试管炸裂
6.检验氧气
用带火星的木条伸入瓶中,若木条复燃,则为氧气(或用燃着的木条伸入瓶中,若燃烧更旺,则为氧气)
7.验满
用带火星的木条放到瓶口,若木条复燃,则已满
有气泡从集气瓶口往外冒,则已满
注:
收集一瓶干燥的氧气,可用向上排空气法;
收集一瓶较纯净的氧气,可用排水法。
3、氧气的工业制法:
分离液态空气法,属于物理变化。
是利用氮气和氧气的沸点不同,将液态空气控制温度蒸发,先蒸发出来的是氮气,剩下的是液氧。
4、催化剂在化学反应中能增大化学反应速率,但本身的质量和化学性质在反应前后都不变。
第1-2章知识点归纳(3)
1、碳酸氢铵的化学性质:
(1)不稳定性
①加热碳酸氢铵实验现象:
白色固体变少、产生刺激性的氨臭味、容器口有水珠、产生的气体能使澄清石灰水变浑浊。
②反应化学方程式:
NH4HCO3====NH3↑+H2O+CO2↑
③碳酸氢铵保存方法:
密封保存在阴凉处。
(2)与酸溶液反应产生二氧化碳气体
(3)与碱反应产生氨气
2、氮气的用途:
用作灯泡填充气、用作粮食、瓜果的保护气(氮气化学性质稳定);
液氮用于医疗手术、用于制氮肥。
3、碱式碳酸铜的化学性质:
(1)受热分解:
①现象:
粉末由绿色变成黑色、容器口有水珠、产生的气体能使澄清石灰水变浑浊。
Cu2(OH)2CO3====2CuO+H2O+CO2↑
(2)与酸反应产生二氧化碳气体。
4、做镁带燃烧实验所用的实验仪器:
坩埚钳、石棉网、酒精灯。
5、CO2含量呈上升趋势的原因:
含碳燃料(化石燃料)的大量燃烧、绿色植物不断减少。
6、进入久未开启的菜窖时要做灯火试验。
7、可以证明水是由氢、氧元素组成的实验有:
电解水和氢气在氧气中燃烧。
8、水的电解实验:
①为了增强水的导电性,可在水中加入少量稀硫酸或氢氧化钠溶液
②加水方法:
先将两玻璃管的活塞打开,再从长颈漏斗处加水直到水面到达两活塞处,然后关闭活塞再打开电源。
通电
③现象:
正极产生气体与负极产生气体的体积比为1:
2;
正极产生的气体能使带火星木条复燃;
负极产生的气体能燃烧。
④反应方程式:
2H2O====2H2↑+O2↑
9、硬水:
是指溶有较多钙、镁元素的水。
硬水软化的常用方法是煮沸。
硬水与软水的区分方法:
分别取样,加入肥皂水,产生泡沫多,垢状物少的是软水;
产生泡沫少,垢状物多的是硬水。
10、污水处理过程中,为了除去固体悬浮物,可用过滤的方法;
用明矾可以吸附水中悬浮颗
粒,形成大颗粒,加速沉降;
用活性炭可以吸附有色或有异味的气体或液体(吸附性属
于物理性质);
用氯气可杀菌消毒。
11、二氧化碳的用途:
①“干冰”用于人工降雨、人造云雾、致冷剂(干冰升华吸收)
②生产汽水(二氧化碳能溶于水,并与水反应生成碳酸)
③能促进绿色植物光合作用
④能灭火(二氧化碳既不燃烧,也不支持燃烧,且密度比空气大)
第三章知识点归纳
班级姓名
1.物质都是由微粒构成的,构成物质的基本微粒是分子、原子、离子。
2.微粒的共性有:
都很小,都在不断地运动,微粒之间有空隙。
3.由分子构成的物质如常见:
氧气、氢气、二氧化碳、水、双氧水等,
由原子构成的物质如:
金属、稀有气体、金刚石,
由离子构成的如:
常见的盐(氯化钠)、酸、碱。
4.由分子构成的物质在发生物理变化时,分子本身不变,只是分子间的空隙发生了改变。
在发生化学变化时,分子本身发生了改变,变成了新的微粒。
5.分子在化学变化中可以再分,分成原子,而原子在化学变化中不可再分,只能重新组合。
6.原子是由原子核和核外电子构成的,原子核由质子、中子构成。
电子的质量很小,原子的质量主要集中在原子核上。
电子在核外作高速运动,原子得到或失去电子后就变成了离子。
离子通过失去或得到电子还能变成原子。
7.相对原子质量的规定:
课本70页。
8.元素是具有相同质子数的同一类原子的总称。
元素分金属元素、稀有气体元素和非金属元素。
9.元素之最、元素与人体健康:
课本77-78页
10.单质、化合物、氧化物的概念:
课本76页
11.常见元素的化合价:
课本83页
单质的化合价为0。
12.元素符号和化学式表示的意义。
如:
H:
氢元素,一个氢原子。
Fe:
铁元素,一个铁原子,铁这种物质。
H2O:
水,一个水分子,水由氢、氧元素组成,水分子由氢原子和氧原子构成。
第四章知识归纳
1、燃烧是一种发光、发热的剧烈的化学反应。
2、物质燃烧一般需要同时满足三个条件:
物质具有可燃性;
可燃物与氧气接触;
可燃物的温度要达到它的着火点。
3、在氧气充足时,碳完全燃烧生成CO2;
氧气不充足时,碳不完全燃烧生成CO。
一氧化碳是无色无味的剧毒气体。
也可以燃烧,也是一种常见的气体燃料。
碳、氢元素的可燃物
燃烧速度
放热
生成物
完全燃烧(氧气充足)
快
多
碳、氢分别生成CO2和水
不完全燃烧(氧气不充足)
慢
少
碳、氢元素生成CO、
碳氢化合物和微小炭黑颗粒
5、可燃性气体在点燃前需验纯,常见的三种可燃性气体CO、CH4、H2。
6、针对3个条件,要阻止物质燃烧,灭火的三个原理分别是:
隔绝可燃物,如森林灭火可以设置隔离带;
隔绝氧气,如油锅起火盖锅盖;
降低温度至着火点以下,如用水灭火。
7、常见的消防标志:
书本P98
8、质量守恒定律:
参加化学反应的各物质的质量之和等于反应后的各物质质量之和。
验证实验:
凡是有气体参加或气体生成的化学反应,必须在密闭容器中进行。
9、质量守恒定律的意义:
肯定不变(各3个)
肯定变(各1个)
可能变(填1个)
宏观
元素种类
元素质量
物质总质量
物质种类
分子个数
微观
原子个数
原子种类
原子质量
分子种类
第五章知识点归纳
(1)
1.共性:
有金属光泽、硬度小、良好的导电性、导热性、延展性。
金属物理性质
特性:
铁—银白色、有磁性;
铁粉—黑色;
铜—紫红色
2.金属的化学性质:
常见的金属有铝、铁、铜(写出它们下列反应的化学方程式)
(1)与O2能反应:
4Al+3O2==2Al2O3
△
3Fe+2O2==Fe3O4
2Cu+O2==2CuO
(2)与稀硫酸或稀盐酸的反应:
在金属活动性顺序里,位于氢前面的金属能置换出酸(如盐酸、稀硫酸)中的氢,而位于氢后面的金属则不能。
2Al+3H2SO4==Al2(SO4)3+3H2↑
2Al+6HCl==2AlCl3+3H2↑
Fe+H2SO4==FeSO4+H2↑
Fe+2HCl==FeCl2+H2↑
现象:
铁钉表面出现气泡,溶液由无色变成浅绿色,反应过程中铁钉质量逐渐减少,溶液质量增加。
(3)与盐溶液的反应:
在金属活动性顺序里,位于前面的金属能把位于其后面的金属从它们的盐溶液里置换出来(钾、钙、钠除外)。
Fe+CuSO4==FeSO4+Cu(湿法炼铜反应原理)
铁钉表面出现红色物质,溶液由蓝色变成浅绿色,
反应后溶液质量减小。
以上
(2)(3)反应中反应的基本类型是置换反