质量控制用表格Word文档格式.docx
《质量控制用表格Word文档格式.docx》由会员分享,可在线阅读,更多相关《质量控制用表格Word文档格式.docx(12页珍藏版)》请在冰豆网上搜索。
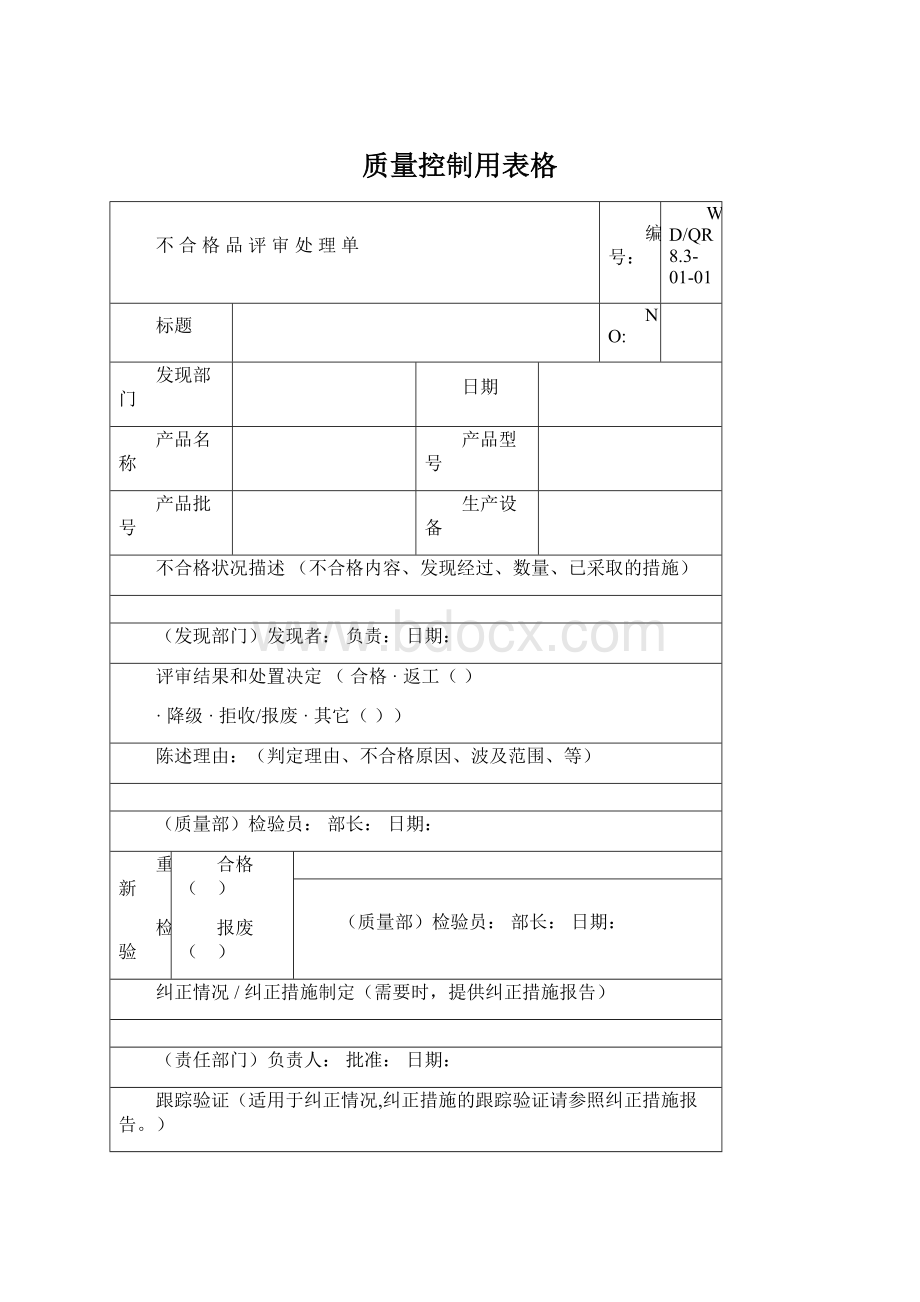
其它())
陈述理由:
(判定理由、不合格原因、波及范围、等)
(质量部)检验员:
部长:
重新
检验
合格 ( )
报废 ( )
纠正情况/纠正措施制定(需要时,提供纠正措施报告)
(责任部门)负责人:
批准:
跟踪验证(适用于纠正情况,纠正措施的跟踪验证请参照纠正措施报告。
)
(质量科)检验员:
[结果通知]
发放:
分发日期:
抄送
(1):
抄送
(2):
质量事故报告
WD/QR8.5.2-02-01NO:
报告日期:
年月日
TO:
FROM:
地址:
联系人:
电话:
传真:
Email:
顾客投诉:
有见附件无
产品名称:
产品型号规格:
批号:
发生地:
发生日期:
事故描述:
代理商(授权代表)的调查结果:
代理商(授权代表)建议:
公司的初步结论:
公司预定的纠正措施:
类似事故:
以前没有发生过不知道
以前发生过发生的国家:
发生地:
发生时间:
报告的公司:
接受报告的主管机构:
处理结果:
代理商:
公告机构:
证书号码:
详细调查结果请留意以后的报告。
纠正措施报告
编号
WD/QR8.5-01-01
标题:
NO:
不合格描述:
签字:
原因分析:
检验员/审核员:
制定纠正措施:
责任:
验证结果:
抄送部门:
质量改进报告
WD/QR8.5-01-02
改进理由陈述:
(提出部门)提案者:
审核:
改进措施制定:
负责人:
(审核部门)审核:
批准:
改进措施实施:
(实施部门)责任者:
验证:
(验证部门)责任者:
不合格品评审控制卡
编号:
CMSQRBHG01-
不合格品名称
不合格品型号
不合格品批号
不合格品数量
发生时间
年月日
不合格报告人
不合格品来源
不合格品分类
不合格品编号
不合格现象
检验员
不合格品的评审意见/原因分析(B类为初审意见)
不合格评审员
研发确认
B类及申请代用的A类不合格品的评审意见
总工程师
评审日期
不合格评审后处置内容(过程或结果)
处置人
不合格品跟踪控制
需要纠正措施吗?
不需要需要,责任人签收:
该不合格品使用在编号为产品上或:
销售到:
或:
不合格品报告
抄送科:
来料质量问题改善要求书
日期:
编号:
供应商
物料名称
规格型号
批号
来货数量
来货日期
检验记录编号
结果
□全检
检验数
不良数
不良率
决定:
□接受
□退货
□拣用
□特许使用
□抽检
AQL=抽检水平:
批量数
抽样数
允许数
缺陷数
不
合
格
描
述
改善
要求
供应商
改善对策
跟进
1.此报告通知供应商时间:
,请在以前回复。
以帮助我们了解处理状况。
2.此报告通知次数:
第一次第二次第三次
检验:
确认:
审核:
YG/QS2101
第0次修订
阳光医药NO.:
产品撤回登记记录
CMSQRCCH01-
日期
型号规格
产品编号
附件
撤回理由
客户名称
批准人
备注
CMS质量检验()统计报表
报表间期:
编号:
CMSQRSJX04-
序号
型号
一次交验
二次交验
总交验数
(台)
总合格数
总合格率
%
待处理数
交验数(台)
合格数(台)
直通率%
合格率%
1
2
3
4
5
6
备
注
填表人:
填报时间:
审核/日期:
纠正措施跟踪表检索号:
不合格报告编号
内容简述
责任人
规定
完成日
实际
验证人
/日期