挥发性脂肪酸的测定种方法文档格式.docx
《挥发性脂肪酸的测定种方法文档格式.docx》由会员分享,可在线阅读,更多相关《挥发性脂肪酸的测定种方法文档格式.docx(13页珍藏版)》请在冰豆网上搜索。
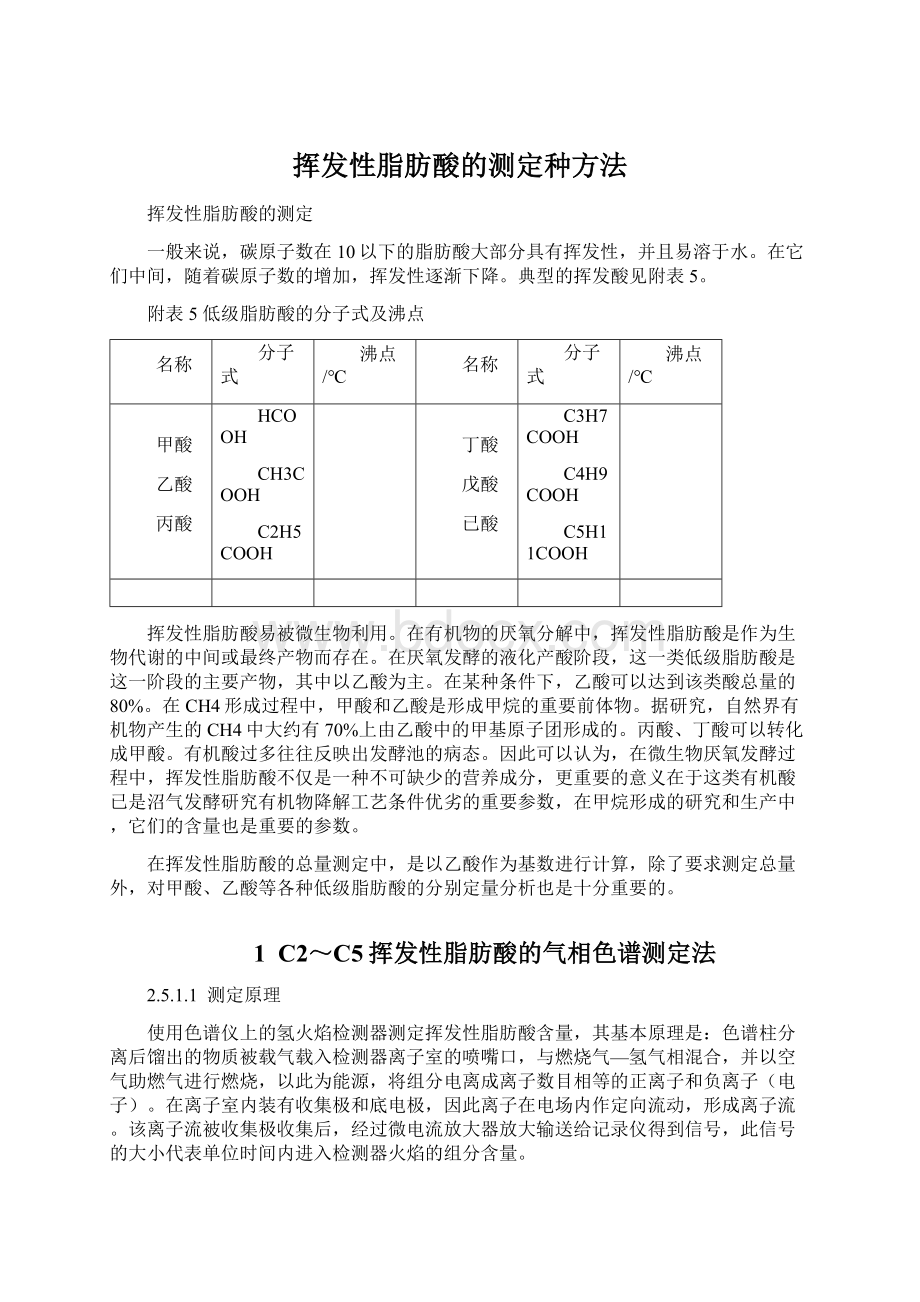
已酸
C3H7COOH
C4H9COOH
C5H11COOH
挥发性脂肪酸易被微生物利用。
在有机物的厌氧分解中,挥发性脂肪酸是作为生物代谢的中间或最终产物而存在。
在厌氧发酵的液化产酸阶段,这一类低级脂肪酸是这一阶段的主要产物,其中以乙酸为主。
在某种条件下,乙酸可以达到该类酸总量的80%。
在CH4形成过程中,甲酸和乙酸是形成甲烷的重要前体物。
据研究,自然界有机物产生的CH4中大约有70%上由乙酸中的甲基原子团形成的。
丙酸、丁酸可以转化成甲酸。
有机酸过多往往反映出发酵池的病态。
因此可以认为,在微生物厌氧发酵过程中,挥发性脂肪酸不仅是一种不可缺少的营养成分,更重要的意义在于这类有机酸已是沼气发酵研究有机物降解工艺条件优劣的重要参数,在甲烷形成的研究和生产中,它们的含量也是重要的参数。
在挥发性脂肪酸的总量测定中,是以乙酸作为基数进行计算,除了要求测定总量外,对甲酸、乙酸等各种低级脂肪酸的分别定量分析也是十分重要的。
1C2~C5挥发性脂肪酸的气相色谱测定法
2.5.1.1测定原理
使用色谱仪上的氢火焰检测器测定挥发性脂肪酸含量,其基本原理是:
色谱柱分离后馏出的物质被载气载入检测器离子室的喷嘴口,与燃烧气—氢气相混合,并以空气助燃气进行燃烧,以此为能源,将组分电离成离子数目相等的正离子和负离子(电子)。
在离子室内装有收集极和底电极,因此离子在电场内作定向流动,形成离子流。
该离子流被收集极收集后,经过微电流放大器放大输送给记录仪得到信号,此信号的大小代表单位时间内进入检测器火焰的组分含量。
2.5.1.2测定条件
⑴试剂设备
①乙酸、丙酸、丁酸、戊酸混合标准液的配制。
分别吸取乙酸(.,相对密度,含量99%)、丙酸(.,相对密度,含量%)、丁酸(.,相对密度,含量99%)、戊酸(.,相对密度,含量100%)各25μL于50mL容量瓶中,再加入甲酸(.,相对密度,含量88%),最后用蒸馏水定容。
其中乙酸、丁酸、戊酸的浓度分别为517μL/L、497μL/L、401μL/L、467μL/L。
②6mol/L硫酸的配制:
将167mL浓硫酸(相对密度)缓慢倒入833mL蒸馏水中。
③甲酸:
相对密度,含量88%。
④离心机4000~16000r/min。
⑤气相色谱仪,FID检测器。
⑵样品预处理用沼气发酵液7mL加入2滴6mol/LH2SO4使pH值降至左右(用pH试纸粗测),离心20~30min,取上层透明清液3mL,加入mL浓甲酸,最终pH值为左右(控制在以下)。
⑶主要实验参数
①条件一。
固定相:
GDX103+H3PO4,2%(60~80目);
色谱柱:
2m×
φ6mm;
柱温:
180~200℃;
气化室温度:
240℃;
检测温度:
210℃;
进样量:
2μL;
载气流量:
N2,50mL/min;
氢气流量:
50mL/min;
空气流量:
600~700mL/min;
衰减:
×
1/8。
②条件二。
φ3mm,不锈钢柱,内填国产GDX-401担体,60~80目;
载气:
N2,流率为90mL/min;
空气流率:
500mL/min;
氢气流率:
210℃。
③条件三。
φ6mm,装有以2%磷酸饱和的60~80目GDX-103担体;
④条件四。
φ2mm,玻璃柱,内装有10%的商品固定液FluoradFC431涂布的Supelcoport担体,100~200目;
130℃;
220℃;
N2,40mL/min。
⑷定性与定量
①定性。
配制模拟标准样品,用已知物质的保留时间对照被测物质的保留时间进行定性。
②定量。
用已知样校正法进行定量,其方法是配制已知浓度的标准样(与样品组分一致),进行色谱试验,测量标准样各组分的峰高(或峰面积),求出组分i的单位峰高(或峰面积)的组分含量或作出峰高和浓度的标准曲线。
当样品组分浓度变化不大时,可采用单位校正法。
当样品组分浓度变化很大时,则需预先用校准样作出浓度和峰高或峰面积的标准曲线,观察其标准曲线是不是通过原点的直线,即是否呈线性。
若呈线性,就可用单点校正法,按下面的公式计算:
——待测样品浓度,μL/L;
——待测样品峰高,mm;
——标准样品浓度,μL/L;
——标准样品峰高,mm;
——待测样品体积+甲酸体积,mL;
——待测样品体积,mL。
2.5.1.3方法的精度和注意事项
⑴以GDX103+H3PO42%为固定相,比用GDX101、PEGS、等作为固定相其保留时间短,且峰形对称。
⑵本法最小检测量为4μL/L,相对误差为%,相对标准偏差〈%(以乙酸计)。
⑶有机酸是一种强极性物质,沸点较高,由于担体对酸的吸附,常常引起酸峰拖尾和鬼峰的出现。
因此,取有机酸直接进样测定时,为了抑制酸的吸附,可采取以下措施。
①在样品中加入一定量的浓甲酸(相对密度,含量88%),使其甲酸加入量(体积)与样品的体积比为5:
100。
甲酸是一种一元羧酸,离解常数(×
10-4)大于其他任何一元羧酸,当含有甲酸的样品进入固定相时,担体表面的吸附中心位置被甲酸暂时占据,这样便抑制了C2~C5酸被担体的吸附。
此外,甲酸在FID上响应很低,故对其他组分的应答影响不大。
②酸的吸附还发生在接近进样口的地方,由于进样口常积累有碳质沉积物,通常采用蒸馏水清洗进样口,并用%磷酸-丙酮液来浸泡进样口,然后在约150℃的温度下将进样口烘烤4~8h。
③用%磷酸-丙酮液来浸泡柱口玻璃毛。
④在分析高浓度时,一定分析周期内注射水或15%甲酸液来洗涤被柱子吸附的酸。
⑤操作条件恒定以后,在进标准酸样或样品之前,用15%的甲酸液来冲洗柱子3~4次。
⑷柱子使用寿命大约4~6个月,一旦发现色谱峰出现拖尾或重复性差,则必须更换柱。
⑸尽管采取了一系列防止吸附的措施,但柱子的吸附问题还是不可能完全解决,特别是对于4000μL/L以上高浓度的酸样,如何克服吸附问题还值得更进一步研究。
⑹当检测器的灵敏度显着降低或更换新柱之后,重新做校正曲线。
2挥发性脂肪酸总量的比色测定法
2.5.2.1测定原理
含挥发性脂肪酸的样液,在加热的条件下,与酸性乙二醇作用生成酯,此酯与羧胺反应,形成氧肟酸。
在高铁试剂存在下,氧肟酸转化为高铁氧肟酸的棕红色络合物,其颜色的深浅在一个较大的范围内与反应初始物——挥发性脂肪酸的含量成正比,故可用比色法测定。
2.5.2.2测定方法
⑴试剂
①1:
1硫酸:
浓硫酸(相对密度,.)加到同体积蒸馏水中稀释配制。
②酸性乙二醇试剂:
取乙二醇.)与配制的稀硫酸混合。
③L的氢氧化钠:
称取180g氢氧化钠.)溶于水中,冷后以蒸馏水稀释至1L。
④10%硫酸羟胺溶液:
称取硫酸羟胺.),溶于100mL蒸馏水中。
⑤羟胺试剂:
量取L的氢氧化钠,与%的硫酸羟胺相混合。
⑥酸性氯化铁试剂:
将分析纯FeCl3·
6H2O溶于500mL水中,准确加入mL浓硫酸,并以蒸馏水稀释至1L。
⑵测定程序
①乙酸标准液的配制。
精确称取乙酸(分析纯,相对密度,含量%),以蒸馏水稀释至100mL,此溶液含乙酸10mg/mL。
准确吸取10mg/mL乙酸标准溶液、、、、、、,分别置于容量瓶内,以蒸馏水定容至刻度,摇匀,即得100μL/L、500μL/L、1000μL/L、1500μL/L、2000μL/L、2500μL/L、3000μL/L的乙酸标准系列液。
②标准曲线的绘制。
取相对密度的乙酸(分析纯)试剂,制成50mL/L、100mL/L、500mL/L、1000mL/L、1500mL/L、2500mL/L、3000mL/L的系列标准液,分别吸取mL分置于试管中(×
),每瓶中准确加入,于沸水浴中加热3min,然后立即以冷水冷却;
再加入羟胺试剂,充分摇匀,然后,充分振荡混匀,以蒸馏水定容,用721型分光光度计以500nm波长测定其光密度,绘制标准曲线,以横坐标表示浓度值,纵坐标表示光密度值。
③样品的测定。
以4000~10000r/min的离心条件,制取沼气发酵样品澄清液,吸取样液置于试管中(×
),准确加入mL酸性乙二醇试剂,充分混合,于沸水浴中加热3min,应避免试管与加热器壁直接接触。
然后立即将试管置于冷水中冷却。
加入羟胺试剂,并混匀,放置1min,然后全部倒进盛有10mL酸性氯化铁试剂的25mL容量瓶中,用蒸馏水定容,并充分摇匀,静置5min,用分光光度计以500nm波长测定光密度。
同样操作做空白试验1份。
计算
式中C——样液光密度值相应于标准曲线上挥发酸的含量,mg;
V——测定样液体积,mL;
——测定时液样的稀释倍数。
2.5.2.3注意事项
①此方法是挥发性脂肪酸总量的经验测定法,比蒸馏法测定更为简便、快速。
除150mg/L以下的低浓度范围外,其测定值相对误差与气相色谱法测定总值的相对误差相近。
②此法中的反应是在严格的pH值条件下进行的,最适pH值为±
。
pH值高于时,色度加剧,pH值低于时,颜色难以稳定,易消失。
③酸性己二醇试剂和羟胺试剂宜使用时配,也可在测定中配入。
例如,以加入己二醇和稀硫酸来代替酸性己二醇试剂,以硫酸羟胺和的氢氧化钠来代替羟胺试剂。
④如果所做的空白测定含量酸量超过200mg/L时必须用氢氧化钠蒸馏提纯己二醇。
⑤酸性氯化铁配制好后,应静置过夜,弃去沉淀。
⑥必须严格遵守操作规程,显色反应必须充分摇动。
⑦比色法没挥发性脂肪酸总量,方便快速,对于特定样品(特别是污水污泥体系)的准确度较高,适合于沼气发酵的常规分析。
3挥发性脂肪酸(VFA)的测定---------碳酸氢盐碱度和VFA分析的联合滴定法
?
挥发性脂肪酸(VFA)是厌氧消化过程的重要中间产物,甲烷菌主要利用VFA形成甲烷,只有少部分甲烷由CO2和H2生成。
但CO2和H2的生成也经过高分子有机物形成VFA的中间过程。
由此看来,形成甲烷的过程离不开VFA的形成,但是VFA在厌氧反应器中的积累能反映出甲烷菌的不活跃状态或反应器操作条件的恶化,较高的VFA(例如乙酸)浓度对甲烷菌有抑制作用。
因此在反应器运行中,出水VFA用作重要的控制指标。
在VFA测定中,常进行VFA总量测定,其单位以mmol/L或换算为按乙酸计,以单位mg/L表示。
对VFA中各种低级脂肪酸(乙酸、丙酸)的分别定量分析也是重要的,有时常需要知道以COD表示的VFA的量(即VFA以单位mgCOD/L)表示,此时也需要知道VFA中各种有机酸的含量,因此它们换算为COD的换算系数是不同的。
VFA包括甲酸、乙酸、丙酸、丁酸、戊酸、己酸以及它们的异构体。
在运转良好的高速厌氧反应器中,VFA中乙酸可占有很高的比例,但当反应器运行状态不好时,丙、丁酸浓度会上升。
(1)分析原理
厌氧处理中会产生大量的CO2,在反应器条件下(pH6~8之间),这些CO2主要以HCO3-形成存在。
这是厌氧处理中最重要的pH缓冲物,由HCO3-或主要