高中专题22化学反应速率和化学平衡疑难突破巅峰冲刺高考化学二轮专项提升Word文档格式.docx
《高中专题22化学反应速率和化学平衡疑难突破巅峰冲刺高考化学二轮专项提升Word文档格式.docx》由会员分享,可在线阅读,更多相关《高中专题22化学反应速率和化学平衡疑难突破巅峰冲刺高考化学二轮专项提升Word文档格式.docx(16页珍藏版)》请在冰豆网上搜索。
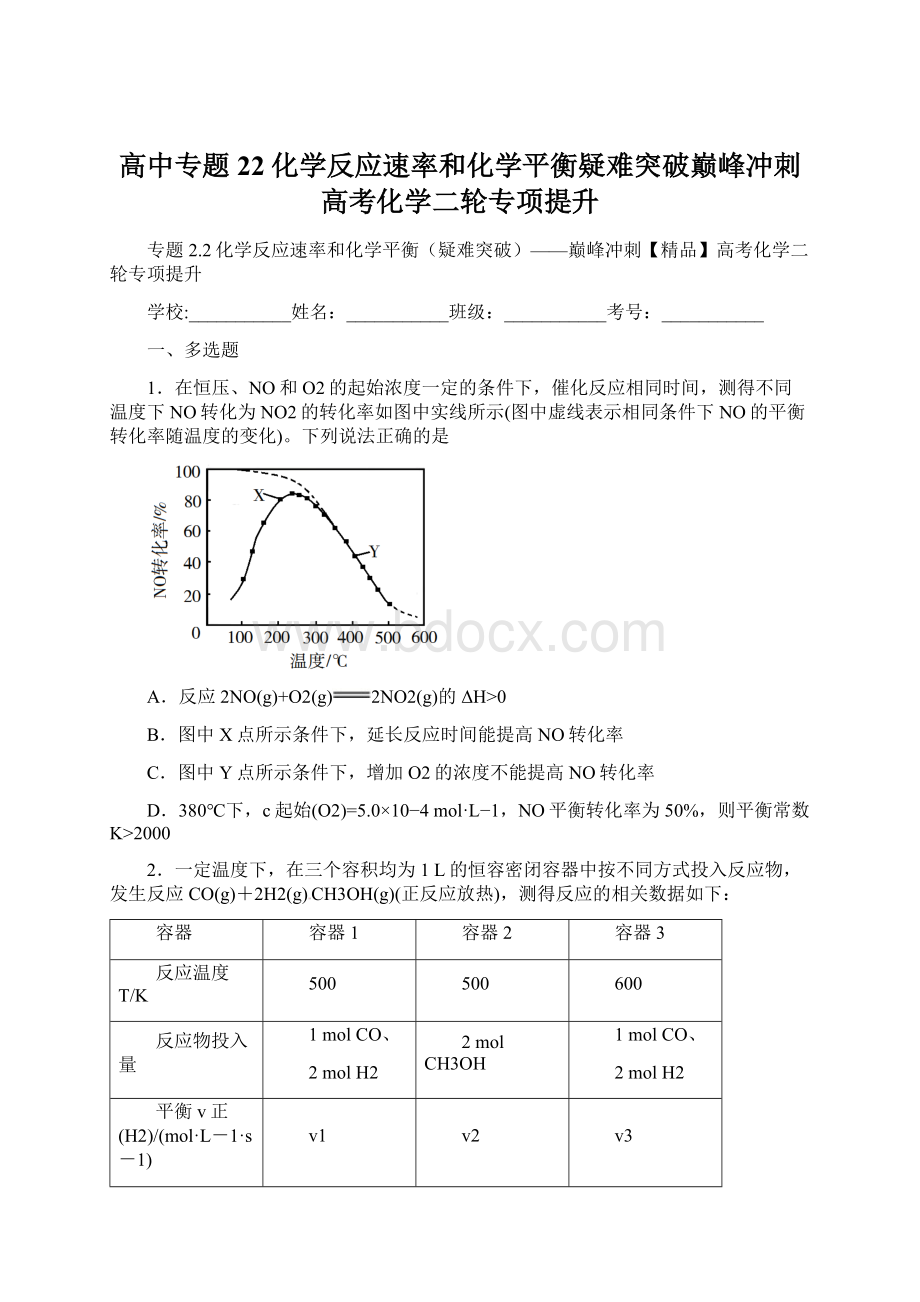
600
反应物投入量
1molCO、
2molH2
2molCH3OH
平衡v正(H2)/(mol·
L-1·
s-1)
v1
v2
v3
平衡c(CH3OH)/(mol·
L-1)
c1
c2
c3
平衡体系总压强p/Pa
p1
p2
p3
物质的转化率α
α1(CO)
α2(CH3OH)
α3(CO)
平衡常数K
K1
K2
K3
下列叙述正确的是()
A.v1<
v2,2c1>
c2B.α1(CO)>
α3(CO),v1<
C.p2>
2p3,K1<
K3D.c2>
2c3,α2(CH3OH)+α3(CO)<
1
二、单选题
3.已知反应式:
mX(g)+nY(?
)pQ(s)+2mZ(g),已知反应已达平衡,此时c(X)=0.3mol/L,其他条件不变,若容器缩小到原来的,c(X)=0.5mol/L,下列说法正确的是()
A.反应向逆方向移动B.Y可能是固体或液体
C.系数n>
mD.Z的体积分数减小
4.某兴趣小组将下表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,以研究硫酸铜的浓度对稀硫酸与锌反应生成氢气速率的影响。
下列判断错误的是( )
实验组别
混合溶液
A
B
C
D
E
F
4mol•L﹣1H2SO4/mL
30
V1
V2
V3
V4
V5
饱和CuSO4溶液/mL
0.5
2.5
5
V6
20
H2O/mL
V7
V8
V9
V10
10
A.V1=30,V6=10,V7=20
B.本实验利用了控制变量思想,变量为铜离子浓度
C.反应一段时间后,实验A中的金属呈灰黑色,实验F的金属呈现红色
D.该小组的实验结论是硫酸铜的量与生成氢气速率成正比
5.在容积不变的密闭容器中存在如下反应:
2SO2(g)+O2(g)2SO3(g)ΔH=-QkJ·
mol−1(Q>
0),某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
A.图Ⅰ研究的是t1时刻增大O2的浓度对反应速率的影响
B.图Ⅱ研究的是t1时刻加入催化剂后对反应速率的影响
C.图Ⅲ研究的是催化剂对平衡的影响,且甲的催化效率比乙高
D.图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较低
6.NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率。
将浓度均为0.020mol·
L-1NaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。
据图分析,下列判断不正确的是( )
A.40℃之前,温度升高反应速率加快,变蓝时间变短
B.40℃之后溶液变蓝的时间随温度的升高变长
C.图中b、c两点对应的NaHSO3的反应速率相等
D.图中a点对应的NaHSO3的反应速率为5.0×
10-5mol·
s-1
7.在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2molA和1molB,发生反应:
。
相关条件和数据见下表:
实验编号
实验Ⅰ
实验Ⅱ
实验Ⅲ
反应温度/℃
700
750
达平衡时间/min
40
n(D)平衡/mol
1.5
化学平衡常数
下列说法正确的是()
A.实验Ⅲ达平衡后,恒温下再向容器中通入1molA和1molD,平衡不移动
B.升高温度能加快反应速率的原理是降低了活化能,使活化分子百分数提高
C.实验Ⅲ达平衡后容器内的压强是实验Ⅰ的0.9倍
D.K3>
K2>
8.已知反应:
CH2=CHCH3(g)+Cl2(g)CH2=CHCH2Cl(g)+HCl(g)。
在一定压强下,按向密闭容器中充入氯气与丙烯。
图甲表示平衡时,丙烯的体积分数()与温度(T)、的关系,图乙表示反应的平衡常数K与温度T的关系。
则下列说法正确的是
A.图甲中
B.若在恒容绝热装置中进行上述反应,达到平衡时,装置内的气体压强将不变
C.温度T1、,Cl2的转化率约为33.3%
D.图乙中,线A表示正反应的平衡常数
9.在一个绝热定容的密闭容器中,1molA与2molB发生反应A(g)+2B(g)xC(g)+2D(g)△H=bkJ·
mol−1(b<0),下列说法正确的是
A.充分反应后,放出热量为bkJ
B.若x=1,容器中压强不变时不能判断反应达到平衡
C.当B和D的物质的量为1:
1时,表明该反应已达到平衡
D.达到平衡过程中,正反应速率可能是先增大再减小
三、计算题
10.由羟基丁酸生成丁内酯的反应如下:
HOCH2CH2CH2COOH+H2O
在298K下,羟基丁酸水溶液的初始浓度为,测得丁内酯的浓度随时间变化的数据如表所示。
回答下列问题:
21
50
80
100
120
160
220
0.024
0.050
0.071
0.081
0.090
0.104
0.116
0.132
(1)该反应在50~80min内的平均反应速率为_____。
(2)120min时羟基丁酸的转化率为______。
(3)298K时该反应的平衡常数_____。
(4)为提高羟基丁酸的平衡转化率,除适当控制反应温度外,还可采取的措施是______。
四、填空题
11.氮是地球上含量最丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
请回答下列问题:
(图中涉及物质为气态)
(1)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式______。
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:
N2(g)+3H2(g)2NH3(g)△H<0,其化学平衡常数K与温度t的关系如下表,
t/℃
200
300
400
K
请完成下列问题:
①试比较K1、K2的大小,K1______K2(填写“>”、“=”或“<”)。
②下列各项能作为判断该反应达到化学平衡状态的依据是_______(填序号字母)。
a.容器内N2,H2,NH3的浓度之比为1:
3:
2b.υ(N2)正=3υ(H2)逆
c.容器内压强保持不变d.混合气体的密度保持不变
③在400℃时,当测得NH3和N2,H2的物质的量分别为1mol和2mol,3mol时,则该反应的υ(N2)正______υ(N2)逆(填写“>,“=”或“<”)。
五、原理综合题
12.砷(As)与氮同一主族,As原子比N原子多两个电子层。
可以形成As2S3、As2O5、H3AsO3、H3AsO4,等化合物,有着广泛的用途。
(1)As的原子序数为______________________。
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。
写出发生反应的化学方程式____________。
该反应需要在加压下进行,原因是___________。
(3)已知:
As(s)+H2(g)+2O2(g)=H3AsO4(s)
H2(g)+O2(g)=H2O(l)
2As(s)+O2(g)=As2O5(s)
则反应As2O5(s)+3H2O(l)=2H3AsO4(s)的=______________________。
(4)298K肘,将2OmL3xmol·
L-1Na3AsO3、20mL3xmol·
L-1I2和20mLNaOH溶液混合,发生反应:
AsO33-(aq)+I2(aq)+2OH-AsO43-(aq)+2I-(aq)+H2O(l)。
溶液中c(AsO43-)与反应时间(t)的关系如图所示。
①下列可判断反应达到平衡的是_____(填标号)。
a.v(I-)=2v(AsO33-)b.溶液的pH不再变化
c.c(I-)=ymol·
L-1d.c(AsO43-)/c(AsO33-)不再变化
②tm时,v正____v逆(填“大于”、“小于”或“等于”)。
③)tm时v逆____tn时v逆(填“大于”、“小于”或“等于”),理由是___________。
④若平衡时溶液的pH=14,则该反应的平衡常数为_____(用x、y表示)。
参考答案
1.BD
【详解】
A.随温度升高NO的转化率先升高后降低,说明温度较低时反应较慢,一段时间内并未达到平衡,分析温度较高时,已达到平衡时的NO转化率可知,温度越高NO转化率越低,说明温度升高平衡向逆方向移动,根据勒夏特列原理分析该反应为放热反应,∆H<
0,故A错误;
B.根据上述分析,X点时,反应还未到达平衡状态,反应正向进行,所以延长反应时间能提高NO的转化率,故B正确;
C.Y点,反应已经达到平衡状态,此时增加O2的浓度,使得正反应速率大于逆反应速率,平衡向正反应方向移动,可以提高NO的转化率,故C错误;
D.设NO起始浓度为amol/L,NO的转化率为50%,则平衡时NO、O2和NO2的浓度分别为0.5amol/L、(5×
10-4-0.25a)mol/L、0.5amol/L,根据平衡常数表达式K=>
=2000,故D正确;
故选BD。
【点睛】
解本题时需要注意:
实线中在最高点之前反应没有达到平衡状态,主要讨论温度对化学反应速率的影响;
最高点之后反应达到平衡状态,可以研究温度对化学平衡的影响。
2.BD
【解析】
【分析】
采用比较的方法分析,对照容器的特点,将容器1和容器2对比,将容器1和容器3对比。
容器2中加入2molCH3OH等效于在相同条件下反应物投入量为1molCO、2molH2,容器2中起始反应物物质的量为容器1的2倍,容器2相当于在容器1达到平衡后增大压强,将容器的体积缩小到原来的一半,增大压强反应速率加快,则v1<
v2,增大压强平衡向正反应方向移动,平衡时c2>2c1,p2<2p1,α1(CO)+α2(CH3OH)<1;
容器1和容器2的温度相同,则K1=K2;
容器3相当于在容器1达到平衡后升高温度,升高温度反应速率加快,则v1<v3,