初中毕业升学考试福建漳州卷化学含答案及解析1Word文档格式.docx
《初中毕业升学考试福建漳州卷化学含答案及解析1Word文档格式.docx》由会员分享,可在线阅读,更多相关《初中毕业升学考试福建漳州卷化学含答案及解析1Word文档格式.docx(14页珍藏版)》请在冰豆网上搜索。
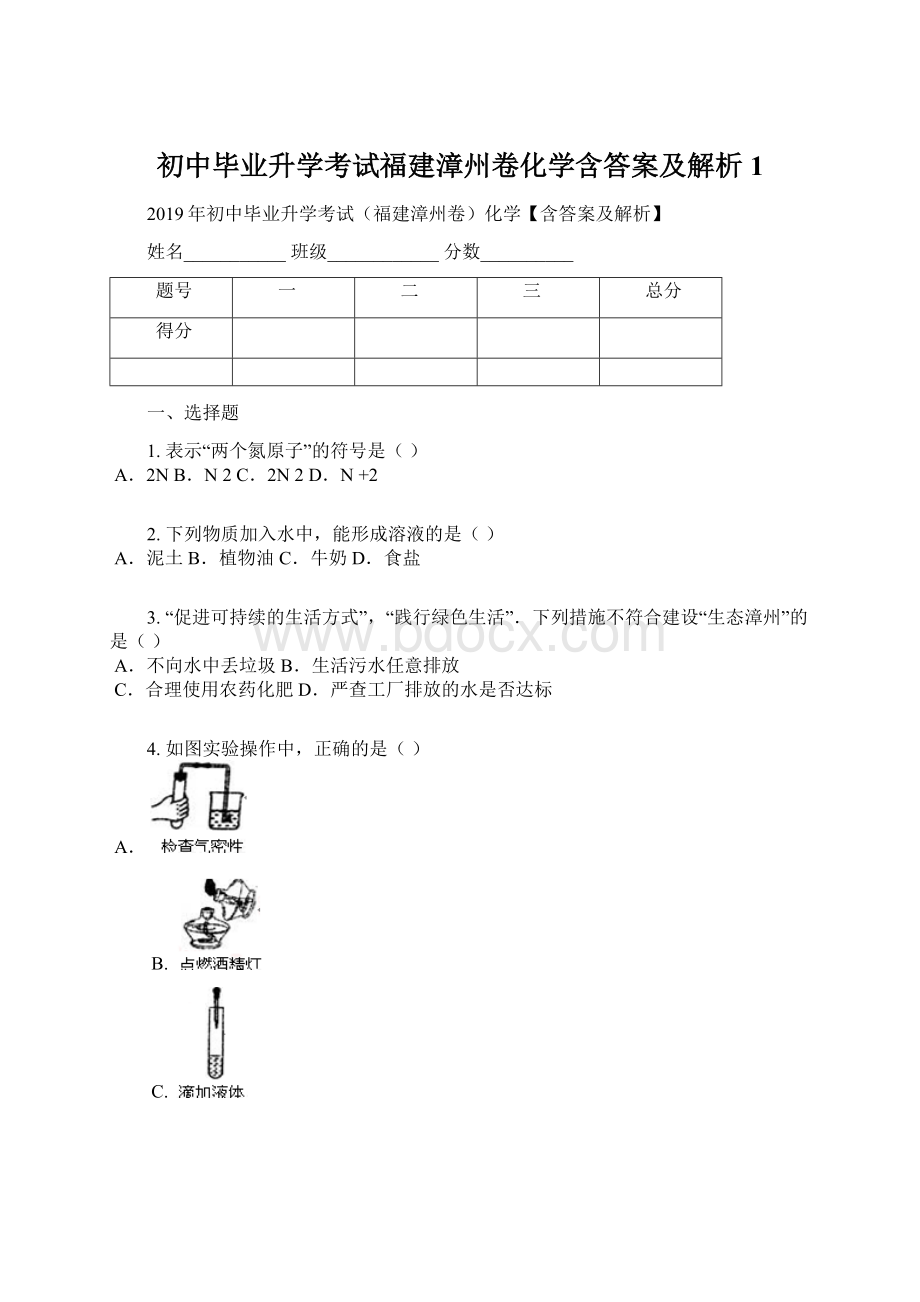
A.泥土B.植物油C.牛奶D.食盐
3.“促进可持续的生活方式”,“践行绿色生活”.下列措施不符合建设“生态漳州”的是()
A.不向水中丢垃圾B.生活污水任意排放
C.合理使用农药化肥D.严查工厂排放的水是否达标
4.如图实验操作中,正确的是()
A.
B.
C.
D.
5.祖国文化灿烂辉煌.有关诗句“春蚕到死丝方尽,蜡炬成灰泪始干”,理解错误的是()
A.蚕“丝”是天然纤维
B.“蜡炬成灰”只发生化学变化
C.“泪”指液态蜡
D.“灰”是指蜡燃烧产生的CO2等物质
6.下列物质所对应的俗名,错误的是()
A.NaOH烧碱B.Na2CO3纯碱C.CaO生石灰D.NaHCO3火碱
7.漳州市诏安县红星乡是“长寿之乡”,与当地富硒有关.如图是硒(Se)原子的结构示意图,下列描述错误的是()
A.是相对稳定结构B.核电荷数为34
C.共有4个电子层D.第二层上有8个电子
8.下列情况中,铁钉容易生锈的是()
A.在干燥的空气中B.浸没在蒸馏水中
C.部分浸入食盐水中D.浸没在植物油中
9.运用如图所示装置探究可燃物的燃烧条件,下列说法错误的是()
A.①②现象对比,说明温度达到可燃物的着火点是燃烧条件之一
B.①③现象对比,说明有氧气参与是燃烧条件之一
C.白磷的着火点低于80℃
D.热水只起到加热作用
10.下列说法错误的是()
A.点燃H2前,要先检验其纯度
B.堆放易燃易爆物,不要堆得过密
C.金刚石、石墨和C60的化学性质相同
D.稀释浓硫酸时,要把浓硫酸沿器壁缓慢注入水里,并不断搅拌
11.下列实验方案不能达到实验目的是()p
12.实验目的实验方案A.除去硫酸锌溶液中混有的少量硫酸铜往溶液中加入足量的锌粉,过滤B.检验氧气将带火星的木条伸入集气瓶中,看是否复燃C.鉴别氢气和氮气闻气体气味,根据气体气味判断D.鉴别二氧化碳和一氧化碳点燃,看是否能燃烧<
p>
A.AB.BC.CD.D
13.下列现象描述正确的是()
A.碳和氧化铜反应后,黑色的氧化铜变成灰色
B.往硫酸铜溶液中滴加氢氧化钠溶液有白色沉淀生成
C.往5%过氧化氢溶液中加入二氧化锰有大量氧气生成
D.硫在氧气中燃烧,产生明亮的蓝紫色火焰,生成有刺激性气味的气体
14.甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是()
A.甲物质的溶解度大于乙物质的溶解度
B.两种物质的溶解度都随着温度的升高而增大
C.t1℃时,60g甲加入到100g水中,充分溶解,得到160g溶液
D.甲、乙的饱和溶液从t2℃降温到t1℃,析出晶体的质量:
甲一定小于乙
15.下列有关说法,错误的是()
A.酸雨是pH<7的降雨
B.白色污染是废弃塑料造成的污染
C.将二氧化碳转化为新型燃料,有利于减缓温室效应
D.运用CNG(压缩天然气)作为汽车燃料,可以减少汽车尾气对空气的污染
16.如图表示四种物质的密闭容器中反应一段时间后质量的变化,则其化学反应表达式是()
A.a+b→c+dB.c→a+bC.a+b
cD.c
a+b
二、填空题
17.
(1)喝口水缓解考试压力,我带的开水是______(填“纯净物”或“混合物”),它已经通过______降低了水的硬度.
(2)化学考试结束回到家,啊,餐厅里飘来了饭的香味,这是因为______(从微观角度解释)…先吃一碗带汤排骨,再吃碗干饭拌青菜.这些食物中除了水、无机盐和油脂外,主要含有的营养素是______、______、______.
(3)家里煮菜用液化石油气,除了石油外,化石燃料还有______、______.液化石油气的主要成分C4H8完全燃烧的产物是二氧化碳和水,则其完全燃烧的化学方程式是______.
18.充有的蒸汽的高压钠灯发出的黄光射程远,透雾能力强,常用于道路和广场的照明.钠的化学性质活泼,常温下可以与氧气、水反应,在实验室里,金属钠保存在煤油中,用镊子从煤油中取出金属钠,放在滤纸上,用小刀切下一小块,投入盛有水(滴有酚酞溶液)的烧杯中,发现钠块浮在水面上,很快熔化成银白色小球,四处游动,发出嘶嘶的响声,偶有火星出现,溶液变成红色.依据提供的信息,回答下列问题.
(1)“钠保存在煤油中”说明钠具有的化学性质是_______________.
(2)“钠块浮在水面上”说明钠具有的物理性质是_______________.
(3)“溶液变成红色”说明钠与水反应的生成物中含有_______________性的物质.
(4)根据所学知识解释钠“熔化成银白色小球”的原因是_______________.
19.回收利用是保护金属资源的一条有效途径,某工业废料含氧化铜和氧化铁,经过处理后可得到铜和硫酸亚铁溶液.主要流程如图:
已知:
CuO+H2SO4═CuSO4+H2OFe+Fe2(SO4)3═3FeSO4
(1)流程Ⅰ中氧化铁发生反应的化学方程式是_____________.
(2)流程Ⅲ充分反应后,还应有的实验操作是_____________.
(3)A﹣E中,含有铁、铜两种元素的是_____________(填字母)
20.世界是物质的,物质是由元素组成的,从H、C、N、O、Ca中选择适当的元素组成物质填空.
(1)最简单的有机化合物是_____________;
(2)具有可燃性的气体单质是_____________;
(3)可用于人工降雨的物质是_____________;
(4)有毒且能作为气体燃料的氧化物是_____________,它燃烧的化学方程式是_____________;
(5)可用来改良酸性土壤的碱是_____________,它与稀盐酸反应的化学方程式是_____________。
21.对物质进行归纳、分类,是学习化学的重要方法.
(1)如图是一位同学整理的有关CO2的知识网络图.
物质①的化学式是_________;
物质②的组成元素有_________种;
物质③中的阳离子符号是_________;
写出CO2转化为物质④的化学方程式_________;
物质⑤中碳元素的化合价是_________价。
(2)根据下列信息回答问题.
①能与碱反应生成盐和水的氧化物叫做酸性氧化物.
②SO2+2NaOH═Na2SO3+H2O
以上物质中属于酸性氧化物的是_________,初中学过的_________也是酸性氧化物;
酸性氧化物一般是_________氧化物(填“金属”或“非金属”)
22.如图是某反应的微观粒子示意图.
(1)根据化学反应的本质,反应物的方框内还应补充的粒子及数目是_________.
A.一个
B.两个
C.一个
D.两个
(2)两种生成物分子的共同之处是_________,该反应属于基本反应类型中的_________反应.
23.
(1)写出图1A中一种玻璃仪器的名称_________.
(2)用高锰酸钾制取氧气时,选用的发生装置是_________(填序号,下同),收集装置是_________;
装药品时还需要的实验用品是_________,反应的化学方程式是_________.
(3)如图2是a、b、c三部分组成的实验装置图.a处反应的化学方程式是_________;
b处的现象是_________;
一段时间后,c处0以上的棉花团比0以下的棉花团变红色的个数_________(填“多”或“少”),原因是_________.
24.漳州小吃手抓面,制作时要用发到大树碱,大树碱的主要成分是K2CO3.为了测定大树碱中K2CO3的质量分数,小文同学进行了如下实验;
(1)用托盘天平称取10g大树碱样品,在称量过程中发现天平指针如图所示,则此时应进行的操作是_________.
(2)用量筒量取一定量的水,为了准确量取水的体积,还需要使用的仪器是_________.
(3)把大树碱样品和水加入烧杯中,用玻璃棒搅拌,使大树碱完全溶解,玻璃棒的作用是_________.
(4)向配好的溶液中逐渐加入CaCl2溶液,生成1g沉淀(假设大树碱中其它成分不参与反应,反应的化学方程式为CaCl2+K2CO3═CaCO3↓+2KCl).计算大树碱中K2CO3的质量分数.
(5)小文同学在配制好溶液后,发现纸片上还有残留固体,则计算出的大树碱K2CO3的质量分数_________(填“偏大”或“偏小”)
三、探究题
25.在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有_________产生,反应的化学方程式是_________.
【发现问题】为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀.
【实验验证1】小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因.p
26.试管(盛有同体积同浓度的盐酸)①②③④镁条长度1cm2cm3cm4cm相同的实验现象(省略题干现象)快速反应,试管发热,镁条全部消失沉淀量差异(恢复至20℃)无少量较多很多<
【得出结论】镁条与盐酸反应产生白色沉淀与_________有关.
【追问】白色沉淀是什么物质?
【查阅资料】①20℃时,100g水中最多能溶解氯化镁54.8g.
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸.
【做出猜想】猜想一:
镁;
猜想二:
氯化镁;
猜想三:
氢氧化镁,猜想的依据是_________(用化学方程式表示).
【实验验证2】将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
p
27.试管操作现象结论A加入足量盐酸_________,白色沉淀_________猜想一不正确,但这种白色沉淀能溶于盐酸B加入足量水白色沉淀_________猜想二不正确C加入适量稀硝酸白色沉淀消失原白色沉淀中含有的离子是:
Mg2+、_________继续滴加几滴硝酸银溶液出现大量白色沉淀<
【拓展延伸】足量镁与盐酸反应过程中,溶液会经历从酸性到碱性并且碱性逐渐增强的过程,从而促使白色碱式氯化镁的生成.
参考答案及解析
第1题【答案】
第2题【答案】
第3题【答案