无机非金属推断题Word格式.docx
《无机非金属推断题Word格式.docx》由会员分享,可在线阅读,更多相关《无机非金属推断题Word格式.docx(19页珍藏版)》请在冰豆网上搜索。
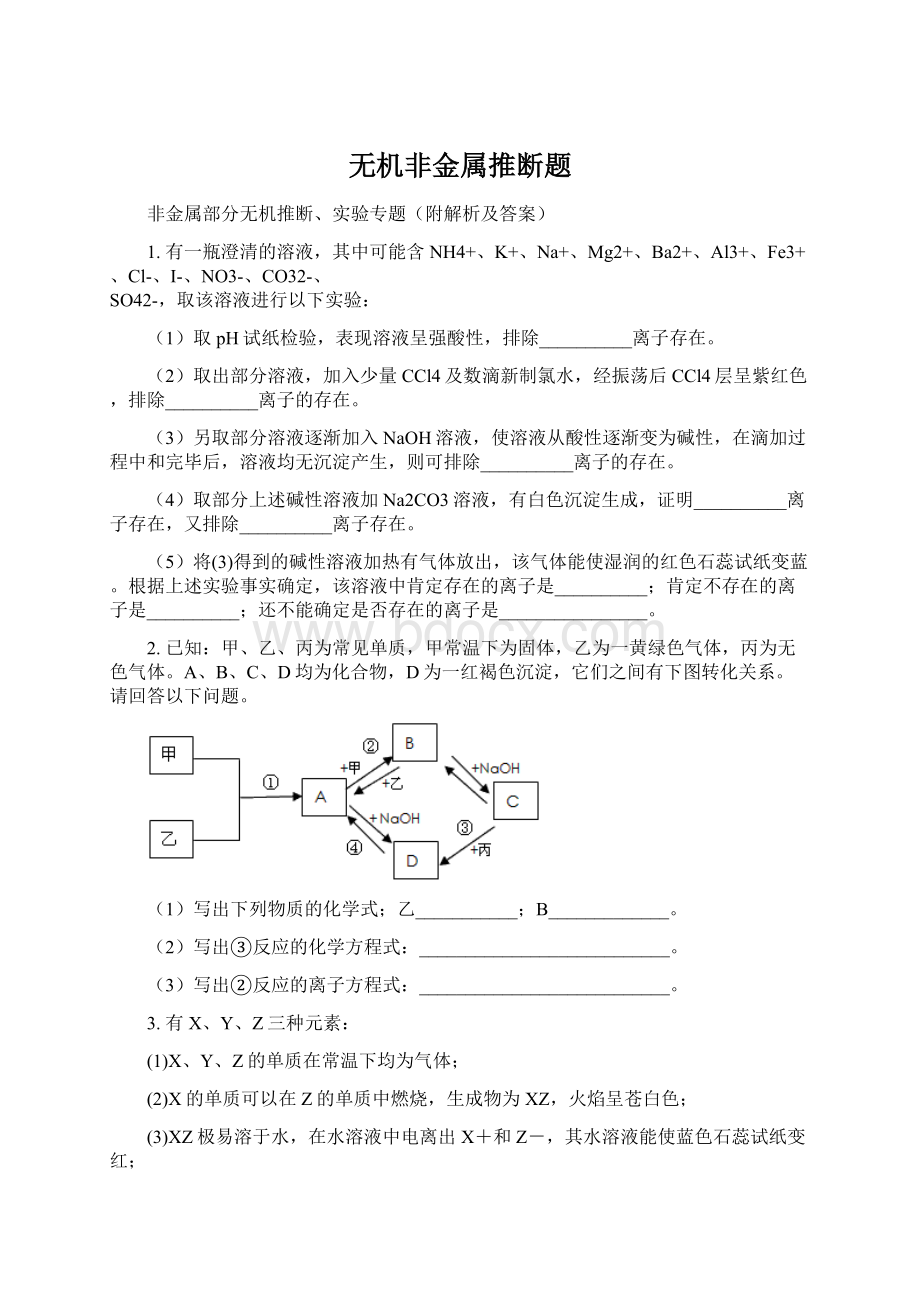
请回答以下问题。
(1)写出下列物质的化学式;
乙___________;
B_____________。
(2)写出③反应的化学方程式:
___________________________。
(3)写出②反应的离子方程式:
3.有X、Y、Z三种元素:
(1)X、Y、Z的单质在常温下均为气体;
(2)X的单质可以在Z的单质中燃烧,生成物为XZ,火焰呈苍白色;
(3)XZ极易溶于水,在水溶液中电离出X+和Z-,其水溶液能使蓝色石蕊试纸变红;
(4)每2个X2分子能与1个Y2分子化合成2个X2Y分子,X2Y常温下为液体;
(5)Z单质溶于X2Y中,所得溶液具有漂白性。
试写出其元素符号:
X________,Y________,Z________,以及化合物的分子式:
XZ________,
X2Y________。
4.氮元素在生命活动中扮演着十分重要的角色,回答下列与氮及
其化合物有关的问题。
Ⅰ.为了提高农作物的产量,德国化学家哈伯、波施等成功地开发了将氮气转化为氨气的生产工艺。
请用化学方程式表示工业合成氨的反应原理:
____________________________________;
Ⅱ.氨气通入水中可制得氨水,氨水能使无色的酚酞试液变红。
请用电离方程式表示其原因:
__________________________________
Ⅲ.氨气可以跟多种物质发生反应,请将如图实验中有关反应的化学方程式填在横线上:
__________________________;
______________________。
5
.下图中各物质均为中学化学中的常见物质,其中A、E、J三种物质为单质,D的摩尔质量比F小16,F为红棕色气体;
K是一种两性氧化物,可用KSCN检验I中的阳离子。
它们的相互转化关系如下图所示(图中部分产物、反应条件未列出)。
回答下列问题:
(1)B的化学式可能为
________;
反应①的反应类型为
(2)F与C反应的化学方程式为________________;
(3)反应③的化学方程式为
____________。
反应④中,当有1
mol
E生成时,转移的电子数为________mol。
(4)H与L稀溶液反应的离子方程式为
____________________。
6.已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使湿润红色石蕊试纸变蓝的气体,
它们之间能发生如下反应:
①A+H2O→B+C
②C+F→D
③D+NaOH
F+E+H2O
(1)写出它们的化学式:
A________、B________、C________、D________、E________、F________;
(2)写出各步反应的化学方程式,并指出反应①的氧化剂和还原剂。
①_______________,氧化剂________、还原剂________。
②___________________。
7.已知A、B、C、D为气体,其中A呈黄绿色,D极易溶于水,形成的溶液可使酚酞变红。
它们之间的转化关系如下图所示:
(1)将B点燃,把导管伸入盛满A气体的集气瓶,可以观察到的实验现象有(填序号)_________________
。
①放热
②黄绿色褪去
③瓶口有白烟
④瓶口有白雾
⑤安静燃烧,发出黄色火焰
⑥安静燃烧,发出苍白色火焰
(2)实验室制D的化学方程式为
___________________________________________________
(3)实验室可用如图所示装置收集D,下列叙述正确的_________________(填序号)。
①
D气体不能用排水法收集
②
干燥管里盛有碱石灰
③
右图中的a为浸有稀H2SO4的棉花
(4)工业生产D的化学方程式是_____________________________________________________________
(5)检验E中阳离子的方法是:
取少量E于试管中,_______________________________________________
8.下图表示某淡黄色固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。
B和C的相对分子质量相差16,化合物D是重要的工业原料。
(1)单质A的名称
________。
(2)写出E与A的氢化物反应生成A的化学方程式_______________________________________。
(3)写出一个由D生成B的化学方程式_________________________________________________。
9.已知CO和H2的混合气体称为水煤气,可由碳与水蒸气在高温下反应生成。
如下图:
已知:
单质E可作为半导体材料,化合物F是有毒的氧化物,C为液态。
据此,请填空:
(1)氧化物A是
_________________________________
(2)化合物F是
_________________________________
(3)反应②的化学方程式是______________________________________________________
(4)反应③的化学方程式是______________________________________________________
10.某化学小组为了证明SO2和Cl2的漂白性,设计了如下图所示的实验装置:
(1)他们制备Cl2依据的原理是:
MnO2
+
4HCl(浓)
MnCl2
2H2O
Cl2↑,应选用上图A、E装置中的__________(填序号)制Cl2,反应中浓盐酸所表现出的性质是______________
、_____________
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的液体加热,B试管中的现象是____________________________________。
(3)NaOH溶液分别与两种气体反应的离子方程式是
________________________________________、_______________________________________。
(4)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。
查阅资料得知:
两种气体按体积比1:
1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是__________________________________________________。
11.某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等。
(1)氯气可以用于漂白、消毒的原因是氯气能与水作用形成具有________性的次氯酸,相关反应的离子方程式为________________________;
(2)在调查某室外游泳池夏季池水消毒情况时,小组成员了解到,该游泳池每周一上午8∶00换水,然后通入氯气消毒,通常游泳池水的含氯量控制在0.5
mg/L至1.0
mg/L
之间时,效果最好。
上图是该小组测定的每天19∶00时游泳池中水的含氯量,有哪几天使用游泳池不卫生____________________
(3)你认为哪几天的天气炎热、阳光强烈________,说出一种理由是____________
(4)在对游泳池水中通入氯气消毒时,当发生氯气泄漏,应立即关闭氯气罐,还应采取下列自救方法_______。
(选填序号)
A.
用湿润的毛巾捂住口鼻跑向低处
B.
用浸湿小苏打或肥皂水的毛巾捂住口鼻跑向高处
C.
用浸湿浓氨水的毛巾捂住口鼻匍匐跑至安全处
D.
用浸湿食盐水的毛巾捂住口鼻顺风跑至安全处
(5)小型游泳池通常使用漂白液(NaClO溶液)而非氯气来消毒池水,试举出使用漂白液而非氯气消毒的一项理由________________________。
12.回答下列问题。
(1)浓硫酸与木炭在加热条件下反应的化学方程式是____________________
(2)试用下图所列各种装置设计一个实验来验证上述反应所产生的各种产物。
这些装置的连接顺序,按产物气流从左到右的方向是(填装置的编号):
_________→________→________→__________。
(3)实验时可观察到装置①中A瓶的溶液褪色c瓶的溶液不褪色。
A瓶溶液的作用是____________________________,
B瓶溶液的作用是______________________________________,
C瓶溶液的作用是__________________________________________。
(4)装置②中所装的固体药品是______________,可验证的产物是____________
(5)装置③中所盛溶液是_______________,可以验证的产物是___________。
13.喷泉是一种常见的自然现象,其产生的原因是存在压强差。
制取氨气并完成喷泉实验(图中夹持装置均已略去)。
①写出实验室制取氨气的化学方程式:
__________________________
②收集氨气应使用___________法,要得到干燥的氨气可选用_____________做干燥剂。
③用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是___________________
该实验的原理是__________________________________________________
④如果只提供如图2的装置,请说明引发喷泉的方法_______________________________________
14.已知二氧化硫可使高锰酸钾溶液褪色,反应的化学方程式为:
5SO2+2KMnO4+2H2O====