金属的化学性质易错难中考真题汇编.docx
《金属的化学性质易错难中考真题汇编.docx》由会员分享,可在线阅读,更多相关《金属的化学性质易错难中考真题汇编.docx(27页珍藏版)》请在冰豆网上搜索。
金属的化学性质易错难中考真题汇编
金属的化学性质易错(难)中考真题汇编
一、初中化学金属的化学性质选择题
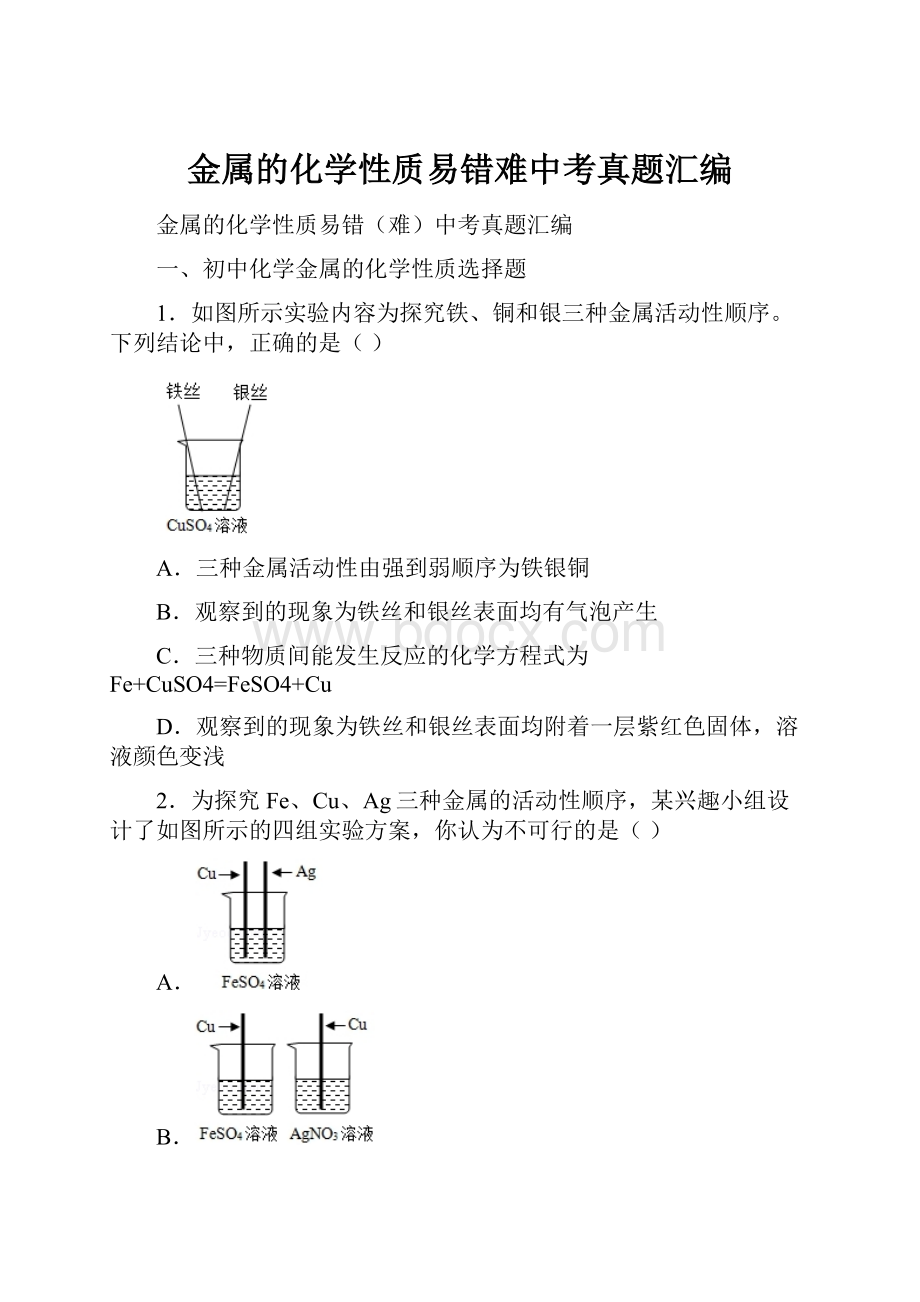
1.如图所示实验内容为探究铁、铜和银三种金属活动性顺序。
下列结论中,正确的是()
A.三种金属活动性由强到弱顺序为铁银铜
B.观察到的现象为铁丝和银丝表面均有气泡产生
C.三种物质间能发生反应的化学方程式为Fe+CuSO4=FeSO4+Cu
D.观察到的现象为铁丝和银丝表面均附着一层紫红色固体,溶液颜色变浅
2.为探究Fe、Cu、Ag三种金属的活动性顺序,某兴趣小组设计了如图所示的四组实验方案,你认为不可行的是()
A.
B.
C.
D.
3.将锌粉加入到硫酸铜溶液中,一段时间后过滤,得蓝色滤液和滤渣。
滤渣的成分是
A.ZnB.CuC.Zn、CuD.ZnSO4、Cu
4.有X、Y、Z三种金属,把它们投入稀盐酸中,只有Z表面有气泡冒出,把X投入到Y的硝酸盐溶液中,X表面有Y析出,X、Y、Z三种金属的活动性由强到弱的顺序是:
A.Z>X>YB.Y>X>ZC.X>Y>ZD.X>Z>Y
5.下列关于金属及金属材料的说法,正确的是( )
A.镁条、铝片、铜丝均能在空气中燃烧
B.铝合金门窗是用纯的金属铝材料制成的
C.人类使用铝的年代早于铜、铁
D.武德合金的熔点低,可作保险丝
6.等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是()
A.M、N两种金属中较活泼的是N
B.生成H2的质量M<N
C.相对原子质量较小的是M
D.产生H2的速率N>M
7.在FeCl2和CuCl2的混合溶液中加入Zn粉。
下列说法错误的是( )
A.若反应完成后Zn无剩余,溶液中若有CuCl2,则一定有FeCl2
B.若反应完成后Zn无剩余,溶液中若无CuCl2,则可能有FeCl2
C.若反应完成后Zn有剩余,则溶液中有ZnCl2,无CuCl2和FeCl2
D.若反应完成后Zn有剩余,则溶液中有ZnCl2,无CuCl2,可能有FeCl2
8.将一定质量的铝粉和锌粉加入到硝酸铜溶液中,充分反应后过滤,得到滤渣和滤液。
下列说法正确的是( )
A.若滤液为蓝色,则滤渣中定有锌和铜
B.若滤渣中加盐酸没有气泡产生,则滤液一定为无色
C.若滤液中有硝酸锌,则滤渣中一定没有铝和锌
D.若滤渣中加盐酸有气泡产生,则滤渣中一定有锌和铜
9.为比较X、Y、Z三种金属活动性大小,进行如图实验。
实验结论正确的是( )
金属X产生氢气金属Y无明显变化金属Y表面析出银金属Z无明显变化
A.
B.
C.
、
D.
、
10.将a、b、c三种金属分别投入稀盐酸中,只有b溶解并产生气泡;把a和c分别放入硫酸铜溶液中,在a表面有铜析出,c没有变化。
则a、b、c的金属活动性顺序是( )
A.c>b>a
B.b>a>c
C.a>c>b
D.b>c>a
11.向一定量的FeSO4和CuSO4的混合溶液中加入一定质量的锌粉,充分反应后过滤,得滤液和滤渣,向滤渣中加入稀盐酸,有气泡产生。
由此判断,下列说法错误的是()
A.滤液的颜色呈蓝色B.滤液中可能存在Fe2+
C.滤液中一定含有Zn2+D.滤渣中一定含有Fe和Cu,可能含有Zn
12.将过量的铁粉放入含AgNO3和Zn(NO3)2的混合溶液里,搅拌,使其充分反应后过滤,滤纸上留下的金属是
A.只有AgB.Fe、ZnC.Fe、AgD.Ag、Zn、Fe
13.有X、Y、Z三种金属,只有Y在自然界主要以单质形式存在,如果把X放入Z的硫酸盐溶液中,X表面有Z析出.据此判断这三种金属的活动性由强到弱的顺序为( )
A.Y、X、ZB.Z、X、YC.Y、Z、XD.X、Z、Y
14.下列化学反应属于复分解反应是( )
A.CH4+2O2
CO2+2H2OB.3Fe+2O2
Fe3O4
C.NaOH+HCl═NaCl+H2OD.H2CO3═CO2↑+H2O
15.下图所示反应,有关说法的错误的是()
A.铝丝需要砂纸打磨
B.溶液由蓝色变为无色
C.金属活动性强弱:
Al>Cu
D.反应的化学方程式为:
Al+CuSO4=Cu+AlSO4
16.硬铝的组成金属有铝、镁、铜、锰等。
已知:
锰丝放入稀硫酸中,有气泡产生;锰丝放入硫酸铝溶液中,表面没有金属析出。
结合我们所学金属再溶液中的活动性顺序,下列有关金属的活动性强弱判断错误的是
A.Mn强于CuB.Al强于Mn
C.Mg强于AlD.Mn强于Mg
17.把金属X放入AgNO3溶液中,X表面有银白色固体析出;若放入FeSO4溶液中,无明显现象。
则X、Ag、Fe三种金属活动性由强到弱的顺序正确的是( )
A.Ag、X、FeB.X、Fe、AgC.Fe、Ag、XD.Fe、X、Ag
18.把一根洁净的铁钉放入稀硫酸中,①在铁钉表面产生气泡;②溶液由无色逐渐变为浅绿色③铁钉质量减轻;④溶液的质量增加。
以上叙述正确的是( )
A.①②③B.①③④C.①④D.①②③④
19.在已调平的托盘天平两边的等质量烧杯中各倒入质量相等、溶质质量分数相同的稀硫酸。
再向两烧杯中分别放入质量相等的铝和镁,反应完毕后,若天平失去平衡,则下列情况可能的是:
①铝、镁均有剩余;②铝、镁均耗尽;③镁耗尽,而铝有剩余
A.仅②
B.①②
C.①③
D.②③
20.仅用下列各组试剂无法完成验证Zn,Cu,Ag三种金属活动性顺序的是()
A.Zn、Ag、CuSO4溶液B.Cu、ZnSO4溶液、AgNO3溶液
C.Zn、Ag、稀硫酸、ZnSO4溶液D.Zn、Cu、稀硫酸、AgNO3溶液
21.向一定质量FeCl2和CuCl2的混合溶液中加入锌粉。
反应过程中,混合物中溶液的质量与加入锌的质量关系如图所示。
有关该反应过程中混合物中的溶液和固体,下列说法正确的是( )
A.a点时,溶液中只含有两种溶质
B.c点时,向固体中滴加稀盐酸,无气泡产生
C.d点时,溶液中的溶质为ZnCl2
D.e点时,固体中只含有2种物质
22.将等质量的镁、铁、锌,分别放入三份质量分数相同的稀盐酸中,反应生成的氢气质量与反应时间的关系如图所示。
根据图中信息,下列判断不正确的是( )
A.图线X表示镁的反应情况
B.铁消耗稀盐酸的质量最大
C.锌一定过量
D.镁一定过量
23.向Cu(NO3)2、AgNO3、Al(NO3)3的混合溶液中加入一定量的Zn,充分反应后过滤。
关于滤渣和滤液有以下四种说法,正确的有()
①滤渣的组成有三种可能②滤液中一定含有Zn(NO3)2和Al(NO3)3
③向滤渣中加入稀盐酸一定有气泡产生④反应前后溶液的质量可能相等
A.1个B.2个C.3个D.4个
24.为验证Mg、Cu、Ag三种金属的活动性强弱,某化学兴趣小组设计了如图所示的四个实验。
其中不必进行的实验是( )
A.
B.
C.
D.
25.某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的锌粉进行处理,并绘制参加反应的锌与溶液中溶质种类的关系图(如图所示),下列说法中不正确的是( )
A.Cu的活动性比Ag强,只用盐酸无法探究两者活动性强弱
B.当溶质种类为1种时,金属单质种类可能为1种
C.c~d间(不含两点)的溶液中金属离子为Zn2+、Cu2+
D.从m1变化到m2时,溶液中硝酸铜的质量分数变大
26.X、Y、Z三种金属及化合物间发生如下化学反应:
Y+ZCl2═Z+YCl2X+ZCl2═Z+XCl2Y+2HCl═YCl2+H2↑X与稀盐酸不反应.则X、Y、Z三种金属的活动性由强到弱的顺序是()
A.Z>Y>XB.X>Y>ZC.Y>X>ZD.Y>Z>X
27.向盛有一定质量稀硫酸的烧杯中加入过量的锌粉,下列4个图象中,能正确反映对应变化关系的是( )
A.
B.
C.
D.
28.向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入mgZn,充分反应后过滤,将滤渣洗涤、干燥后再称量,得到的质量为mg。
据此,下列说法不正确的是()
A.取反应后的滤液观察,滤液可能呈蓝色
B.取反应后的滤液滴加稀盐酸,有白色沉淀产生
C.取滤渣滴加稀硫酸,可能有气泡产生
D.滤渣中的物质至少有两种
29.为比较A、B、C三种金属的活动性,某同学设计了如图所示实验,由此判断三种金属活动性由强到弱的顺序是( )
A.A>C>BB.A>B>CC.C>A>BD.B>C>A
30.向AgNO3溶液中加入一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液。
关于该滤渣和滤液有下列四种说法:
①向滤渣中加入稀盐酸,一定有气泡产生。
②向滤液中加入稀盐酸,一定有沉淀产生。
③滤渣中一定含有Ag。
④滤液中一定含有Fe(NO3)2,一定不含AgNO3,可能含有Al(NO3)3
以上说法正确的个数为()
A.0个B.1个C.2个D.3个
【参考答案】***试卷处理标记,请不要删除
一、初中化学金属的化学性质选择题
1.C
解析:
C
【解析】
试题分析:
金属活动顺序表:
KCaNaMgAlZnFeSnPbHCuHgAgPtAu在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。
金属的位置越靠前,金属的活动性越强。
位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。
实验中,铁与硫酸铜反应生成硫酸亚铁和铜,化学方程式为Fe+CuSO4=FeSO4+Cu,铁的表面有红色固体析出,银与硫酸铜不反应,没有明显现象;溶液的颜色由蓝色变成浅绿色。
考点:
金属活动性顺序的探究
2.A
解析:
A
【解析】
A、铜不能将硫酸亚铁中的铁置换出来,说明铁的活动性比铜的强;银不能将硫酸亚铁中的铁置换出来,说明铁的活动性比银的强。
但没有比较出铜和银的活动性强弱,错误;B、铜不能将硫酸亚铁中的铁置换出来,说明铁的活动性比铜的强;铜能将硝酸银中的银置换出来,说明铜的活动性比银的强,故三种金属的活动性强弱顺序是铁、铜、银,正确;C、铁能将硫酸铜中的铜置换出来,说明铁的活动性比铜的强;银不能将硫酸铜中的铜置换出来,说明铜的活动性比银的强,故三种金属的活动性强弱顺序是铁、铜、银,正确;D、铜与稀盐酸不反应,说明铜位于氢的后面;铁能与稀盐酸反应,说明铁位于氢的前面;铜能将硝酸银中的银置换出来,说明铜的活动性比银的强,故三种金属的活动性强弱顺序是铁、铜、银,正确。
故选A。
点睛:
判断三种金属活动性强弱最简单的方法有两种:
用中间的金属和两边金属的溶液或中间金属的溶液和两边的金属。
如判断铁、铜、银的活动性顺序,方法有:
硫酸亚铁溶液、铜、硝酸银溶液或铁、硫酸铜溶液、银。
3.B
解析:
B
【解析】
【详解】
锌粉与硫酸铜溶液反应生成硫酸锌溶液和铜,Zn+CuSO4==Cu+ZnSO4,一段时间后过滤,得蓝色滤液,说明滤液中含有硫酸铜,即反应后硫酸铜溶液有剩余,则滤渣的成分是铜。
故选B。
【点睛】
金属活动性顺序中,排在前面的金属能将排在后面的金属从其化合物的水溶液中置换出来,硫酸铜溶液是蓝色的。
4.A
解析:
A
【解析】
X、Y、Z三种金属,投入稀盐酸中,只有Z表面有气泡冒出,说明Z>H,H>X,H>Y;把X投入到Y的硝酸盐溶液中,X表面有Y析出,说明X>Y,所以三种金属的活动性顺序是:
Z>X>Y,故选A。
5.D
解析:
D
【解析】
【详解】
A、镁条能在空气中燃烧,铝片、铜丝均不能在空气中燃烧,故A说法不正确;
B、铝合金门窗是用铝的合金材料制成的,故B说法不正确;
C、人类使用铝的年代晚于铜、铁,故C说法不正确;
D、武德合金的熔点低,可作保险丝,故D说法正确。
故选D。
6.C
解析:
C
【解析】
【详解】
A、由图中信息可知,M与稀盐酸反应的速率快,说明M比N活泼,此选项错误;
B、由图中信息可知,M与稀盐酸反应生成氢气的质量大,此选项错误;
C、设M、N的质量都是z,相对原子质量分别为x、y,生成氢气的质量为m、n,
,解得x=
,
,解得y=
,
因为m>n,所以x<y,即N的相对原子质量大于M的相对原子质量,此选项正确;
D、由图中信息可知,M与稀盐酸反应生成氢气的速率快于N和稀盐酸反应生成氢气的速率,此选项错误。
故选C。
【点睛】
金属活动性越强,单位时间内产生的氢气越多。
7.D
解析:
D
【解析】
【详解】
在FeCl2和CuCl2的混合溶液中加入Zn粉,锌会先与氯化铜反应,氯化铜反应完后,再与氯化亚铁反应,所以:
A、若反应完成后Zn无剩余,溶液中若有CuCl2,氯化铜没有完全反应,则一定有FeCl2,故A正确;
B、若反应完成后Zn无剩余,溶液中若无CuCl2,加入的锌可能与氯化亚铁发生了置换反应,也可能没有,则可能有FeCl2,故B正确;
C、若反应完成后Zn有剩余,锌会与氯化铜、氯化亚铁完全反应,则溶液中有ZnCl2,无CuCl2和FeCl2,故C正确;
D、若反应完成后Zn有剩余,则溶液中有ZnCl2,一定没有CuCl2、FeCl2,故D错误。
故选D。
8.D
解析:
D
【解析】
【分析】
根据三种金属活动性强弱关系铝>锌>铜,将一定质量的铝粉和锌粉加入到硝酸铜溶液中,铝会先与硝酸铜反应生成硝酸铝和铜,铝粉完全反应后锌再与硝酸铜反应生成硝酸锌和铜。
【详解】
A、若滤液为蓝色,说明了铝和锌已完全发生了反应,则滤渣中一定没有锌和铜,故选项错误;
B、若滤渣中加盐酸没有气泡产生,说明了铝和锌没有剩余,滤液的硫酸铜不一定完全反应,滤液可能为蓝色,故选项错误;
C、若滤液中有硝酸锌,则滤渣中一定没有铝,可能含有锌,故选项错误;
D、若滤渣中加盐酸有气泡产生,则滤渣中一定有锌和铜,可能含有铝,故选项正确。
故选D。
9.A
解析:
A
【解析】
【分析】
根据金属活动性顺序进行分析,在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来。
【详解】
将X加入稀盐酸中,产生氢气,说明活动性X>H;将Y加入稀盐酸中,无明显现象,说明活动性H>Y;将Y加入硝酸银溶液中,有银析出,说明活动性Y>Ag;将Z、Y加入硝酸银溶液中,无明显现象,说明活动性Ag>Z,故金属活动性为:
X>Y>Z;故选A。
【点睛】
氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来。
10.B
解析:
B
【解析】
【分析】
金属活动性顺序表中,在氢元素前面的金属能将氢元素从稀硫酸或盐酸中置换出来;除钾、钙、钠外,在金属活动性顺序中排在前面的金属可以将排在它后面的金属从盐溶液中置换出来。
【详解】
由于三种金属只有金属b可以和稀盐酸反应产生气泡,说明金属b的化学性质最活泼;把a和c分别放入硫酸铜溶液中,在a表面有铜析出,c没有变化,说明a的金属活动性比c强,故三种金属的活动性强弱关系是b>a>c,故选B.
11.A
解析:
A
【解析】
【分析】
在金属活动性顺序中,铜、锌、铁的活动性顺序为锌>铁>铜,向FeSO4和CuSO4的混合溶液中加入一定质量的锌粉,锌先与硫酸铜的反应生成硫酸锌和铜,多余的锌与硫酸亚铁的反应生成硫酸锌和铁,充分反应后过滤,得滤液和滤渣,向滤渣中加入稀盐酸,有气泡产生,所以滤渣中一定含有铁、铜,可能含有锌。
【详解】
A、向FeSO4和CuSO4的混合溶液中加入一定质量的锌粉,锌先与硫酸铜的反应生成硫酸锌和铜,多余的锌与硫酸亚铁的反应生成硫酸锌和铁,充分反应后过滤,得滤液和滤渣,向滤渣中加入稀盐酸,有气泡产生,说明硫酸铜反应完全,滤液中一定不含硫酸铜,所以滤液颜色一定不会显蓝色,故A不正确;
B、锌先与硫酸铜的反应生成硫酸锌和铜,多余的锌与硫酸亚铁的反应生成硫酸锌和铁,加入的锌可能置换出一部分铁,则滤液中可能存在Fe2+,故B正确;
C、锌先与硫酸铜的反应生成硫酸锌和铜,多余的锌与硫酸亚铁的反应生成硫酸锌和铁,滤液中一定含有Zn2+,故C正确;
D、锌先与硫酸铜的反应生成硫酸锌和铜,多余的锌与硫酸亚铁的反应生成硫酸锌和铁,向滤渣中加入稀盐酸,有气泡产生,说明有铁生成,滤渣中一定含有Fe和Cu,可能含有Zn,故D正确。
故选A。
【点睛】
在金属活动性顺序中,排在氢前面的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来。
12.C
解析:
C
【解析】
试题分析:
过量的铁粉放入含AgNO3和Zn(NO3)2的混合溶液里,搅拌,因为铁的活动性大于银小于锌属于能置换出银,滤纸上留下的金属是Fe、Ag。
故选C.
考点:
金属的活动性
13.D
解析:
D
【解析】
【分析】
【详解】
有X、Y、Z三种金属,只有Y在自然界主要以单质形式存在,说明Y的活动性最弱,如果把X放入Z的硫酸盐溶液中,X表面有Z析出,说明X的活动性大于Z。
故选D.
14.C
解析:
C
【解析】
【详解】
A、CH4+2O2
CO2+2H2O,该反应的反应物中氧气是单质,不是两种化合物相互交换成分生成两种新的化合物的反应,不属于复分解反应,故不符合题意;
B、3Fe+2CO2
Fe3O4,该反应符合“多变一”的特征,属于化合反应,故不符合题意;
C、NaOH+HCl═NaCl+H2O,该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,故符合题意;
D、H2CO3═CO2↑+H2O,该反应符合“一变多”的特征,属于分解反应,故不符合题意;
故选C
【点睛】
掌握复分解反应的特征(换成分,价不变)是正确解析本题的关键。
15.D
解析:
D
【解析】
【分析】
【详解】
A.铝丝与硫酸铜溶液反应需要将其表面的氧化物及污物清除,因此铝丝需要砂纸打磨,正确;
B.铝置换出硫酸铜溶液里面的铜,溶液由蓝色变为无色,正确;
C.由溶液由蓝色变为无色可知,铝置换出硫酸铜溶液里面的铜,故金属活动性强弱:
Al>Cu,正确;
D.反应的化学方程式为:
2Al+3CuSO4=3Cu+Al2(SO4)3,故错误。
故选D。
16.D
解析:
D
【解析】
【分析】
【详解】
锰丝放入稀硫酸中,有气泡产生;
说明锰的金属活动性强于氢;
锰丝放入硫酸铝溶液中,表面没有金属析出,说明铝的金属活动性强于锰;
结合铜的金属活动性弱于氢;镁的金属活动性强于氢铝;
所以应选D。
17.D
解析:
D
【解析】根据题意:
把金属X放入AgNO3溶液中,X表面有银白色固体析出,说明X活泼性大于银;若放入FeSO4溶液中,无明显现象,说明了说明Fe活泼性大于X。
则三种金属的活泼性由强到弱的顺序是Fe、X、Ag。
故选D。
点睛:
金属活动性顺序表是按金属活动性由强到弱的顺序进行排列,处于H元素前的金属可与酸发生置换反应;活动性强的金属能把活动性弱的金属从其盐溶液中置换出来。
18.D
解析:
D
【解析】
【详解】
把一根洁净的铁钉放入稀硫酸中的反应原理:
Fe+H2SO4=FeSO4+H2↑,①在铁钉表面产生气泡;②溶液由无色(稀硫酸)逐渐变为浅绿色(FeSO4)溶液③铁钉被消耗,铁钉质量减轻;④根据Fe+H2SO4=FeSO4+H2↑可知,每56份质量的铁能生成2份质量的氢气,溶液的质量增加;描述正确的是:
①②③④;
故选:
D。
19.D
解析:
D
【解析】
【详解】
①两种金属剩余,表明酸完全反应,等量的酸会生成等量的氢气,天平仍然平衡;
②两种金属耗尽,根据化学方程式计算可知,等量的铝和镁完全反应,生成氢气的质量关系为:
铝>镁,天平不平衡;
③镁耗尽铝有剩余分两种情况:
当镁和硫酸恰好完全反应时,二者生成的氢气一样多,天平保持平衡;当镁过量硫酸有剩余时,铝产生的氢气多,天平不平衡。
根据题意可知天平失去平衡,所以可能的情况是②③。
故选D。
20.C
解析:
C
【解析】
试题分析:
依据金属活动性顺序表,锌在氢前,铜在氢后,铜在银前;A.锌与硫酸铜溶液析出红色金属,银与硫酸铜溶液无明显现象,选项说法正确;B.铜与硫酸锌溶液无明显现象,使硝酸银溶液变蓝色,析出银白色的金属,选项说法正确;C.没有涉及铜及其化合物,故无法测定铜与锌和银的金属活动性顺序,选项说法错误;D.锌与稀硫酸有气泡产生,铜与稀硫酸没有明显现象,铜使硝酸银溶液变蓝色,析出银白色的金属,,选项说法正确;故选C
考点:
金属活动性顺序表的应用
21.C
解析:
C
【解析】
在金属活动性顺序表中,锌、铁、铜的活动性依次减弱,故向一定质量FeCl2和CuCl2的混合溶液中加入锌粉,锌粉先与氯化铜反应,后与氯化亚铁反应,锌与氯化铜反应溶液的质量增加1份质量,锌与氯化亚铁反应溶液的质量增加9份质量,故可知,bd段为锌与氯化亚铁反应;
A、a点时,溶液中的部分氯化铜参加了反应,生成了氯化锌,故溶液中的溶质有氯化铜和氯化锌和氯化亚铁,错误;
B、c点时,锌将氯化铜完全反应,又于部分氯化亚铁反应,故固体中有铁生成,加入稀盐酸时,一定有气泡冒出,错误;
C、d点时,锌将氯化铜和氯化亚铁完全反应,故溶液中的溶质有氯化锌,正确;
D、e点时锌有剩余,故固体中有铜、铁和锌,错误。
故选C。
22.C
解析:
C
【解析】
【详解】
观察图像可知,三种金属反应的速率X>Y>Z,判断出三种金属的活动性顺序为X>Y>Z,从而得知X为镁,Y为锌,Z为铁。
相同质量的三种金属完全参加反应,应该是镁消耗的酸最多,铁次之,锌最少,但图中铁产生氢气最多,即消耗稀盐酸最多;镁锌产生氢气一样多,即消耗稀盐酸一样多,故镁过量,但锌无法确定。
故选C。
23.C
解析:
C
【解析】
【详解】
锌的金属活动性比铜、银强,比铝弱,不能与硝酸铝溶液反应;向Cu(NO3)2、AgNO3、Al(NO3)3的混合溶液中加入一定量的Zn,锌首先与AgNO3溶液反应生成硝酸锌溶液和银,AgNO3反应完,若还有锌粉,锌才能与Cu(NO3)2溶液反应生成硝酸锌溶液和铜;
①滤渣的组成有三种可能,可能只含有银,也可能含有银和铜,也可能是银、铜和过量的锌,故①正确;
②硝酸铝没有参加反应,反应后生成硝酸锌,滤液中一定含有Zn(NO3)2和Al(NO3)3,故②正确;
③向滤渣中加入稀盐酸不一定有气泡产生,滤渣中可能不含锌,故③错误;
④锌与硝酸银、硝酸铜反应的化学方程式分别是Zn+2AgNO3═Zn(NO3)2+2Ag、Zn+Cu(NO3)2═Zn(NO3)2+Cu,根据化学方程式可知,每65份质量的锌反应生成216份质量的银,参加反应的锌的质量小于生成银的质量,反应后溶液质量减小;每65份质量的锌反应生成64份质量的铜,参加反应的锌的质量大于生成铜的质量,反应后溶液质量增大;所以反应前后溶液的质量可能相等,故④正确。
正确的是①②④有3个。
故选C。
【点睛】
用同种金属置换不同的盐溶液,盐中金属排在金属活动性顺序中较后的金属首先被置换出来。
本题要考虑锌的质量对反应后的溶质成分、过滤后的滤渣成分的影响。
24.C
解析:
C
【解析】
由金属活动顺序表的应用分析四个实验,发现验证实验的设计思路为:
根据三种金属与盐酸反应情况,可验证铁的活动性比铜、银强;然后利用金属铜和硝酸银的置换结果,验证铜的活动性比银强.对比四个实验,实验B证明金属铜不能置换出酸中的氢,而实验D又可以证明银的活动性小于铜,所以