专题31 电化学综合应用.docx
《专题31 电化学综合应用.docx》由会员分享,可在线阅读,更多相关《专题31 电化学综合应用.docx(13页珍藏版)》请在冰豆网上搜索。
专题31电化学综合应用
专题31电化学综合应用
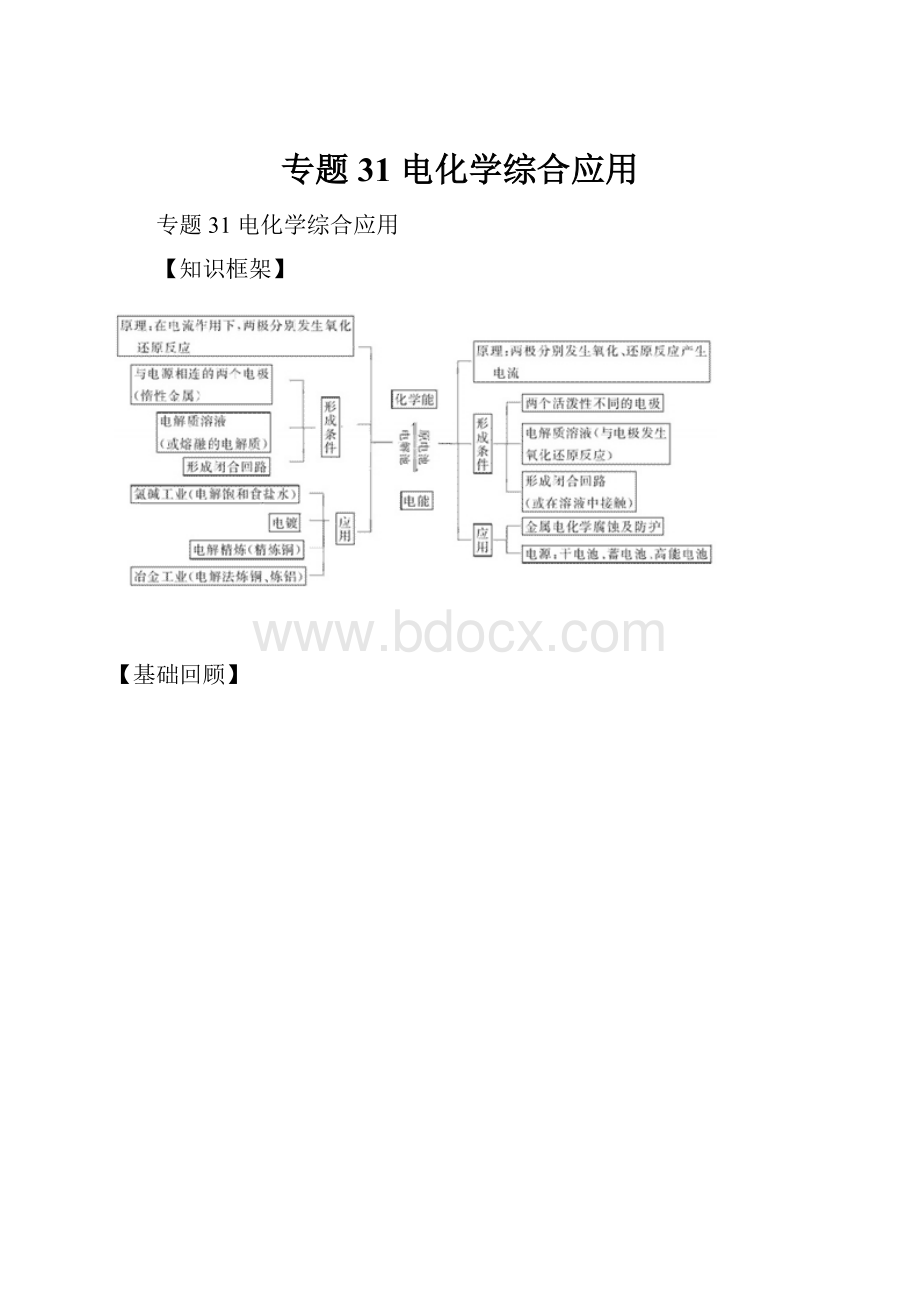
【知识框架】
【基础回顾】
一、三池(原电池、电解池、电镀池)比较
二、金属腐蚀及防护
1、金属腐蚀的种类
2、金属的防护
(1)电化学防护
①牺牲阳极的阴极保护法—原电池原理
a.负极:
比被保护金属活泼的金属;
b.正极:
被保护的金属设备。
②外加电流的阴极保护法—电解原理
a.阴极:
被保护的金属设备;
b.阳极:
惰性金属。
(2)改变金属的内部结构,如制成合金、不锈钢等。
(3)加防护层,如在金属表面喷油漆、涂油脂、电镀、喷镀或表面钝化等方法。
【技能方法】
电化学定量计算方法与技巧
1、计算类型
原电池和电解池的计算包括两极产物的定量计算、溶液pH的计算、相对原子质量和阿伏加德罗常数的计算、产物的量与电量关系的计算等。
2、方法技巧
(1)根据电子守恒计算
用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的电子数相等。
(2)根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列出比例式计算
(3)根据关系式计算
根据得失电子守恒定律关系建立起已知量与未知量之间的桥梁,构建计算所需的关系式。
如以通过4mole-为桥梁可构建如下关系式:
(式中M为金属,n为其离子的化合价数值)
该关系式具有总揽电化学计算的作用和价值,熟记电极反应式,灵活运用关系式便能快速解答常见的电化学计算问题。
【提示】在电化学计算中,还常利用Q=I•t和Q=n(e-)×NA×1.60×10-19C来计算电路中通过的电量。
【基础达标】
1.【江西省崇义中学2015届高三上学期月考(4)】下列关于原电池和电解池的叙述正确的是( )
A.原电池中失去电子的电极为阴极
B.原电池的两极一定是由活动性不同的两种金属组成
C.原电池的负极、电解池的阳极都发生氧化反应
D.电解时电解池的阳极一定是阴离子放电
【答案】C
【解析】
试题分析:
A.原电池中失去电子的电极为负极,错误;B.原电池的两极是由活动性不同的电极组成,可能是两种金属组成,也可能是金属与非金属构成,错误;C.原电池的负极、电解池的阳极都是失去电子发生氧化反应,正确;D.电解时电解池的阳极若是惰性电极,则是阴离子放电;若是活性电极,则是电极本身失去电子,发生氧化反应,错误。
考点:
考查关于原电池和电解池的名称、构成材料、电极反应及反应的物质的判断的知识。
2.铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法错误的是( )
A.正极电极反应式为:
2H++2e-===H2↑
B.此过程中还涉及到反应:
4Fe(OH)2+2H2O+O2===4Fe(OH)3
C.此过程中Cu并不被腐蚀
D.此过程中电子从Fe移向Cu
【答案】A
【解析】
铁、铜接触处在潮湿空气中发生吸氧腐蚀,其中Fe作负极,电极反应式为Fe-2e-===Fe2+,Cu作正极,电极反应式为O2+4e-+2H2O===4OH-,原电池反应为2Fe+O2+2H2O===2Fe(OH)2,但Fe(OH)2易与空气中的O2发生反应4Fe(OH)2+O2+2H2O===4Fe(OH)3.
3.【山西大学附属中学2015届高三12月月考化学试题】关于右图装置说法正确的是( )
A.装置中电子移动的途径是:
负极FeM溶液石墨正极
B.若M为NaCl溶液,通电一段时间后,溶液中可能有NaClO
C.若M为FeCl2溶液,可以实现石墨上镀铁
D.若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀
【答案】B
【解析】
试题分析:
A.装置中电子移动的途径是:
负极到Fe电极;然后是溶液中的阴离子在阳极石墨放电到电源的正极,错误;B.若M为NaCl溶液,通电一段时间后,阳极产生H2,溶液中的NaOH与阳极产生的Cl2发生反应产生NaCl和NaClO,所以溶液中可能有NaClO,正确;C.若M为FeCl2溶液,在阳极溶液中的Fe2+失去电子变为Fe3+,所以不可能实现石墨上镀铁,错误;D.若M是海水,该装置是电解池,是外接电源的阴极保护方法使铁不被腐蚀,不是“牺牲阳极的阴极保护法”,错误。
考点:
考查电解原理的应用的知识。
4.【甘肃省高台县第一中学2014年秋学期期末考试】下列与金属腐蚀有关的说法正确的是( )
A.图1中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图2中,一段时间后会出现白色沉淀-灰绿色沉淀-红褐色沉淀的现象
C.图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀
D.图4中,用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的正极
【答案】B
【解析】
试题分析:
A、插入海水中的铁棒,发生吸氧腐蚀,越靠近液面腐蚀越严重,A错误;B、图2中形成铜铁原电池,一段时间后会出现白色沉淀-灰绿色沉淀-红褐色沉淀的现象,B正确;C、图3中,燃气灶的中心部位不易生锈,主要是由于高温下燃气还原金属氧化物,C错误;D、图4中,镁比铁活泼,镁块发生氧化反应,镁块相当于原电池的负极,D错误;答案选B。
考点:
金属的腐蚀与防护
5.【广东省肇庆市2015届高三第一期末化学试题】相同材质的铁在下图中的四种情况下腐蚀最快的是( )
【答案】A
【解析】
试题分析:
A、铁、铜和食醋形成原电池,铁作负极,加快其腐蚀;B、铝、铁和食盐水形成原电池,铝作负极,铁作正极,减缓铁腐蚀;C、铁上面镀铜减缓铁的腐蚀;D、锌、铁和酸雨形成原电池,铁作正极,减缓铁腐蚀,铁腐蚀最快的是A。
考点:
考查原电池原理的应用,金属的腐蚀与防护。
【能力提升】
1.下图各烧杯中盛有海水,铁在其中被腐蚀,腐蚀的速率由快到慢的顺序为( )
A.⑤②①③④ B.④③①②⑤
C.⑤④②①③ D.③②④①⑤
【答案】C
【解析】
判断金属腐蚀的快慢,首先判断该金属是否充当原电池或电解池的电极,若是电解池的阳极,金属腐蚀速率最快,其次是充当原电池的负极腐蚀较快,而作为电解池的阴极和原电池的正极则不被腐蚀.⑤中,Fe作为电解池的阳极,腐蚀最快,②③④均为原电池,③中,Fe为正极,不被腐蚀,②④中Fe均为负极被腐蚀,Fe和Cu的金属活动性差别比Fe和Sn大,故④中铁腐蚀较快,则铁被腐蚀的速率由快到慢的顺序为⑤④②①③
2.【江西省吉安市白鹭洲中学2015届高三上学期期中考试】下面有关电化学的图示,完全正确的是( )
【答案】D
【解析】
试题分析:
A.在Cu—Zn原电池中,由于金属活动性Zn>Cu,所以Zn是负极,Cu是正极,在正极上发生还原反应,错误;B.粗铜精炼时,粗铜作阳极,精铜作阴极,所以电极连接有误,错误;C.在Fe片上镀锌时,Fe作阴极,Zn作阳极,电极连接不正确,错误;D.电解饱和NaCl溶液时,在阳极发生反应:
2Cl-—2e-=Cl2↑,Cl2有强氧化性,与KI发生反应:
Cl2+2KI===2KCl+I2。
I2与淀粉溶液变为蓝色;在阴极,发生反应,2H++e-=H2↑,由于氢气的密度比空气小,所以用向下排空气的方法收集,正确。
考点:
考查有关电化学的图示的正误判断的知识。
3.现将氯化铝溶液蒸干灼烧并熔融后用铂电极进行电解,下列有关电极产物的判断正确的是( )
A.阴极产物是氢气 B.阳极产物是氧气
C.阴极产物是铝和氧气 D.阳极产物只有氯气
【答案】B
【解析】
将氯化铝溶液蒸干灼烧得到Al2O3,电解熔融的Al2O3,阳极为O2-放电,阳极产物为氧气;阴极为Al3+放电,阴极产物为Al.
4.【福建省三明一中2015届高三上学期第二次月考】电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。
在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。
已知:
3I2+6OH—==IO3—+5I—+3H2O下列说法不正确的是( )
A.右侧发生的电极方程式:
2H2O+2e-==H2↑+2OH-
B.电解结束时,右侧溶液中含有IO3-
C.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变
D.电解槽内发生反应的总化学方程KI+3H2O==KIO3+3H2↑
【答案】C
【解析】
试题分析:
A、在一定的电压下通电,发现左侧溶液变蓝色,这说明左侧碘离子放电失去电子转化为单质碘,因此左侧是阳极。
一段时间后,蓝色逐渐变浅,这说明右侧中的氢氧根向左侧移动,与生成的碘反应生成碘酸根和碘离子,蓝色消失,所以右侧是氢离子放电,电极反应式为右侧发生的电极方程式:
2H2O+2e-==H2↑+2OH-,A正确;B、生成的碘酸根可以通过阳离子交换膜移向右侧,所以电解结束时,右侧溶液中含有IO3-,B正确;C、如果用阳离子交换膜代替阴离子交换膜,则右侧产生的氢氧根不能移向左侧,碘不能与氢氧根反应,所以电解槽内发生的总化学方程式发生改变,C错误;根据以上分析可知电解槽内发生反应的总化学方程
D正确,答案选C。
考点:
考查电解原理的应用
5.用石墨做电极电解1mol/LCuSO4溶液,当c(Cu2+)为0.5mol/L时,停止电解,向剩余溶液中加入下列何种物质可使电解质溶液恢复至原来的状态( )
A.CuSO4 B.CuO C.Cu(OH)2 D.CuSO4•5H2O
【答案】B
【解析】电解过程中的反应为:
阳极:
4OH--4e-===2H2O+O2↑,阴极:
2Cu2++4e-=2Cu。
总反应为:
2CuSO4+2H2O=2H2SO4+2Cu+O2↑。
由以上反应可知,电解使2molCuSO4和2molH2O变成了2molH2SO4,同时析出铜,放出O2,溶液中每生成2molCu则放出1molO2,故需补充CuO或CuCO3。
【终极闯关】
1.【北京市朝阳区2014~2015学年度高三年级第一学期期末统一考试】碘盐中添加的碘酸钾在工业上可用电解KI溶液制取,电极材料是石墨和不锈钢,化学方程式是:
有关说法不正确的是( )
A.石墨作阳极,不锈钢作阴极
B.I-在阳极放电,H+在阴极放电
C.电解过程中电解质溶液的pH变小
D.电解转移3mole-时,理论上可制得KIO3107g
【答案】C
【解析】
试题分析:
A、根据方程式可知碘离子失去电子,水电离出的氢离子得到电子转化为氢气。
电解池中阳极失去电子,阴极得到电子,所以该电解池中阳极是惰性电极,则石墨作阳极,不锈钢作阴极,A正确;B、根据A中分析可知I-在阳极放电,H+在阴极放电,B正确;C、电解时氢离子放电,从而产生氢氧根,因此溶液的碱性增强,则pH变大,C错误;D、根据方程式可知生成1mol碘酸钾转移6mol电子,则电解转移3mole-时,理论上可制得KIO3的质量是
D正确,答案选C。
考点:
考查电解原理的应用
2.两个惰性电极插入500mLAgNO3溶液中,通电电解。
当电解液的pH从6.0变为3.0时,(设电解过程中阴极没有H2放出,且电解液在电解前后体积变化可以忽略不计)电极上析出银的质量最大为( )
A.27mg B.54mg C.106mg D.216mg
【答案】B
【解析】
首先结合离子放电顺序,弄清楚两极的反应:
阳极4OH--4e-===O2↑+2H2O;阴极Ag++e-===Ag,电解的总反应式为
由电解的总反应式可知,电解过程中生成的n(H+)=n(HNO3)=n(Ag)=(10-3mol•L-1-10-6mol•L-1)×0.5L≈5×10-4mol,m(Ag)=5×10-4mol×108g•mol-1=0.054g=54mg。
3.【浙江省建人高复2015届高三上学期第三次月考】下列有关电化学的内容正确的是( )
A.马口铁和白铁皮破损后,白铁皮比马口铁腐蚀快,所以使用白铁皮时要注意防止铁皮出现刮痕
B.原电池中电子从负极流出流入正极,电解池中电子从阴极流出流入电源负极
C.已知磷酸亚铁锂电池总反应为
电池中的固体电解质可传导Li+,则该电池充电时阳极电极反应式为:
LiFePO4+e-=FePO4+Li+
D.常温下以C选项中电池为电源以石墨为电极电解200mL饱和食盐水,当消耗1.4gLi时,溶液的pH为14(忽略溶液的体积变化)
【答案】D
【解析】
试题分析:
A.马口铁和白铁皮破损后,由于白铁皮表面有活动性比Fe强的Zn,马口铁表面有活动性比Fe弱的Sn,所以都会构成原电池,前者首先被腐蚀的是Zn,后者Fe先被腐蚀,因此Fe被腐蚀的速率后者大于前者。
使用白铁皮时铁皮出现刮痕也同压会对铁起到保护作用,错误;B.原电池中电子从负极流出流入正极,电解池中电子从阳极流出流入电源正极,错误;C.已知磷酸亚铁锂电池总反应为
电池中的固体电解质可传导Li+,则该电池充电时阴极电极反应式为:
LiFePO4+e-=FePO4+Li+,错误;D.常温下以C选项中电池为电源以石墨为电极电解200mL饱和食盐水,由于在整个闭合回路中电子转移的数目相等。
当消耗1.4gLi时,n(e-)=1.4g÷7g/mol=0.2mol,则在NaCl溶液中发生反应
产生NaOH的物质的量是0.2mol,由于溶液的体积是0.2L,所以c(NaOH)=1mol/L,根据在室温下水的离子积常数是1×10-14,可得溶液的pH为14,正确。
考点:
考查金属的腐蚀与保护、原电池、电解池的反应原理及应用的知识。
4.【浙江省台州中学2015届高三上学期第三次统练试题】工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示。
下列说法错误的是( )
已知:
①Ni2+在弱酸性溶液中发生水解
②氧化性:
Ni2+(高浓度)>H+>Ni2+(低浓度)
A.碳棒上发生的电极反应:
4OH--4e-=O2↑+2H2O
B.电解过程中,B中NaCl溶液的物质的量浓度将不断减少
C.为了提高Ni的产率,电解过程中需要控制废水pH
D.若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
【答案】B
【解析】
试题分析:
A、碳棒为阳极发生氧化反应,在碱性条件下发生的电极反应:
4OH--4e-=O2↑+2H2O,A正确;B、电解过程中,B中NaCl溶液的物质的量浓度将不断增大,B错误;C、因氧化性:
Ni2+(高浓度)>H+>Ni2+(低浓度)为了提高Ni的产率,电解过程中需要控制废水pH,C正确;D、现在两个电解室分别显酸性和碱性,若将图中阳离子膜去掉,将A、B两室合并,溶液的酸碱性发生变化,则电解反应总方程式发生改变,D正确;答案选B。
考点:
电解原理、电解池
5.500mLKNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是( )
A.原混合溶液中n(K+)为2mol
B.上述电解过程中共转移4mol电子
C.电解得到的Cu的物质的量为0.5mol
D.电解后溶液中c(OH-)为2mol/L
【答案】B
【解析】
试题分析:
根据题意知,用石墨作电极电解硝酸钾和硝酸铜混合溶液时,阴极上的电极反应依次为Cu2++2e-====Cu,2H++2e-====H2↑;阳极上电极反应为:
4OH--4e-====O2↑+2H2O;当通电一段时间后,两极均收集到22.4L气体(标准状况),气体的物质的量为1mol;阳极上生成1mol氧气失去4mol电子,阴极上每生成1mol氢气得到2mol电子,每生成1mol铜得到2mol电子,根据转移电子守恒得铜的物质的量1mol,则铜离子的物质的量浓度2mol/L,根据电荷守恒得钾离子浓度2mol/L。
A、根据上述分析知,混合溶液中c(K+)为2mol•L-1,钾离子的物质的量为1ml,错误;B、上述电解过程中共转移4mol电子,正确;C、根据上述分析知,铜的物质的量为1mol,错误;D、当电解硝酸铜时溶液中生成氢离子,当电解硝酸钾溶液时,实际上是电解水,故电解生成氢离子的物质的量为2mol,氢离子浓度4mol/L,c(OH—)为2.5×10-15mol/L,错误。
考点:
考查电解原理的应用及电解计算。