特殊电极反应式.docx
《特殊电极反应式.docx》由会员分享,可在线阅读,更多相关《特殊电极反应式.docx(14页珍藏版)》请在冰豆网上搜索。
特殊电极反应式
特殊电极反应式
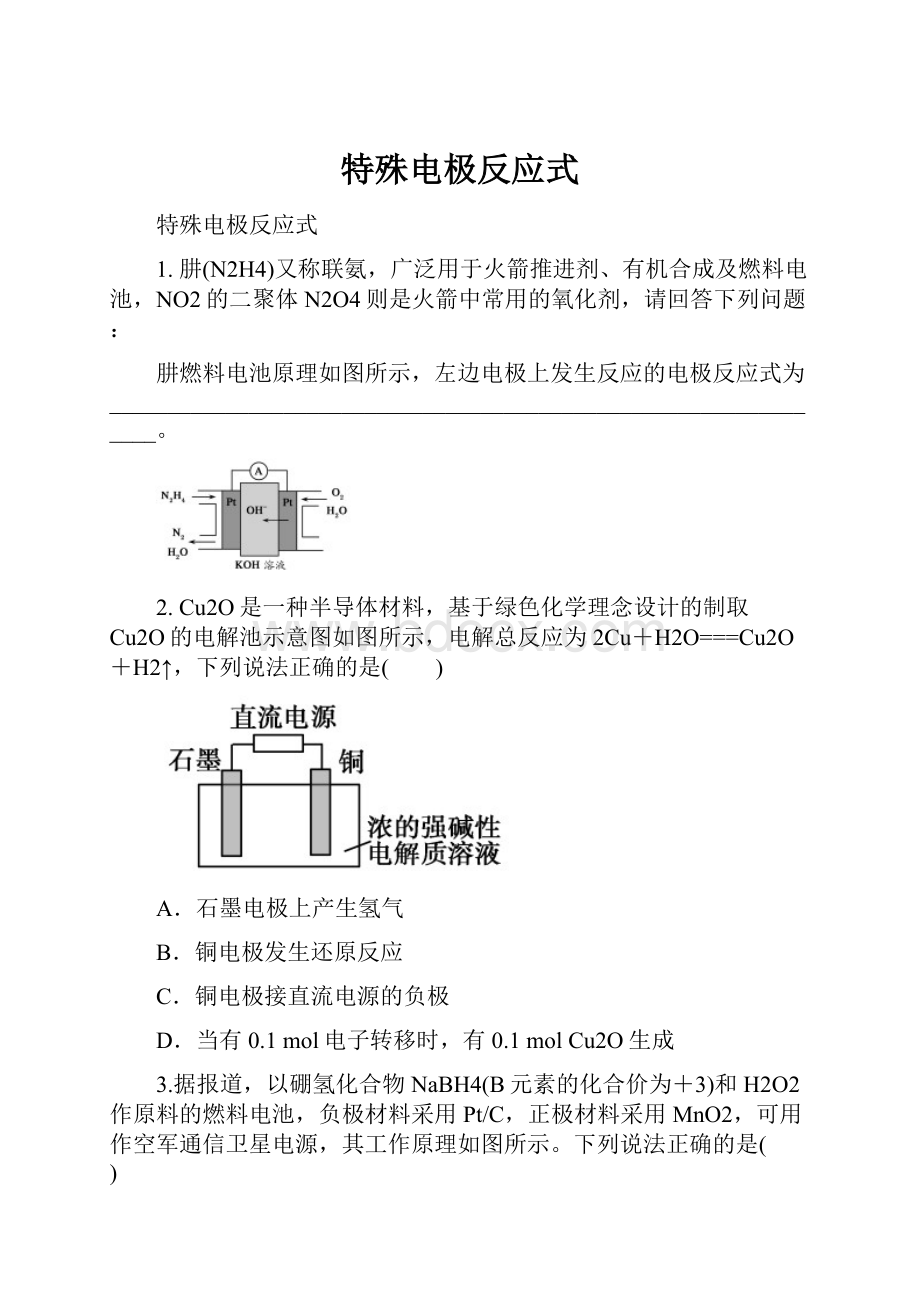
1.肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用的氧化剂,请回答下列问题:
肼燃料电池原理如图所示,左边电极上发生反应的电极反应式为________________________________________________________________。
2.Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图所示,电解总反应为2Cu+H2O===Cu2O+H2↑,下列说法正确的是( )
A.石墨电极上产生氢气
B.铜电极发生还原反应
C.铜电极接直流电源的负极
D.当有0.1mol电子转移时,有0.1molCu2O生成
3.据报道,以硼氢化合物NaBH4(B元素的化合价为+3)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。
下列说法正确的是( )
A.电池放电时Na+从a极区移向b极区
B.每消耗3molH2O2,转移的电子为3mol
C.电极a采用MnO2,MnO2既作电极材料又有催化作用
D.该电池的负极反应为BH
+2H2O-8e-===BO
+8H+
4.电化学在日常生活中用途广泛,图①是镁—次氯酸钠燃料电池,电池总反应为:
Mg+ClO-+H2O===Cl-+Mg(OH)2,图②是Cr2O
工业废水的处理。
下列说法正确的是( )
A.图②中Cr2O
向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3被除去
B.图②的电解池中,有0.084g阳极材料参与反应,阴极会有336mL的气体产生
C.图①中发生的还原反应是:
Mg2++ClO-+H2O+2e-===Cl-+Mg(OH)2↓
D.若图①中3.6g镁溶解产生的电量用以图②废水处理,则理论可产生10.7g氢氧化铁沉淀
5.锂空气电池是一种新型的二次电池,其放电时的工作原理如图所示,下列说法正确的是( )
A.该电池放电时,正极的反应式为O2+4e-+4H+===2H2O
B.该电池充电时,阴极发生了氧化反应:
Li++e-===Li
C.电池中的有机电解液可以用稀盐酸代替
D.正极区产生的LiOH可回收利用
6.钛被称为“21世纪金属”,是研制卫星、火箭、宇宙飞船及深海潜艇的重要材料。
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置模拟获得金属钙(需定期更换石墨棒),并以钙为还原剂,还原二氧化钛制备金属钛。
下列叙述正确的是( )
A.甲装置工作过程中OH-向Ag2O/Ag极移动,乙装置工作过程中O2-向阴极移动
B.若电解金属Ti效率为η,则制备1molTi时消耗Al的物质的量为
(1-η)mol
C.乙装置阳极的电极反应式为C+2O2--4e-===CO2↑
D.在制备金属钛前后,整套装置中CaO的总量减少
7.镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越来越成为人们研制绿色原电池的关注焦点.其中一种镁原电池的反应为xMg+Mo3S4
MgxMo3S4;在镁原电池放电时,下列说法错误的是---( )
A.Mg2+向正极迁移 B.正极反应为:
Mo3S4+2xe-===Mo3S
C.Mo3S4发生氧化反应 D.负极反应为:
xMg-2xe-===xMg2+
8.某兴趣小组同学利用氧化还原反应:
2KMnO4+10FeSO4
+8H2SO4===2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,
其中甲、乙两烧杯中各物质的物质的量浓度均为1mol·L-1,
盐桥中装有饱和K2SO4溶液.回答下列问题:
(1)发生氧化反应的烧杯是________(填“甲”或“乙”).
(2)外电路的电流方向为:
从________到________.(填“a”或“b”)
(3)电池工作时,盐桥中的SO移向________(填“甲”或“乙”)烧杯.
(4)甲烧杯中发生的电极反应为______________________________________________.
9.
电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图如图(电解池中隔膜仅阻止气体通过,a、b极均为惰性电极)。
下列说法正确的是
江西省南昌市2013届高三第三次模拟考试理综试题及答案
电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图如图(电解池中隔膜仅阻止气体通过,a、b极均为惰性电极)。
下列说法正确的是
A.电解时,b极是阴极放出H2,发生氧化反应
B.溶液中OH—逐渐向b极移动
C.龟解时,a极的电极反应式为:
D.若在b极产生标况下224mL氢气,则消耗尿素2g
10.MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。
阴极的电极反应式是 。
若电解电路中通过2mol电子,MnO2的理论产量。
阳极的电极反应式是。
11.以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应为。
12.2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到570℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如下图)。
请回答:
钯电极A是电解池的极(填“阳”或“阴”),该极上的电极反应式是
13.Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的水处理剂,其电解制法如图所示,请根据图示分析:
(1)Fe电极的电极反应方程式为:
。
(2)Ni电极接的是电源的极,电解后,该电极附近溶液的pH。
(3)当Ni电极上放出标准状况下3.36L气体时,铁极质量减小g。
14..铅蓄电池的工作原理为:
Pb+PbO2+2H2SO4=2PbSO4+2H2O研读右图,下列判断不正确的是
A.K闭合时,d电极反应式:
PbSO4+2H2O-2e-=PbO2+4H++SO42-
B.当电路中转移0.2mol电子时,I中消耗的H2SO4为0.2mol
C.K闭合时,II中SO42-向c电极迁移
D.K闭合一段时间后,II可单独作为原电池,d电极为正极
E.当电路中转移0.2mol电子时,a极质量(填“增大”或减小)g
15.甲乙两烧杯Na2SO4溶液,甲烧杯中用铜做电极电解,乙烧杯中用石墨做电极电解。
当两烧杯中的阴极上产生等量的气体时,停止通电,欲使用电解液恢复到起始状态,应向甲乙两溶液中加入的物质的质量比为:
。
16.某可充电的锂离子电池以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质。
放电时的电池反应为:
Li+LiMn2O4==Li2Mn2O4。
下列说法正确的是:
A.放电时,LiMn2O4发生氧化反应B.放电时,正极反应为:
Li++LiMn2O4+e-==Li2Mn2O4
C.充电时,LiMn2O4发生氧化反应D.充电时,阳极反应为:
Li++e-==Li
17.天津是我国研发和生产锂离子电池的重要基地。
锂离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。
电池反应为LiCoO2+C6
CoO2+LiC6,下列说法正确的是:
()
(A)充电时,电池的负极反应为LiC6-e-=Li++C6
(B)放电时,电池的正极反应为CoO2+Li++e-=LiCoO2
(C)羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质
(D)锂离子电池的比能量(单位质量释放的能量)低
18.三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:
用NaOH调NiCl2溶液pH至7.5,加放适量硫酸钠后进行电解。
电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍。
以下说法正确的是()
(A)可用铁作阳极材料
(B)电解过程中阳极附近溶液的pH升高
(C)阳极反应方程式为:
2Cl--2e-=Cl2
(D)1mol二价镍全部转化为三价镍时,外电路中通过了1mol电子。
19.某同学设计了一种利用电解法制取Fe(OH)2装置(如下图)。
通电后,溶液中产生大量白色沉淀,且较长时间不变色。
下列说法中正确的是( )
A.电源中的a一定为正极,b一定为负极
B.不能使用NaCl溶液作电解液
C.A、B两端都必须使用铁作电极
D.B电极发生的反应可能为:
2H2O+2e-=H2↑+2OH-
20.研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:
5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是:
A.正极反应式:
Ag+Cl--e-=AgClB.每生成1molNa2Mn5O10转移2mol电子
C.Na+不断向“水”电池的负极移动D.AgCl是还原产物
21.研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。
该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。
关于该电池的下列说法不正确的是
A.水既是氧化剂又是溶剂B.放电时正极上有氢气生成
C.放电时OH-向正极移动D.总反应为:
2Li+2H2O===2LiOH+H2↑
22.Ag2O2是银锌碱性电池的正极活性物质,可通过下列方法制备:
在KOH加入适量AgNO3溶液,生成Ag2O沉淀,保持反应温度为80℃,边搅拌边将一定量K2S2O8溶液缓慢加到上述混合物中,反应完全后,过滤、洗涤、真空干燥得到固体样品。
反应方程式为2AgNO3+4KOH+K2S2O8
Ag2O2↓+2KNO3+K2SO4+2H2O
回答下列问题:
(1)上述制备过程中,检验洗涤是否完全的方法是
。
(2)银锌碱性电池的电解质溶液为KOH溶液,电池放电时正极的Ag2O2转化为Ag,负极的Zn转化为
K2Zn(OH)4,写出该电池反应方程式:
。
(3)准确称取上述制备的样品(设Ag2O2仅含和Ag2O)2.558g,在一定的条件下完全分解为Ag和O2,得到224.0mLO2(标准状况下)。
计算样品中Ag2O2的质量分数(计算结果精确到小数点后两位)。
23.
用铅蓄电池电解AgNO3、Na2SO3的溶液,a、b、c、d电极材料均为石墨。
已知铅蓄电池的总反应为:
Pb(s)+PbO2(s)+2H2SO4(aq)
2PbSO4(s)+2H2O
(1),通电时a电极质量增加,下列说法正确的是
[ ]
A.电路中通过1mol电子时,Y电极质量增加48g
B.放电时铅蓄电池负极的电极反应式为:
PbO2(s)+4H+ (aq)+SO42- (aq)+4e-==PbSO4 (s)+2H2O
(1)
C.c、d电极产生气体的物质的量之比为1:
2
D.X极为负极
24.用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生。
某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/L的FeCl2溶液,研究废液再生机理。
记录如下(a、b、c代表电压数值):
序号
电压/V
阳极现象
检验阳极产物
I
x≥a
电极附近出现黄色,
有气泡产生
有Fe3+、有Cl2
II
a>x≥b
电极附近出现黄色,
无气泡产生
有Fe3+、无Cl2
III
b>x>0
无明显变化
无Fe3+、无Cl2
(1)用KSCN检验出Fe3+的现象是_______________________。
(2)I中,Fe3+产生的原因可能是Cl—在阳极放电,生成的Cl2将Fe2+氧化。
写出有关反应:
____________________________________________________。
(3)由II推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有_________性。
(4)II中虽未检验出Cl2,但Cl—在阳极是否放电仍需进一步验证。
电解pH=1的NaCl溶液做对照实验,记录如下:
序号
电压/V
阳极现象
检验阳极产物
IV
a>x≥c
无明显变化
有Cl2
V
c>x≥b
无明显变化
无Cl2
①NaCl的浓度是_________mol/L
②IV中检测Cl2的实验方法______________________________________________。
③与II对比,得出的结论(写出两点):
_____________________________________________。
【答案】(15分)
(1)溶液变红
(2)2Cl— -2e— =Cl2↑ Cl2+2Fe2+=2Cl—+2Fe3+
(3)还原
(4)①0.2
②取少量阳极附近的溶液,滴在淀粉KI试纸上,试纸变蓝
③通过控制电压,证实了产生Fe3+的两种原因都成立;通过控制电压,验证了Fe2+先于Cl-放电
25.人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如下图。
①电源的负极为 (填“A”或“B”).
②阳极室中发生的反应依次为 、 。
电解亚硫酸钠溶液
一.电解Na2SO3溶液
【分析】溶液中存在的离子有H+、OH-、Na+、SO32-.简单分析就是要比较H+和Na+得到电子的能力以及OH-和SO32-失去电子的能力,显然产物应该分别为氢气和硫酸根离子。
方程式为:
Na2SO3+H2O=Na2SO4+H2
【讨论】假如得到氧气,则氧气也能和亚硫酸根离子作用得到硫酸根离子,况且这里的氧是新生氧,具有“很强的生命力”。
附:
酸性条件下氧气的还原电位是+1.229V;硫酸根和亚硫酸之间的还原电位是+0.17V。
算了一下,要得到氧气出现需要pH=0(氢离子浓度为1mol/L)时亚硫酸浓度低于十的负36次方才有可能。
【延伸】假如这里具有强还原性的离子不是阴离子,又会怎样?
因为在电场的作用下,阳离子是往阴极移动的,使得阳极附近的阳离子浓度降低,影响阳离子的还原性,而在阴极的发生的还原反应,譬如,氯化亚铁溶液就存在这个问题。
二.电解FeCl2溶液
【分析】这里的问题就是刚才提出的问题,亚铁离子在电解时,会“慢慢”移动到阴极,但毕竟比较少,但不管怎样,在阳极即便得到氯气,生成的氯气也会和亚铁离子作用得到铁离子,理论分析,电解氯化铁一定会使得溶液先变黄色,阴极产生气体,甚至可以得到氢氧化铁沉淀,阳极产生的气体是否能被完成反应掉?
是否有氧气产生?
这些有待实验证明。
笔者以为,该实验和浓度以及酸碱度有关。
实验结果(电解10分钟):
在阴极产生的气体明显比阳极要多,至少要2倍以上,用湿润的KI淀粉试纸没有检出Cl2,也没有感觉到的刺激性气味。
随着电解时间的增加,阳极的溶液颜色不断加深,从浅绿色变化为黄色,黄色溶液不断向阴极扩散。
阴极附近没有产生白色或者灰绿色的沉淀(可能电解时间较短)。
三.电解FeCl3溶液
实验现象:
阳极与阴极都产生了气泡,但是阳极产生气体的体积约是阴极产生气体的3倍。
阳极产生的气体有强烈的刺激性气味。
电解质溶液颜色变化不明显。
分析结论:
阳极Cl-放电生成Cl2。
阴极则是Fe3+与H+同时放电,H+反应程度更大一些。
很明显,以上两种情况出现了矛盾。
原因就是两者的浓度有显著的不同,这里也说明了粒子的氧化性或者还原性显然和浓度关系比较大。
四.电解K2MnO4溶液
工业上采用铁和石墨为电极,电解K2MnO4溶液制取KMnO4。
(1)电解时,应以__________作阴极,电解过程中,阴极附近溶液的pH将会____________(填增大、减小或不变)。
(2)阳极反应式为_____________________________________。
(3)电解的总化学方程式为_____________________________。
(1)铁增大
(2)MnO42---e-=MnO4-
(3)2K2MnO4+2H2O=2KMnO4+2KOH+H2↑
注:
氢氧根失电子,形成羟基自由基,亚铁离子或者铁离子能与羟基自由基发生feton反应(终产物为Fe2+),使之分解为水和氧气.
(6)工业上用Na2SO3吸收尾气中的SO2,再用右图装置电解(惰性电极)NaHSO3制取H2SO4,阳极电极反应式,阳极区逸出气体的成分为__________(填化学式)。
在这种情况下,由于亚硫酸氢钠并不是在阳极区,因此难以失去电子,则在阳极得到氧气,并同时得到二氧化硫!