福建省化学竞赛预赛试题答案及评分标准_精品文档.doc
《福建省化学竞赛预赛试题答案及评分标准_精品文档.doc》由会员分享,可在线阅读,更多相关《福建省化学竞赛预赛试题答案及评分标准_精品文档.doc(7页珍藏版)》请在冰豆网上搜索。
2012年福建省高中学生化学竞赛预赛试题答案及评分标准(第7页,共7页)
2012年福建省高中学生化学竞赛预赛试题
答案及评分标准
第1题(10分)
1-1 6分
I2+SO32-+H2O=2I-+SO42-+2H+
2I-+2Cu2++SO32-+H2O=2CuI↓+SO42-+2H+
2CuI+8HNO3(浓)=2Cu(NO3)2+4NO2↑+I2+4H2O
每个方程式各2分。
方程式未配平扣1分,写成分子方程式不给分。
1-24分
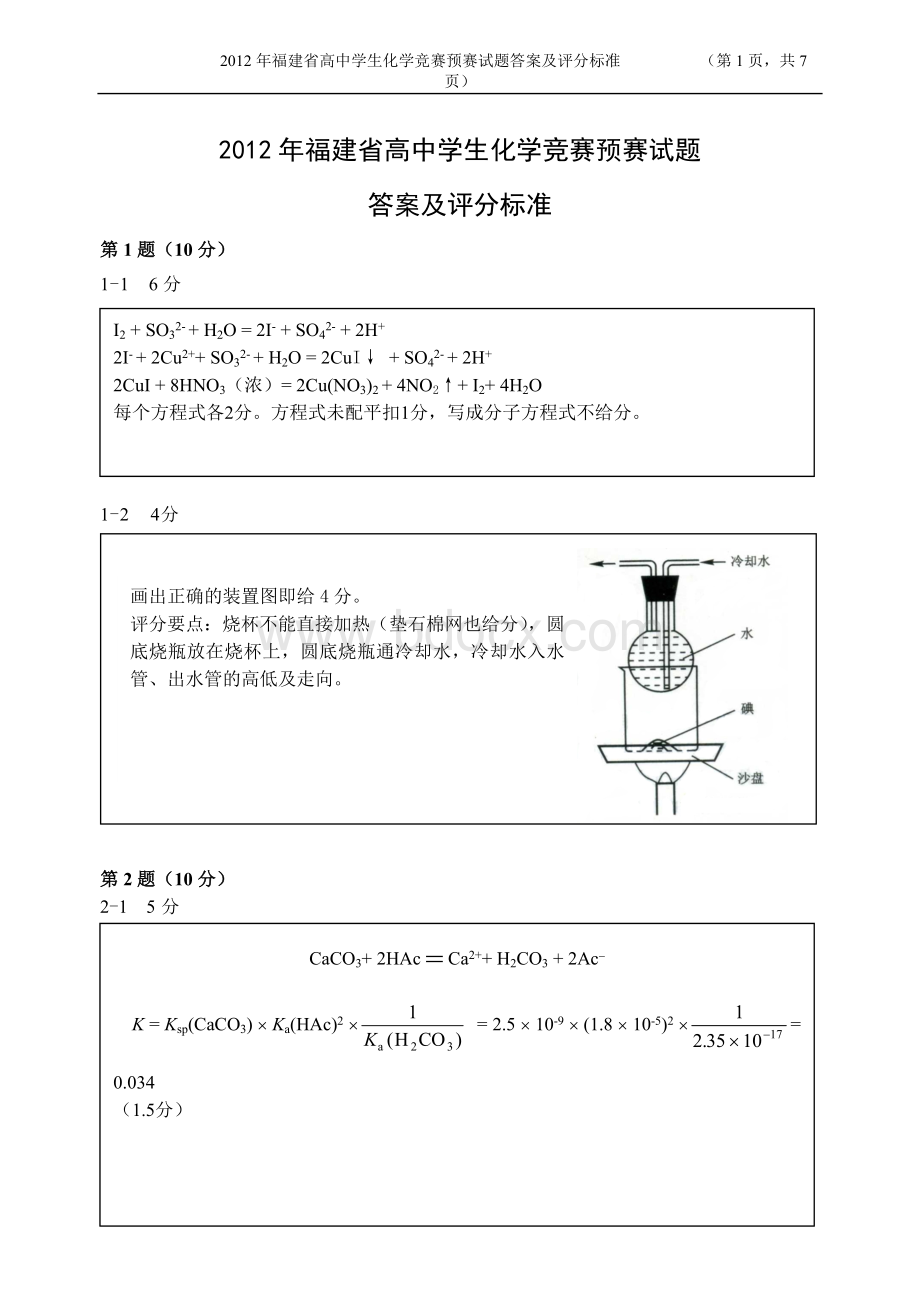
画出正确的装置图即给4分。
评分要点:
烧杯不能直接加热(垫石棉网也给分),圆底烧瓶放在烧杯上,圆底烧瓶通冷却水,冷却水入水管、出水管的高低及走向。
第2题(10分)
2-15分
CaCO3+2HAc=Ca2++H2CO3+2Ac-
K=Ksp(CaCO3)´Ka(HAc)2´=2.5´10-9´(1.8´10-5)2´=0.034
(1.5分)
CaC2O4+2HAc=Ca2++H2C2O4+2Ac-
K=Ksp(CaC2O4)´Ka(HAc)2´=2.5´10-9´(1.8´10-5)2´
=2.1´10-13(1.5分)
由反应平衡常数可以判断,CaC2O4不溶HAc。
CaCO3溶于HAc的平衡常数虽然也较小,但是由于H2CO3不稳定,易分解为CO2离开反应体系,所以CaCO3溶于HAc。
因此,沉淀A为CaC2O4和CaCO3,沉淀B为CaC2O4.
(2分)
2-2 3分
不行(不正确)(1分)
理由:
因为菠菜中草酸与铁同时存在,由于草酸的还原性,铁应为Fe2+,需要用硝酸或者其他氧化剂将其氧化为Fe3+ (1分)
同时菠菜汤汁呈绿色,会干扰鉴别,应加入活性碳脱色 (1分),
使溶液接近无色,然后用KSCN鉴别,显血红色说明存在铁离子。
2-32分
不能,胃中含有盐酸,CaC2O4和CaCO3均能溶于盐酸。
第3题(11分)
3-14分,每个图2分。
(不要求标出键角、键长,但基本形状要相同)
3-24分
P4+5O2=P4O10(1分)
P4O10+6CaO=2Ca3(PO4)2↓(1分)
P4+6CaO+2FeO+4O2=2Ca3(PO4)2↓+2Fe(2分)
3-33分
PCl3键角大。
(1分)
两个分子中心原子杂化方式相同,构型相同(三角锥形)(1分)
Cl的电负性比F小,PCl3分子中P上电子云密度相对较大,排斥力较大,所以键角较大。
(1分)
第4题(9分)
4-13分
MgCO3分解温度低(1分)
原因:
两者的碳酸盐均分解为氧化物,分解温度高低主要取决于金属离子的极化作用(0.5分),Mg2+的电荷高(0.5分),而Li+、Mg2+半径十分接近(0.5分),因此Mg2+极化作用强(0.5分)。
4-2 3分
BF3中B—F键能较高(1分)
原因:
BF3中B为sp2杂化,平面三角形分子,B与F间除有s键处,还存在键。
(1分)
NF3中N为sp3杂化,为三角锥形分子,不存在有大p键,N—F为单键。
(1分)
4-3 3分
4NaOH+3Fe==4Na+2H2+Fe3O4(2分)
原因:
因为生成固体的Fe3O4及气态Na和H2,离开反应体系,从平衡角度看,反应可以向右进行。
(1分)
第5题(10分)
5-17分
(a),(b),(c)每个2分,共6分。
5-23分
CaCO3比CaO更稳定。
(1分)
(1分)
,因CO2的平衡分压远小于大气中CO2的分压,故碳酸钙稳定。
(1分)
第6题(10分)
6-14分,每个原子核外电子排布2分。
P:
1s2,2s2,2p6,3s2,3p3;
Ti:
1s2,2s2,2p6,3s2,3p6,4s2,3d2
6-26分,每个分子2分。
(a)SO2:
S原子采用sp2杂化,与两个氧原子各形成一个σ键外,三个原子还形成一个Π34键。
(b)NO3-:
N原子采用sp2杂化,与三个氧原子各形成一个σ键外,四个原子还形成一个Π46大π键。
(c)CO2:
C原子采用sp杂化,与两个氧原子各形成一个σ键外,三个原子还形成两个Π34大π键。
第7题(10分)
评分总则:
在计算式中,未带入单位不扣分。
但计算结果表示应考虑有效数字和单位。
本题所有求算结果均为四位有效数字,第一次有效数字错误扣0.5分;求算物理量均需正确标注单位,第一次单位错误扣0.5分,但有效数字和单位错误累计扣分不超过1分。
7-1 4分
邻苯二甲酸氢钾的摩尔数:
或3.000×10-3mol (2分)
NaOH的摩尔数:
n=3.000mmol或3.000×10-3mol
NaOH溶液的浓度:
(2分,未将体积单位从mL换成L扣1分)
7-22分
NaOH滴定H2SO4的化学反应方程式:
H2SO4+2NaOH===Na2SO4+2H2O(2分,未配分扣1分)
采用酚酞指示剂,到达终点时溶液颜色为微红色。
(1分)
7-33分
稀释后H2SO4溶液的摩尔浓度:
(2分,少掉计量系数“2”扣1分)
未知H2SO4样品液的摩尔浓度:
(1分)
第8题(15分)
8-15分,每个化合物1分,结构式和命名各0.5分。
A
丙烯
B
环丙烷
C
(R)-1,2-二溴丙烷
C,D答案可互换
D
(S)-1,2-二溴丙烷
C,D答案可互换
E
1,3-二溴丙烷
8-22分
(1分)
取代反应(1分)
8-32.5分,每个0.5分。
A-d的可能结构:
B-d的可能结构:
8-40.5分
A1
8-55分,每个0.5分。
A2
A2,A3可互换
A3
A2,A3可互换
A4
A4,A5可互换
A5
A4,A5可互换
A6
A7
X1
X1,X2可互换
X2
X1,X2可互换
Y
Z
第9题(6分)
9-12分,每个0.5分
烯键、羟基、羰基、羧基
9-2 2分,B,E,H每少写一个扣0.5分,多写的每2个扣0.5分,但扣分最高不超过2分。
B,E,H是正确的。
9-32分
第10题(9分)
10-1 6分,每个1分
A
B
C
D
E
F
写成酸不扣分
10-23分,每个0.5分
G
H
I
J
K
DEEP