届高考化学考前冲刺提分训练晶体结构及简单计算答案 详解课后总结.docx
《届高考化学考前冲刺提分训练晶体结构及简单计算答案 详解课后总结.docx》由会员分享,可在线阅读,更多相关《届高考化学考前冲刺提分训练晶体结构及简单计算答案 详解课后总结.docx(12页珍藏版)》请在冰豆网上搜索。
届高考化学考前冲刺提分训练晶体结构及简单计算答案详解课后总结
——晶体结构及简单计算
【提分训练】
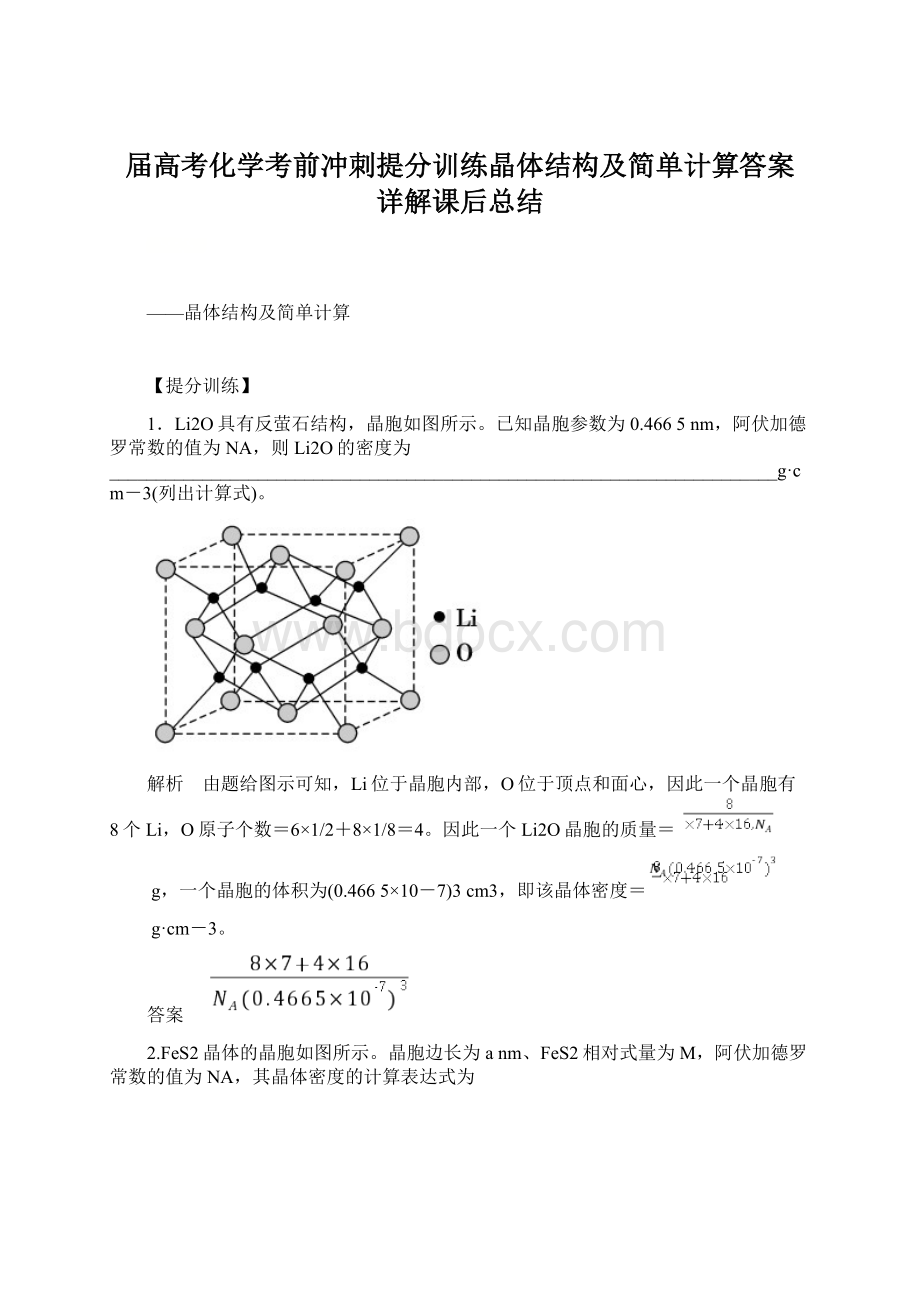
1.Li2O具有反萤石结构,晶胞如图所示。
已知晶胞参数为0.4665nm,阿伏加德罗常数的值为NA,则Li2O的密度为________________________________________________________________________g·cm-3(列出计算式)。
解析 由题给图示可知,Li位于晶胞内部,O位于顶点和面心,因此一个晶胞有8个Li,O原子个数=6×1/2+8×1/8=4。
因此一个Li2O晶胞的质量=
g,一个晶胞的体积为(0.4665×10-7)3cm3,即该晶体密度=
g·cm-3。
答案
2.FeS2晶体的晶胞如图所示。
晶胞边长为anm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为_______________________________________________________________________g·cm-3;晶胞中Fe2+位于S
所形成的正八面体的体心,该正八面体的边长为________nm。
解析 该晶胞中Fe2+位于棱上和体心,个数为12×
+1=4,S
位于顶点和面心,个数为8×
+6×
=4,故晶体密度为
×4g÷(a×10-7cm)3=
×1021g·cm-3,根据晶胞结构,S
所形成的正八面体的边长为该晶胞中相邻面的面心之间的连线之长,即为晶胞边长的
,故该正八面体的边长为
anm。
答案
×1021
a
3.金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为____________。
六棱柱底边边长为acm,高为ccm,阿伏加德罗常数的值为NA,Zn的密度为____________________________________________g·cm-3(列出计算式)。
解析 金属Zn晶体为六方最密堆积方式(A3型)。
六棱柱底边边长为acm,则六棱柱上下面的面积均为6×
a2cm2,则六棱柱的体积为6×
a2ccm3,锌原子在六棱柱的顶点、上下面心和晶胞内,一个晶胞含锌原子个数=12×1/6+2×1/2+3=6,因此一个晶胞中Zn的质量=
g,由此可知,Zn的密度=
g·cm-3。
答案 六方最密堆积(A3型)
4.
(2)K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是_____________________。
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。
K与O间的最短距离为________nm,与K紧邻的O个数为________。
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于________位置,O处于________位置。
解析
(2)K原子半径大,且价电子数少(K原子价电子数为1,Cr原子价电子排布为3d54s1,价电子数为6),金属键弱,熔、沸点低。
(4)根据晶胞结构可知,K与O间的最短距离为面对角线的一半,即
nm≈0.315nm。
K、O构成面心立方,配位数为12(同层4个,上、下层各4个)。
(5)由图可知K、I的最短距离为体对角线的一半,I处于顶角,K处于体心,I、O之间的最短距离为边长的一半,I处于顶角,O处于棱心。
答案
(2)K的原子半径较大且价电子数较小,金属键较弱
(4)0.315(或
×0.446) 12 (5)体心 棱心
5.(3)单质铜及镍都是由________键形成的晶体。
(4)某镍白铜合金的立方晶胞结构如图所示。
①晶胞中铜原子与镍原子的数量比为________。
②若合金的密度为dg·cm-3,晶胞参数a=__________________________nm。
解析 (3)铜和镍属于金属,则单质铜及镍都是由金属键形成的晶体。
(4)①根据均摊法计算,晶胞中铜原子个数为6×
=3,镍原子的个数为8×
=1,则铜和镍的数量比为3∶1;②根据上述分析,该晶胞的组成为Cu3Ni,合金的密度为dg·cm-3,根据ρ=
,则晶胞参数a=
×107nm。
答案 (3)金属
(4)①3∶1 ②
×107
6.某砷镍合金的晶胞结构如图所示,阿伏加德罗常数的值为NA,则该晶体的密度ρ=____________g·cm-3,该晶体中与每个Ni原子距离最近的As原子有________个。
解析 晶胞内有2个As原子,Ni原子个数为2×
+4×
+2×
+4×
=2,因而晶胞内原子总质量m=
=
g,晶胞体积V=
a2c×1030cm3,晶胞密度等于
=
g·cm-3,晶胞是由两个完全相同的平行六面体上下堆叠而成,例如下底最左边的Ni原子为6个这样的平行六面体所占有,每个这样的平行六面体含有1个As原子,因而该晶体中与每个Ni原子距离最近的As原子有6个。
答案
6
7.(2019·全国卷Ⅱ)近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe�Sm�As�F�O组成的化合物。
回答下列问题:
(1)元素As与N同族。
预测As的氢化物分子的立体结构为________,其沸点比NH3的________(填“高”或“低”),其判断理由是___________________。
(2)Fe成为阳离子时首先失去____________轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为________。
(3)比较离子半径:
F-________O2-(填“大于”“等于”或“小于”)。
(4)一种四方结构的超导化合物的晶胞如图1所示。
晶胞中Sm和As原子的投影位置如图2所示。
图中F-和O2-共同占据晶胞的上下底面位置,若两者的比例依次用x和1-x代表,则该化合物的化学式表示为________;通过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:
ρ=________g·cm-3。
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为
,则原子2和3的坐标分别为________、________。
解析
(1)AsH3的中心原子As的价层电子对数为(5+3)/2=4,包括3对成键电子和1对孤对电子,故其立体结构为三角锥形。
NH3中N的电负性比AsH3中As的大得多,故NH3易形成分子间氢键,从而使其沸点升高。
(2)Fe的价层电子排布式为3d64s2,其阳离子Fe2+、Fe3+的价层电子排布式分别是3d6、3d5,二者均首先失去4s轨道上的电子;Sm失去3个电子成为Sm3+时首先失去6s轨道上的电子,然后失去1个4f轨道上的电子,故Sm3+的价层电子排布式为4f5。
(3)F-与O2-电子层结构相同,核电荷数越大,原子核对核外电子的吸引力越大,离子半径越小,故离子半径F-<O2-。
(4)由晶胞结构中各原子所在位置可知,该晶胞中Sm个数为4×
=2,Fe个数为1+4×
=2,As个数为4×
=2,O或F个数为8×
+2×
=2,即该晶胞中O和F的个数之和为2,F-的比例为x,O2-的比例为1-x,故该化合物的化学式为SmFeAsO1-xFx。
1个晶胞的质量为
g=
g,1个晶胞的体积为a2cpm3=a2c×10-30cm3,故密度ρ=
g·cm-3。
原子2位于底面面心,其坐标为
;原子3位于棱上,其坐标为
。
答案
(1)三角锥形 低 NH3分子间存在氢键
(2)4s 4f5 (3)小于 (4)SmFeAsO1-xFx
8.含氟化合物在生产生活中有重要的应用,回答下列问题:
(1)基态氟原子核外电子的运动状态有________种,有________种不同能量的原子轨道,其价层轨道表示式为____________________。
(2)N与F可形成化合物N2F2,下列有关N2F2的说法正确的是________(填字母)。
a.分子中氮原子的杂化轨道类型为sp2
b.其结构式为F-N≡N—F
c.其分子有两种不同的空间构型
d.1molN2F2含有的σ键的数目为4NA
(3)NaHF2可用于制无水氟化氢和供雕刻玻璃、木材防腐等用。
常温常压下为白色固体,易溶于水,160℃分解。
NaHF2中所含作用力的类型有________(填字母)。
a.离子键b.共价键
c.配位键d.氢键
(4)二氟甲烷(CH2F2)难溶于水,而三氟甲烷(CHF3)可溶于水,其可能的原因是______________________________________________________________。
(5)氟化钙的晶胞结构如图所示。
晶胞中Ca2+离子的配位数为____________________。
与F-等距且最近的Ca2+形成的空间构型为____________________。
已知氟化钙的晶胞边长为apm,其密度为ρg·cm-3,则阿伏加德罗常数的数值为____________________(列出计算式即可)。
解析
(1)氟原子核外电子数为9,核外没有运动状态相同的电子,基态氟原子核外电子的运动状态有9种,核外电子排布为:
1s22s22p5,有3种不同能量的原子轨道,价层轨道表示式为
。
(2)其结构式为F—N==N—F,故b错误;1molN2F2含有的σ键的数目为3NA,故d错误;故选a、c。
(4)三氟甲烷中的H原子可与H2O中的O原子之间形成氢键,因此可溶于水。
(5)从氟化钙的晶胞结构可以看出Ca2+居于晶胞的顶点和面心,在每个Ca2+周围距离相等且最近的F-有8个,Ca2+离子的配位数为8,F-居于晶胞的八个小正方体的体心,在每个F-周围距离相等最近的Ca2+有4个,形成的空间构型为正四面体,在一个晶胞中含有Ca2+的数目为4,含有F-的数目为8,列式计算ρg·cm-3×(a×10-10)3cm=4×78/NAg,所以NA=
。
答案
(1)9 3
(2)ac
(3)abd
(4)三氟甲烷中由于3个F原子的吸引使得C原子的正电性增强,从而三氟甲烷中的H原子可与H2O中的O原子之间形成氢键
(5)8 正四面体
【课后总结】
1.晶胞中微粒数目的计算方法——均摊法
熟记几种常见的晶胞结构及晶胞含有的粒子数目。
A.NaCl(含4个Na+,4个Cl-)
B.干冰(含4个CO2)
C.CaF2(含4个Ca2+,8个F-)
D.金刚石(含8个C)
E.体心立方(含2个原子)
F.面心立方(含4个原子)
2.有关晶胞计算的思维模板
(1)晶体密度的计算
(2)晶体微粒与M、ρ之间的关系
若1个晶胞中含有x个微粒,则1mol晶胞中含有xmol微粒,其质量为xMg(M为微粒的相对原子质量);又1个晶胞的质量为ρa3g(a3为晶胞的体积,a为晶胞边长或微粒间距离),则1mol晶胞的质量为ρa3NAg,因此有xM=ρa3NA。