工艺流程中化学方程式的书写.docx
《工艺流程中化学方程式的书写.docx》由会员分享,可在线阅读,更多相关《工艺流程中化学方程式的书写.docx(13页珍藏版)》请在冰豆网上搜索。
工艺流程中化学方程式的书写
工业流程——反应方程式的书写
在高中新课程改革实施后,高考越来越注重与生产、生活实际相结合。
高考化学卷将根据物质的化学性质编写的无机框图推断题改为与生产、生活实际相结合的化学工业流程题。
以前考的无机框图推断题多为人为设计,问题的设置较单一,逻辑推理气氛浓厚,与真实的化学情境相差较远。
化学工业流程题结合生活生产实际,关注资源的综合利用和循环经济,根据物质实际的制备、分离和提纯,设计问题考查元素化合物知识、实验基本操作、化学反应原理、绿色化学观点、安全生产等知识。
命制题目:
确立考查点→遴选素材库→打磨问题链→推敲分布点
(预测题目困难,但考查点可预测)
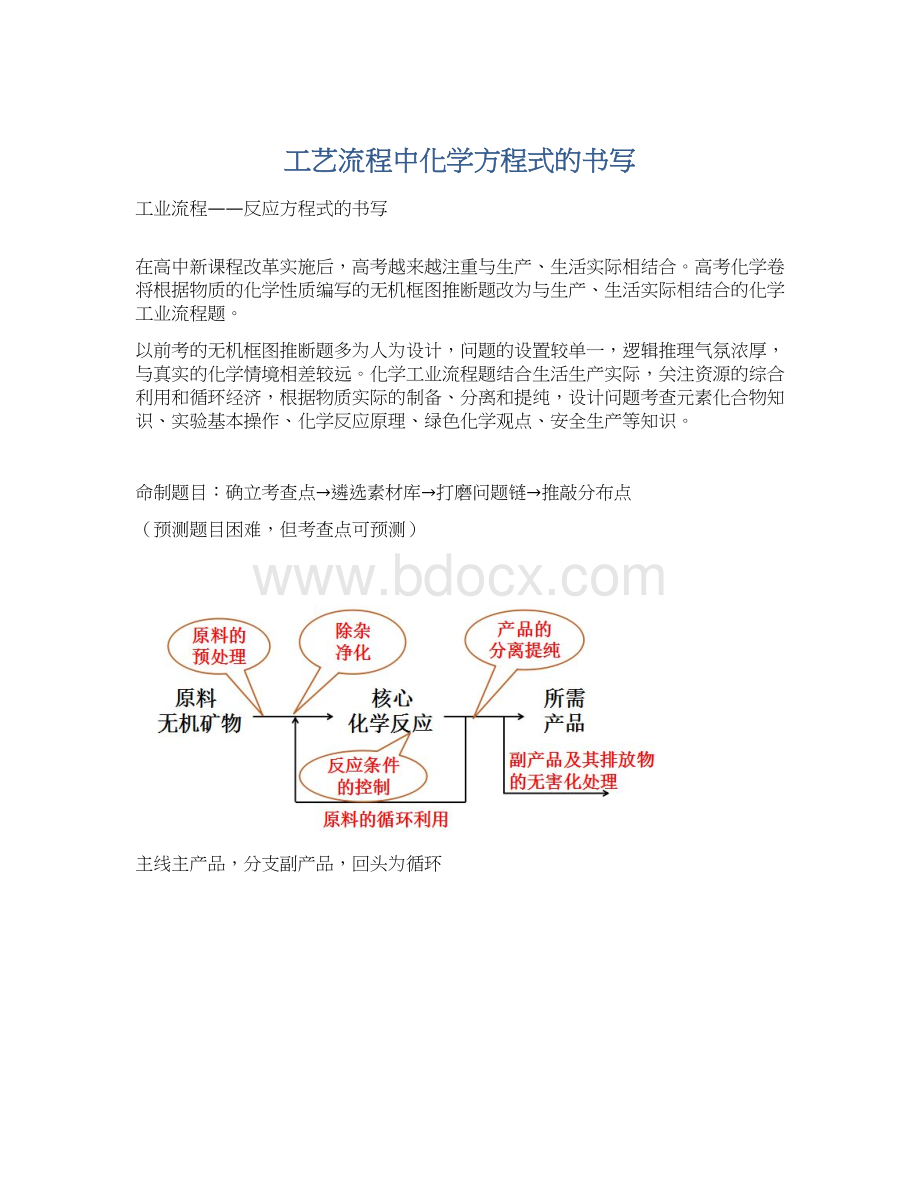
主线主产品,分支副产品,回头为循环
考查点:
①化学基本概念、化学基本理论、元素化合物、化学实验、化学计算等知识的理解和应用
②对图形图表的观察和进行初步加工、吸收、有序存储的能力
③对试题中提供的新信息、准确提取并与已有的知识块整合重组及表达能力
核心化学反应——陌生方程式的书写
化学工业流程题中考查的化学方程式的书写,教材上一般没有出现过这样的化学方程式,对于学生来说是陌生的,但是不会超出学生的能力范围。
只要学生能根据所学的元素化合物知识,利用化学反应中物质转化的原理,就能顺利由反应物推导出生成物,并结合配平的原则与技巧,最后能正确写出陌生的化学方程式。
对于书写教材中没有出现过的化学反应方程式,可以沿着以下的思路进行解决:
氧化还原反应
非氧化还原反应
首先判断反应类型
一、氧还反应——化合价
运用氧还规律
①判断产物形式
氧化剂还原产物,还原剂氧化产物
产物能否在给定溶液的酸碱性存在
②配平
关注箭头指向
箭头指入:
反应物
箭头指出:
生成物
关注写离子方程式还是化学方程式
常见的氧化剂、还原剂及其对应还原产物、氧化产物:
氧化剂
常见还原产物
还原剂
常见氧化产物
O2
OH-,H2O,O2-
活泼金属
金属离子
X2(Cl2,Br2,I2)
X-(Cl-,Br-,I-)
Fe2+
Fe3+
Fe3+
(遇弱)Fe2+,(遇强)Fe
Cu+
Cu2+
Cu2+
Cu+,Cu
H2
H2O,H+
Ag+
Ag
C
CO,CO2
酸性KMnO4溶液
Mn2+
CO
CO2
KClO3
Cl2,Cl-
S
SO2
MnO2
Mn2+
SO2/SO32-
SO3/SO42-
HClO
Cl-
S2-
S、SO2
浓H2SO4
SO2,
X-(Cl-,Br-,I-)
X2(Cl2,Br2,I2)
HNO3
(稀)NO,(浓)NO2,
H2C2O4
CO2
Na2O2,H2O2
OH-,H2O
NH3
N2,NO
1、氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
依据上图,完成下列填空:
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为。
电解
(6)2NaCl+2H2O======2NaOH+H2↑+Cl2↑ Cl2+2NaOH=2NaClO+H2↑
(13福建卷,24题)二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂
.
(1)氯化钠电解法是一种可靠的工业生产ClO2方法.该法工艺原理如图.其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2.发生器中生成ClO2的化学方程式为
答案:
2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
(13全国新课标1,27题,15分)锂离子电池的应用很广,其正极材料可再生利用。
某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙炔黑和铝箔等。
充电时,该锂离子电池负极发生的反应为6C+xLi++xe-===LixC6。
现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出)。
回答下列问题:
(2)写出“正极碱浸”中发生反应的离子方程式__________________________。
(3)“酸浸”一般在80℃下进行,写出该步骤中发生的所有氧化还原反应的化学方程式______________________________________;
答案:
(2)2Al+2OH-+6H2O===2[Al(OH)4]-+3H2↑
(3)2LiCoO2+3H2SO4+H2O2
Li2SO4+2CoSO4+O2↑+4H2O
2H2O2
2H2O+O2↑
(16全国卷1,28题14分)NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
回答下列问题:
(2)写出“反应”步骤中生成ClO2的化学方程式_______。
答案:
(2)2NaClO3+SO2+H2SO4=ClO2+2NaHSO4;
(15全国卷1,27题,14分)
硼及其化合物在工业上有许多用途。
以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:
回答下列问题:
(6)单质硼可用于生产具有优良抗冲击性能的硼钢。
以硼酸和金属镁为原料可制备单质硼,用化学方程式表示制备过程______。
答案:
(6)2H3BO3
B2O3+3H2OB2O3+3Mg
2B+3MgO
(根据反应物性质结合质量守恒定律)
2、非氧还反应
结合物质性质和反应实际判断产物
①判断产物
产物能否在给定溶液的酸碱性存在
②配平
关注箭头指向
箭头指入:
反应物
箭头指出:
生成物
关注写离子方程式还是化学方程式
1、海水的综合利用可以制备金属镁,其流程如下图所示:
(1)若在空气中加热MgCl2·6H2O生成的是Mg(OH)Cl或MgO,写出相应反应的化学方程式;用电解法制取金属镁时,需要无水氯化镁。
1、
(1)MgCl2·6H2O
Mg(OH)Cl+HCl↑+5H2O↑
MgCl2·6H2O
MgO+2HCl↑+5H2O↑;
2、氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
依据上图,完成下列填空:
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为:
。
(2)Ca2++CO32-=CaCO3↓, Mg2++2OH-=Mg(OH)2↓
(14江苏化学卷)烟气脱硫能有效减少二氧化硫的排放。
实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[Al2(SO4)x(OH)6—2x]溶液,并用于烟气脱硫研究。
(1)酸浸时反应的化学方程式为;
答案:
Al203+3H2SO4=Al2(S04)3+3H20
(13全国新课标1,27题,15分)锂离子电池的应用很广,其正极材料可再生利用。
某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙炔黑和铝箔等。
充电时,该锂离子电池负极发生的反应为6C+xLi++xe-===LixC6。
现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出)。
回答下列问题:
(4)写出“沉钴”过程中发生反应的化学方程式__________________________。
答案:
(4)CoSO4+2NH4HCO3===CoCO3↓+(NH4)2SO4+H2O+CO2↑
(09江苏16题,改编)以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸铵和氧化铁红颜料,原料的综合利用率较高。
其主要流程如下:
(2)已知反应III为2KCl+(NH4)2SO4=K2SO4↓+NH4CI,写出反应I的化学方程式:
_______________________________________。
答案:
(15全国卷1,27题,14分)
硼及其化合物在工业上有许多用途。
以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:
回答下列问题:
(1)写出Mg2B2O5·H2O与硫酸反应的化学方程式________。
答案:
(1)Mg2B2O5·H2O+2H2SO4
2H3BO3+2MgSO4