有机化学市八补课.docx
《有机化学市八补课.docx》由会员分享,可在线阅读,更多相关《有机化学市八补课.docx(24页珍藏版)》请在冰豆网上搜索。
有机化学市八补课
有机化学
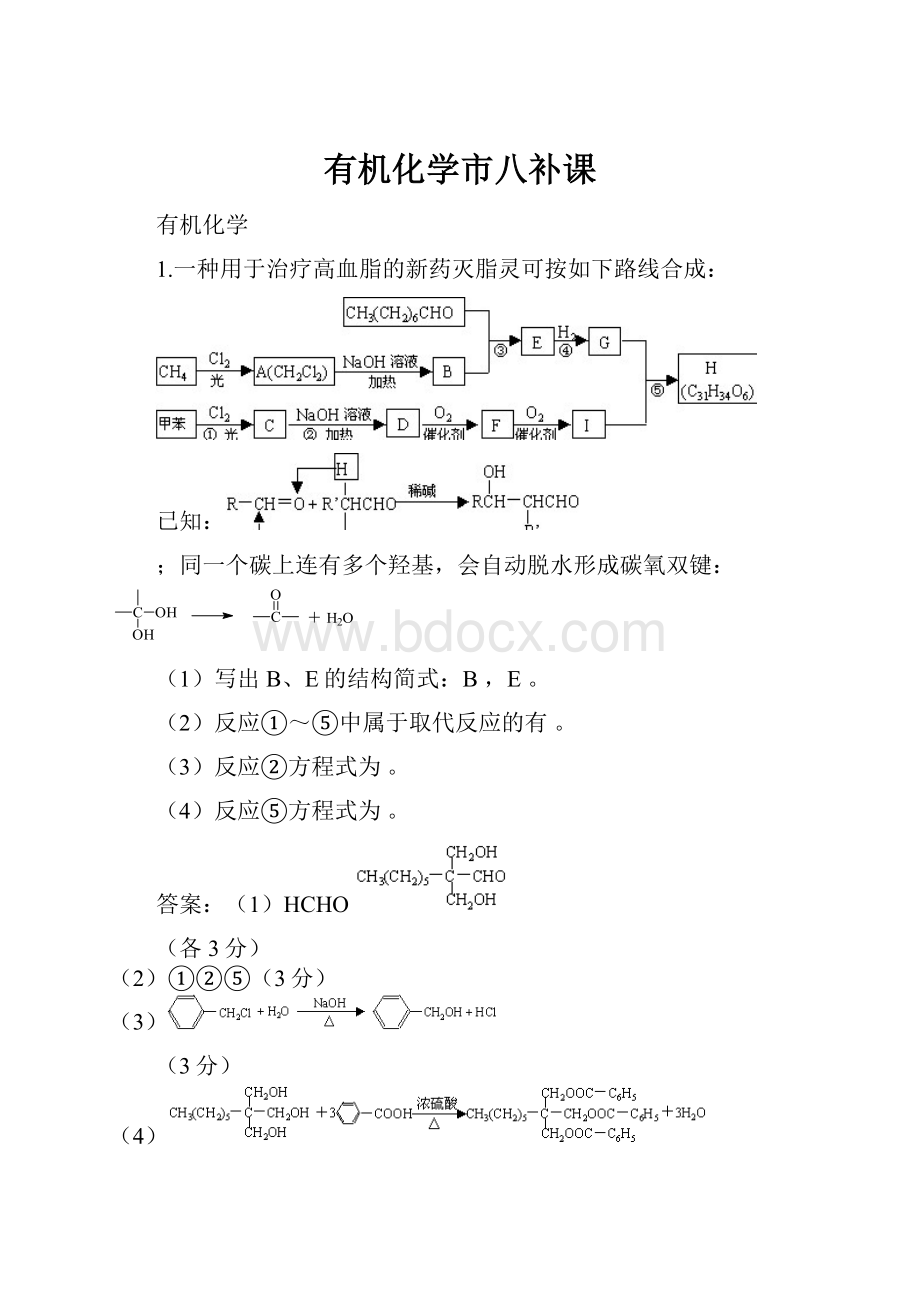
1.一种用于治疗高血脂的新药灭脂灵可按如下路线合成:
已知:
;同一个碳上连有多个羟基,会自动脱水形成碳氧双键:
(1)写出B、E的结构简式:
B,E。
(2)反应①~⑤中属于取代反应的有。
(3)反应②方程式为。
(4)反应⑤方程式为。
答案:
(1)HCHO
(各3分)
(2)①②⑤(3分)
(3)
(3分)
(4)
(3分)
乙偶姻是一个极其重要的香料品种,主要用于配制奶香型、肉香型、草莓香型香精,也可用于合成其他精细化学品。
已知乙偶姻中只含有C、H、O三种元素,其相对分子质量为88,分子中C、H、O原子个数比为2:
4:
1。
请回答:
(1)X是乙偶姻的同分异构体,属于酯类,X结构有____________种。
已知:
2.乙偶姻中含有碳氧双键,与乙偶姻有关的反应如下:
(2)写出反应①、②的反应类型:
反应①___________、反应②___________。
(3)A的一氯代物只有一种。
写出乙偶姻、C的结构简式:
乙偶姻__________________、C_________________。
(4)写出D→E反应的化学方程式__________________________________。
(5)设计实验方案。
.检验F中的官能团,
.完成反应③的转化的实验操作
答案
(1)4(各2分)
(2)消去反应(2分)加聚反应(2分)
(3)
(各2分)
(4)
(3分)
(5)取少量乙醛溶液置于试管中,加入新制的氢氧化铜悬浊液,加热,产生红色沉淀。
(3分) 取一根一端绕成螺旋状的光洁铜丝,放在酒精灯外焰加热,观察到铜丝表面由红变黑,立即把它伸入盛有乙醇的试管中,反复几次,并闻到液体有刺激性气味,观察到铜丝表面变红。
(3分)
28.由乙烯和其它无机原料合成环状化合物其合成过程如下(水及其它无机产物均已省略):
请分析后回答下列问题:
(1)反应的类型分别是
①___________、②________________;
(2)D物质中的官能团为___________________;
(3)C物质的结构简式___________________,物质X与A互为同分异构体,则X的结构简式为_________________,X的名称为_______________________________;
(4)B、D在一定条件下除能生成环状化合物E外,还可在一定条件下反应生成一种高分子化合物,试写出B、D反应生成该高分子化合物的方程式:
_____________________________________________________________________________
29.已知一个碳原子上连有两个羟基时,其结构极不稳定,易发生下列变化,生成较稳
定物质:
如:
A-F是六种有机化合物,它们之间的关系如下图,请根据要求回答:
(1)在一定条件下,经反应①后,生成C和D,C的分子式为,反应①的类型为。
(2)反应③的化学方程式为.
(3)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2):
n(H2O)=2:
1,则B的分子式为。
(4)F是高分子光阻剂生产中的主要原料。
F具有如下特点:
①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种。
F在一定条件下发生加聚反应的化学方程式为。
(5)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。
G有种
结构,写出其中两种同分异构体的结构简式、。
答案28.(共8分)
(1)①加成反应酯化反应(或“取代反应”)
—COOH
(2)或羧基
(3)OHC—CHOH3C—CH—Br1,1—二溴乙烷
(4)
(2分)
29.(12分)
(1)C2H4O取代反应(5)4种(2分)
28.汽油中支链烃和环烃越多,汽油质量越高,通常用辛烷(2,2,3,3—四甲基丁烷)值来表示汽油质量。
辛烷值越高,汽油的质量就越高。
无铅汽油通常是加入甲基叔丁基醚作为高辛烷值组成。
甲基叔丁基醚难溶于水。
用以下两种方案制甲基叔丁基醚。
方案甲:
(甲基叔丁基醚)
(叔丁醇)
方案乙:
(1)叔丁醇的系统命名为;它有4种醇类同分异构体,写出其中一种的结构简式___________________,它还有多种醚类同分异构体,其中一种可由乙醇在浓硫酸作用下分子间脱水生成,其结构简式为_________________________。
(2)已知醇在铜的催化下可发生氧化反应,如
试推测叔丁醇是否能发生类似反应_______(填“能”、“不能”)。
(3)已知CH3CH2OH有3种不同化学环境的氢原子,则叔丁醇有____种不同化学环境的氢原子。
(4)方案乙不如方案甲,因为方案乙会发生两种类型的副反应,生成________________、______________________、______________________(写结构简式)等副产品。
(5)甲方案中,分离两种生成物以得到甲基叔丁基醚粗产品的方法是________。
a.水洗分液法b.蒸馏法c.过滤法
29.烯烃复分解反应实现了有机物碳碳双键两边基团的换位。
如:
2CH2=CHCl
CH2=CH2+ClCH=CHCl
又知羟基在一端的醇在一定条件下可直接氧化为羧酸,E是一种氯代二元羧酸。
现以丙烯为主要原料合成乙酸和聚合物
(1)写出下列结构简式:
A_________________,B___________________。
(2)写出反应类型:
反应①____________,反应②____________,反应③____________。
(3)不是由C直接转化为F,而是C先与HCl加成,这一步的目的是_________________。
(4)完成E→F的化学方程式___________________________;反应类型_______________。
28.(8分)
(1)2-甲基2-丙醇(1分);CH3CH2CH2CH2OH,CH3CH2OCH2CH3(各1分,共2分)
(2)不能(1分)
(3)2(1分)
(4)CH3OCH3、
、
(2分,少写1种扣1分)
(5)a(1分)
29.(12分)
(1)A、CH3CHO(2分)B、ClCH2CH=CHCH2Cl(2分)
(2)①取代反应(1分)②取代反应(1分)③氧化反应(1分)
(3)保护碳碳双键不被氧化(2分)
(4)
(2分。
不写H2O不给分,不写条件扣1分)消去反应(1分)
8.下图是一种形状酷似一条小狗的有机物,化学家TimRickard将其取名为
“doggycene”,有关doggycene的说法正确的是
A.该有机物属于苯的同系物
B.“doggycene”可以使溴水褪色
C.该物质常温下为气态
D.1mol该物质在氧气中完全燃烧生成CO2和水的物质的量之比为2:
1
28.下列是有机化合物A的转化过程:
(1)若D在一定条件可以氧化为B,则A的结构简式:
。
(2)若有X、Y两物质与A是同类物质的同分异构体,也能发生上述转化。
①若B能发生银镜反应;C不能发生消去反应,则X的结构简式;
②若B,D均不能发生银镜反应;则Y的可能的结构简式。
(3)若Z与A为不同类别同分异构体,并且具有下列性质:
①Z不能与NaHCO3溶液反应;②Z不能使溴水褪色;
③1摩尔Z与足量金属钠反应可以生成1摩尔H2;
④Z分子的一氯取代产物只有二种(不考虑立体异构现象)。
则Z的结构简式。
29.在有机分析中,常用臭氧化分解来确定有机物中碳碳双键的位置与数目。
如:
(CH3)2C=CH-CH3(CH3)2C=O+CH3CHO
某有机物A经臭氧化分解后发生下列一系列的变化:
已知A的分子结构中有两个六元环;B不能发生银镜反应;1摩尔F与足量银氨溶液完全反应可以生成2摩尔银。
试回答下列问题:
(1)有机物A、B的结构简式为A:
________E:
_______。
(2)写出下列反应类型D→E:
;G→H:
。
(3)写出下列反应的化学方程式:
①C→D:
;②H→I:
。
;
(4)写出与F具有相同分子式,含有六元环、属于酯类的同分异构体的结构简式:
。
(任意写出两种)
28.(共8分)
(1)A的结构简式:
CH3CH2COOCH2CH2CH3(2分)
(2)①XHCOOCH2C(CH3)3(2分);②YCH3COOCH(CH3)C2H5
、CH3CH2COOCH(CH3)2(2分)
(3)Z的结构简式。
(2分)
29.(共12分)
(1)结构简式为A:
(2分)
E:
。
(2分)
(2)反应类D→E:
加聚反应;G→H:
加成反应(还原反应)。
(2分)
(3)化学方程式:
①C→D:
;(2分)
②H→I:
。
(2分)
(4)结构简式:
。
(2分)
15、食品香精菠萝酯的生产路线(反应条件略去)如下:
下列叙述错误的是
A.苯氧乙酸和菠萝酯均可与NaOH溶液发生反应
B.苯酚和菠萝酯均可发生氧化反应
C.步骤
(1)产物中残留的苯酚可用FeCl3溶液检验
D.步骤
(2)产物中残留的烯丙醇可用溴水检验
16.被称为“魔棒”的荧光棒已成为节日之夜青少年的喜爱之物,其发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光。
草酸二酯(CPPO)结构简式为:
下列有关说法不正确的是:
A.发光的魔棒不能凑近石油气之类的可燃性气体,否则会导致爆炸
B.草酸二酯的分子式为:
C26H24O8Cl6
C.如果在发光中途,把它放入冰箱的冷冻室中,发光便会停止或基本停止
D.1molCPPO与氢氧化钠稀溶液反应(苯环上卤素不水解),最多消耗4molNaOH
28、某厂以甘蔗为原料制糖,对产生的大量甘蔗渣按下图所示转化进行综合利用。
其中B是A水解的最终产物;C的化学式为C3H6O3,一定条件下2个C分子间脱去2个水分子可生成一种六元环状化合物;D可使溴水褪色;H的三聚合物I也是一种六元环状化合物。
(图中部分反应条件及产物没有列出)
(1)写出下列物质的结构简式:
高分子化合物F___________________;六元环状化合物I___________________。
(2)C→D的反应类型为_________________D→E的反应类型为_____________。
(3)写出下列反应的化学方程式:
A→B_________________________________________________________
C→可降解塑料_________________________________________________。
29、某有机物X(C11H9O6Br)分子中有多种官能团,其结构简式为:
(其中Ⅰ、Ⅱ为未知部分的结构),为推测X的分子结构,进行如下转化
已知向D的水溶液中滴入FeCl3溶液发生显色反应,滴入NaHCO3溶液有无色无味
气体产生,且D苯环上的一氯代物有两种。
(1)D中含氧官能团的名称:
;X的结构简式:
(2)写出B→E的化学方程式:
(3)D不可能发生的反应有:
A.加成反应B.消去反应C.取代反应D.氧化反应E.加聚反应
(4)D有多种同分异构体,遇FeCl3溶液发生显色反应,又能发生银镜反应,其中能水解的同分异构体的结构简式为:
,其中不能水解的同分异构体的结构简式为:
(各写出一种)
28、(本题共8分)
(1)(各1分,共2分)
(2)(各1分,共2分)消去反应酯化反应(或取代反应)
(3)(各2分,共4分)
29.(本题共12分)
(1)羟基羧基(各1分,共2分)
(2分)
(2)HOCH2—CH2OH+O2OHC—CHO+2H20(2分)(3)BE(2分)
(4)(各2分,共4分)
(其他合理答案也可)
29.已知:
CH2=CH—CH=CH2+CH2=CH2
,物质A在体内脱氢酶的作用下会氧化为有害物质GHB。
下图是关于物质A的一种制备方法及由A引发的一系列化学反应。
请回答下列问题:
⑴写出反应类型反应①反应③。
⑵写出化合物B的结构简式。
⑶写出反应②的化学方程式。
⑷写出反应④的化学方程式。
⑸反应④中除生成外,还可能存在一种副产物(含
结构),它的结构简式为。
⑹与化合物互为同分异构体的物质不可能为(填写字母)。
a.醇b.醛c.羧酸d.酚
29.(本题共12分)
⑴加成反应消去反应⑵HOCH2CH2CH2CHO
⑶HOCH2CH2CH2COOH
+H2O
⑷CH2=CHJ-CH=CH2+CH2=CH-COOH
⑸
⑹d
29.以石油裂解气为原料,通过一系列化学反应可得到重要的化工产品增塑剂G。
请完成下列各题:
(1)写出反应类型:
反应①反应④
(2)写出反应条件:
反应③反应⑥
(3)反应②③的目的是:
。
(4)写出反应⑤的化学方程式:
。
(5)B被氧化成C的过程中会有中间产物生成,该中间产物可能是(写出一种物质的结构简式),检验该物质存在的试剂是。
(6)写出G的结构简式。
29.
(1)加成反应取代反应
(2)NaOH/醇溶液(或KOH醇溶液)NaOH/水溶液
(3)防止双键被氧化
(4)CH2=CHCH2Br+HBrCH2Br—CH2—CH2Br
(5)HOCH2CHClCH2CHO或OHCCHClCH2CHO或OHCCHClCH2COOH新制氢氧化铜悬浊液
(6)
1.氢氧化镁固体在水中溶解,有下列平衡:
Mg(OH)2(s)
Mg2++2OH―,加入下列哪种物质可使Mg(OH)2固体的质量减少
A.Na2CO3 B.MgCl2 C.NH4Cl D.NaCl
2.已知25℃时,Agl饱和溶液中c(Ag+)为1.22×10-8mol·L-1,AgCl的饱和溶液中c(Ag+)为1.30×10-5mol·L-1。
若在5mL含有KCl和KI浓度均为0.01mol·L-1的混合溶液中,滴加8mL0.01mol·L-1的AgNO3溶液,则下列叙述中不正确的是
A.溶液中所含溶质的离子浓度大小关系为:
c(K+)>c(NO—3)>c(Ag+)>c(Cl-)>c(I-)
B.溶液中先产生的是AgI沉淀
C.AgCl的KSP的数值为1.69×10-10
D.若在AgI县浊液中滴加少量的KCl溶液,黄色沉淀不会转变成白色沉淀
3.以下是25℃时几种难溶电解质的溶解度:
难溶电解质
Mg(OH)2
Cu(OH)2
Fe(OH)2
Fe(OH)3
溶解度/g
9×10-4
1.7×10-6
1.5×10-4
3.0×10-9
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子。
例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可。
请回答下列问题:
(1)上述三个除杂方案都能够达到很好效果,Fe2+、Fe3+都被转化为_______________(填化学式)而除去。
(2)①中加入的试剂应该选择_________为宜,其原因是________________________。
(3)②中除去Fe3+所发生的总反应的离子方程式为_____________________________。
(4)下列与方案③相关的叙述中,正确的是__________________(填字母)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+一定不能大量存在
(1)氢氧化铁
(2)氨水;不会引入新的杂质
(3)2Fe3++3Mg(OH)2==3Mg2++2Fe(OH)3
(4)ACDE
4.某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。
下列说法正确的是
提示:
BaSO4(s)
Ba2+(aq)+SO42-(aq)的平衡常数Ksp=c(Ba2+)·c(SO42-),称为溶度积常数。
A.加入Na2SO4可以使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
5.当固体AgCl放在较浓的KI溶液中振荡时,则部分AgCl转化为AgI,原因是
A.AgI比AgCl稳定 B.碘氧化性比氯弱
C.I-的还原性比Cl-强 D.溶解度AgI比AgCl小
6.常温下,0.1mol·L—1某一元酸(HA)溶液中
=1×108,下列叙述正确的是
A.该一元酸溶液的pH=1
B.该溶液中由水电离出的c(H+)=1×10-11mol·L—1
C.该溶液中水的离子积常数为1×10-22
D.用pH=11的NaOH溶液V1L与V2L0.1mol·L—1该一元酸(HA)溶液混合,若混合溶液的pH=7,则V1<V2
7.一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示。
则下列说法错误的是
A.醋酸的电离度:
c<b<a
B.溶液的PH值:
b<a<c
C.蘸取a点溶液滴在湿润的PH试纸上,测得PH值一定偏大
D.若分别取a、b、c三点的溶液各10mL,各用同浓度的氢氧化钠溶液中和,消耗NaOH溶液的体积a>b>c
8.已知0.1mol/L的醋酸溶液中存在电离平衡:
CH3COOH
CH3COO-+H+要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是
A、加少量烧碱溶液 B、升高温度 C、加少量冰醋酸 D、加水
9.根据酸碱质子理论,凡是能给出质子的分子或离子都是酸,凡是能结合质子的分子或离子都是碱。
按照这个理论,下列微粒属于两性物质的是:
①HS一 ②CO32一③H2PO4一④NH3 ⑤H2S ⑥CH3COOH ⑦OH一⑧H2O ⑨NO2一 ⑩H2NCH2COOH
A.①⑤ B.③⑥ C.①②⑨ D.①③⑧⑩
10.已知25℃时0.1mol·L-1醋酸溶液的pH约为3,向其中加入少量醋酸钠晶体,待晶体溶解后发现溶液的pH增大。
对上述现象有两种不同的解释:
甲同学认为醋酸钠水解呈碱性,增大了c(OH-),因而溶液的pH增大;乙同学认为醋酸钠溶于水电离出大量醋酸根离子,抑制了醋酸的电离,使c(H+)减小,因而pH增大。
你认为上述解释中 (“甲”或“乙”)正确。
(1)为了验证上述哪种解释正确,继续做如下实验:
向0.1mol·L-1的醋酸溶液中加入少量的下列物质中的 (填写编号),然后测定溶液的pH。
A.固体CH3COOK B.固体CH3COONH4
C.气体NH3 D.固体NaHCO3
(2)若 (填“甲”或“乙”)的解释正确,溶液的pH应 (填“增大”“减少”或“不变”)。
答案:
乙
(1)B
(2)乙增大
11.能说明醋酸是弱电解质的是
①用浓硫酸和醋酸钠固体共热可制得醋酸 ②醋酸钠溶液呈碱性
③可以用食醋清除热水瓶内的水垢 ④pH=2的醋酸溶液稀释1000倍后pH小于5
A.①③④ B.①② C.②④ D.②
12.已知酸性强弱顺序为H2CO3>
>HCO3-,下列化学方程式正确的是BC
25.下图表示373K时,反应A(g)
2B(g)在前110s内的反应进程(将该反应看作匀速进行)
(1)写出该反应的化学平衡常数表达式K=_____________________
T(K)
273
323
373
K
0.0005
0.022
0.36
(2)A(g)
2B(g)在不同温度下的K值见上表,则该反应的逆反应为_________反应(填“放热”或“吸热”)。
从开始至第一次达到平衡过程中,用B表示反应平均速率为_______。
(3)温度升高,B的转化率_____________(填“增大”、“减小”、或“不变“,下同),B的反应速率___________。
(4)373K时,将A气体放入一密闭容器内进行反应。
根据图判断:
90~100s时,曲线变化的原因是(文字表达式)____________________________________。
反应进行至70s时,改变的条件可能是___________(填编号)。
A.加入负催化剂B.扩大容器体积C.升高温度D.增加A的浓度
25⑴K=[B]2/[A]
(2)放热2X10-3mol/l.S2分
(3)减小增大(4)加入了A物质B
23、下表是元素周期表的一部分。
表中所列的字母分别代表某一化学元素。
请你根据表中所给元素,回答下列问题
⑴L层上未成对电子数最多的元素是(填元素符号),原子核外有5种不同能量的电子且最外层上p电子数比s电子数多2个的元素是(填元素符号)
(2)h和g的最高价氧化物比较,熔点高的是(填写氧化物化学式),其理由是;j和k的氢化物比较,沸点高的是(填写氢化物化学式),其理由是
(3)以上元素两两形成的中学中常见的化合物中既有离子键,又有非极性共价键的有
(写一种)(填写化学式)
(4)b、i、l三元素形成的离子化合物的电子式为
23、(每空1分,共8分)
(1)N,S
⑵SiO2,SiO2是原子晶体,而CO2是分子晶体;H2O,水分子间作用力大于H2S分子间作用力;(3)Na2O2(或FeS2;Na2SX等等,填写任意一个正确的即可);
(4)
30、白云石化学式为CaCO3·xMgCO3。
以它为原料,可制取耐火材料MgO等。
称取27.6g白云石样品,高温加热到质量不再变化,收集到CO2的体积为6.72L(标准状况)。
(1)计算白云石化学式中的X值
(2)该样品高温条件下充分反应后剩余固体的质量?
(3)该样品高温条件下充分反应后剩余固体中MgO的质量?
30、