实验--二氧化氮的测定_精品文档.ppt
《实验--二氧化氮的测定_精品文档.ppt》由会员分享,可在线阅读,更多相关《实验--二氧化氮的测定_精品文档.ppt(21页珍藏版)》请在冰豆网上搜索。
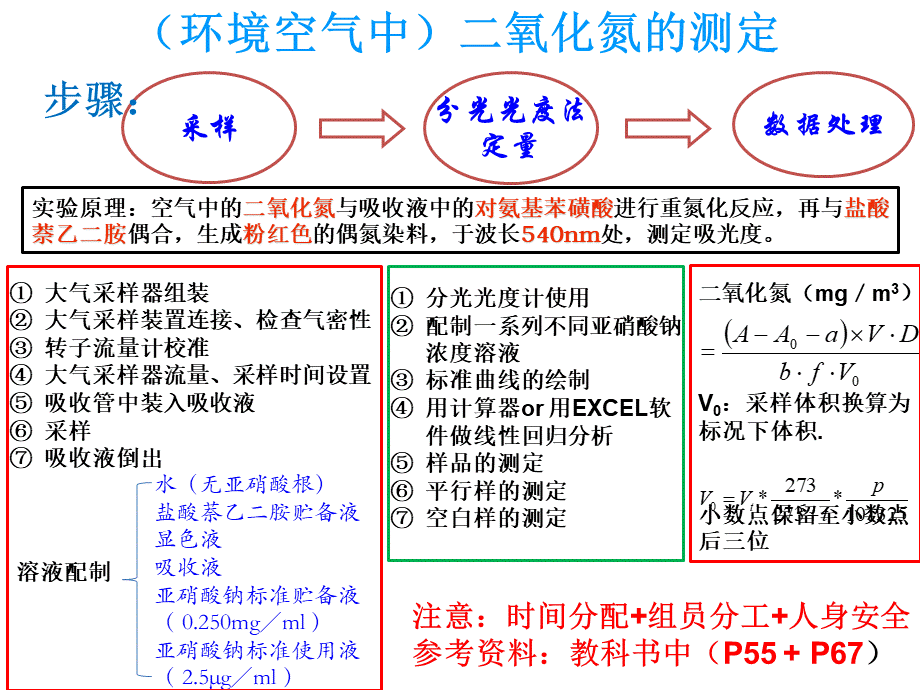
(环境空气中)二氧化氮的测定,大气采样器组装大气采样装置连接、检查气密性转子流量计校准大气采样器流量、采样时间设置吸收管中装入吸收液采样吸收液倒出,溶液配制,水(无亚硝酸根)盐酸萘乙二胺贮备液显色液吸收液亚硝酸钠标准贮备液(0.250mgml)亚硝酸钠标准使用液(2.5gml),实验原理:
空气中的二氧化氮与吸收液中的对氨基苯磺酸进行重氮化反应,再与盐酸萘乙二胺偶合,生成粉红色的偶氮染料,于波长540nm处,测定吸光度。
分光光度计使用配制一系列不同亚硝酸钠浓度溶液标准曲线的绘制用计算器or用EXCEL软件做线性回归分析样品的测定平行样的测定空白样的测定,二氧化氮(mgm3)V0:
采样体积换算为标况下体积.小数点保留至小数点后三位,步骤:
注意:
时间分配+组员分工+人身安全参考资料:
教科书中(P55+P67),采样,采样:
方法:
溶液吸收法吸收液:
对氨基苯磺酸和盐酸萘乙二胺配制而成。
短时间采样(1h以内):
取一支多孔玻板吸收瓶,装入10.0ml吸收液,标记吸收液液面位置后以0.4Lmin的流量,采集环境空气624L。
长时间采样(24h以内):
用大型多孔玻板吸收瓶,内装25.0ml或50.0ml吸收液,液柱不低于80mm,标记吸收液液面位置,使吸收液的温度保持在204,以0.2Lmin的流量,采集环境空气288L。
注意:
采样期间、样品运输和存放过程中应避免阳光照射。
气温超过24时,长时间(8h以上)运输和存放样品应采取降温措施。
分光光度法分光光度计定量步骤:
标准色列的配制测定标准色列的吸光度绘制工作曲线样品吸光度的测定样品中二氧化氮的含量,相关反应:
歧化反应:
NO2+H2OHNO2+HNO3重氮化反应:
HNO2+对氨基苯磺酸+乙酸重氮化合物偶氮反应:
重氮化合物+盐酸萘乙二胺偶氮染料(粉红色),干扰及消除臭氧:
浓度超过0.25mgm3,产生负干扰,采样时在吸收瓶入口处串接一段1520cm长的硅橡胶管,可消除干扰。
方法最低检出浓度方法检出限为0.12g/10ml。
当吸收液体积为10ml,采样体积为24L时,空气中二氧化氮的最低检出浓度为0.005mgm3。
仪器试剂水:
无亚硝酸根的水1.00g/L盐酸萘乙二胺贮备液:
称取0.50g盐酸萘乙二胺于500ml容量瓶中,用水稀释至标线。
此溶液贮于密封的棕色试剂瓶中,在冰箱中冷藏可稳定三个月。
显色液:
称取2.5g对氨基苯磺酸,溶解于约100ml热水中,将溶液冷却至室温,全部移入500ml容量瓶中,加入25.0ml盐酸萘乙二胺贮备液和25ml冰乙酸,用水稀释至标线。
此溶液于密闭的棕色瓶中,在25以下暗处存放,可稳定三个月。
若呈现淡红色,应弃之重配。
500ml/组,也可溶于沸水中配制显色液,可提高其溶解速度,节约时间,且对大气中NO2的测定无显著差异,吸收液:
临用时将显色液和水按41(V/V)比例混合,即为吸收液。
吸收液的吸光度不超过0.005(540nm,1cm比色皿,以水为参比)。
否则,应检查水、试剂纯度或显色液的配制时间和贮存方法。
亚硝酸钠标准贮备液:
0.250mgml。
准确称取0.3750g亚硝酸钠(NaNO2,优级纯,预先在干燥器内放置24h)溶解于水,移入1000ml容量瓶中,用水稀释至标线。
贮于密闭的棕色试剂瓶中,可稳定三个月。
亚硝酸钠标准使用液:
2.5gml。
每组自配500ml。
配制方法:
用单标移液管准确移取1.00ml亚硝酸钠标准贮备液于100ml容量瓶中,用水稀释至标线。
临用前现配。
分析步骤校准曲线的绘制:
每人绘制12条。
取6支10ml具塞比色管,按下表配制亚硝酸钠标准系列。
表1亚硝酸盐标准色列,各管混匀,于暗处放置20min(室温低于20时,显色40min以上),用1cm比色皿,以水为参比,在波长540nm处,测量吸光度。
扣除零浓度的吸光度,对应的浓度(ug/ml),计算标准曲线的回归方程。
ybxa曲线要求:
A00.005a0.005b0.96r0.999,样品测定:
采样后放置20min(室温20以下放置40min以上),用水将采样瓶中吸收液的体积补至标线,混匀,按绘制标准曲线步骤测定样品的吸光度。
注意:
1.若样品的吸光度超过校准曲线的上限,应用空白试样溶液稀释,再测定其吸光度。
2.样品应尽快测定,否则应将样品于低温暗处存放。
样品于30暗处存放可稳定8h;于20暗处存放可稳定24h;于04冷藏至少可稳定3d。
3.吸收液应避光并不能长时间暴露在空气中,以防止光照使吸收显色或吸收空气中的二氧化氮而使试剂空白液吸光度增高。
空白试样的测定:
与采样用吸收液同一批配制的吸收液。
计算二氧化氮(NO2,mgm3)式中:
A样品溶液的吸光度;A0空白试验溶液的吸光度;b标准曲线的斜率,吸光度mlg;a标准曲线的截距;V采样用吸收液体积,ml;V0换算为标准状态(273K、101.325kPa)下的采样体积,L;D样品的稀释倍数;fSaltzman实验系数。
二氧化氮浓度计算结果应准确到小数点后第三位。
Saltzman实验系数(f):
用渗透法制备的二氧化氮校准用混合气体,在采气过程中被吸收液吸收,生成的偶氮染料相当于亚硝酸根的量与通过采样系统的二氧化氮总量的比值。
f=0.88(当空气中二氧化氮浓度高于0.720mgm3时,f=0.77)。
分光光度计的使用检查干燥剂筒内硅胶是否为蓝色,否则,应立即换硅胶。
打开电源开关,开启比色皿暗箱盒调0,关上暗箱盒盖调100%。
调节波长到使用波长,仪器在暗箱盖打开的情况下预热30分钟。
待机状态,暗箱盖应打开。
比色皿配对:
选用吸光度最小的比色皿盛参比溶液。
1、实验室已准备样品吸收液亚硝酸钠标准贮备液(0.250mg/ml)2、同学们需准备工作亚硝酸钠标准使用液的配制(0.00250mg/ml)按比例配制一系列标准溶液分光光度法测标准溶液的吸光度、绘制标准曲线。
分光光度法测定两个采集的平行样,实验要求,使用计算器进行线性回归操作步骤(CASIOfx-82MS)模式初始化:
进入REG模式:
进入线性回归:
清零:
输入数据:
x数据y数据截距a:
斜率b:
相关系数r:
求x:
y数据,SHIFT,CLR,2,=,MODE,3,1,SHIFT,CLR,1,=,,,DT,SHIFT,S-VAR,SHIFT,S-VAR,1,2,SHIFT,3,S-VAR,S-VAR,SHIFT,1,使用Excel软件进行线性回归分析步骤:
演示:
8.实验方案:
写出实验的方法名称和原理;写出本次实验需完成的实验步骤。
根据本次实验的具体要求,列出实验所用仪器清单(包括仪器的名称、规格、数量)。
数据记录。
作业:
某监测点以0.5L/min流量采集空气中NO260min。
用盐酸萘乙二胺分光光度法测得样品溶液和试剂空白溶液的吸光度为0.234和0.003;校准曲线回归方程的斜率和截距分别为0.96和0.004;环境温度和气压分别为30和101.4kPa。
Saltzman实验系数为0.88。
试计算空气中NO2的浓度。