高考化学一轮复习课时训练选修3《物质结构与性质》Word文档格式.docx
《高考化学一轮复习课时训练选修3《物质结构与性质》Word文档格式.docx》由会员分享,可在线阅读,更多相关《高考化学一轮复习课时训练选修3《物质结构与性质》Word文档格式.docx(10页珍藏版)》请在冰豆网上搜索。
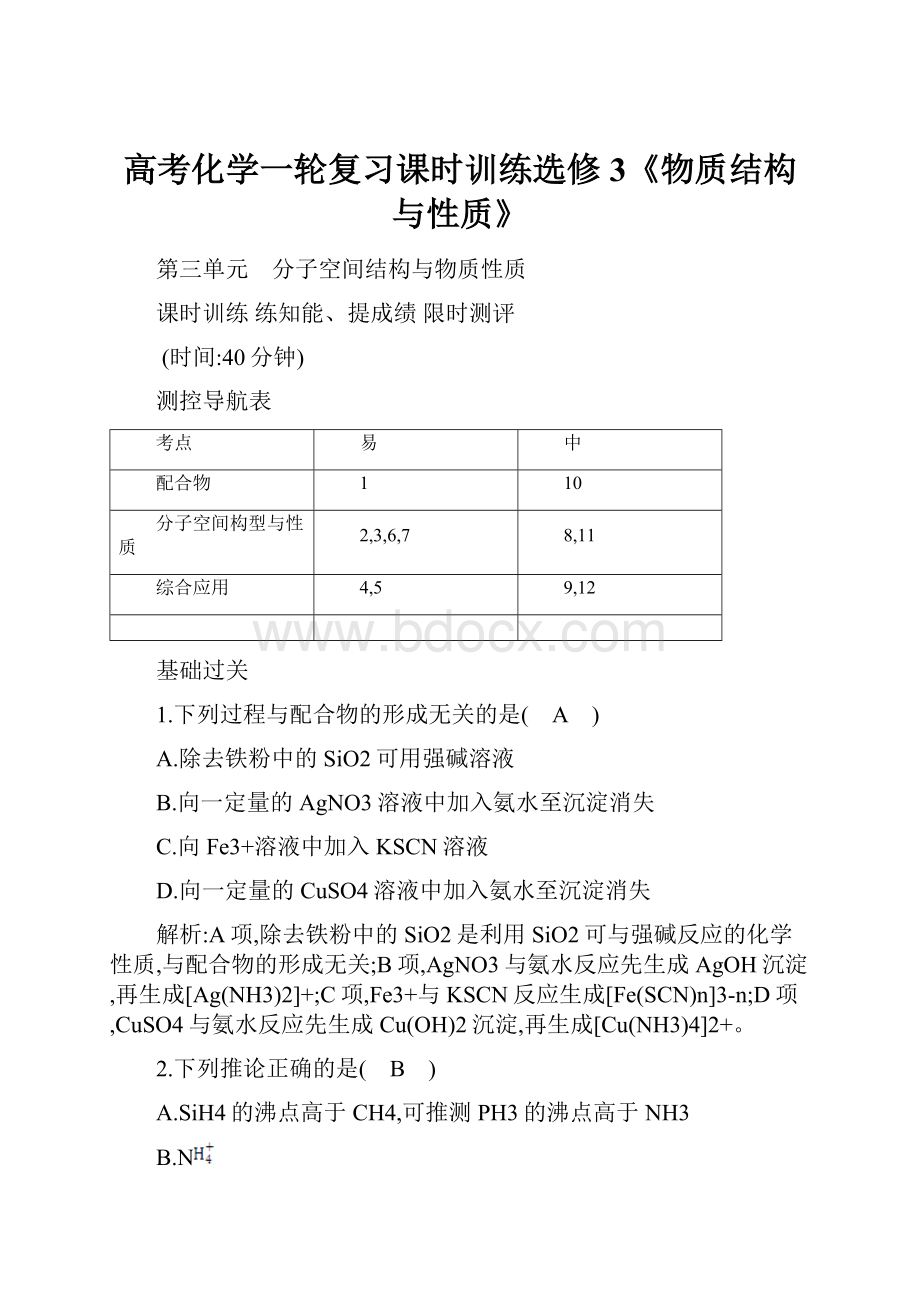
解析:
A项,除去铁粉中的SiO2是利用SiO2可与强碱反应的化学性质,与配合物的形成无关;
B项,AgNO3与氨水反应先生成AgOH沉淀,再生成[Ag(NH3)2]+;
C项,Fe3+与KSCN反应生成[Fe(SCN)n]3-n;
D项,CuSO4与氨水反应先生成Cu(OH)2沉淀,再生成[Cu(NH3)4]2+。
2.下列推论正确的是( B )
A.SiH4的沸点高于CH4,可推测PH3的沸点高于NH3
B.N
为正四面体结构,可推测P
也为正四面体结构
C.CO2晶体是分子晶体,可推测SiO2晶体也是分子晶体
D.C2H6是碳链为直线形的非极性分子,可推测C3H8也是碳链为直线形的非极性分子
NH3分子间存在氢键,沸点反常偏高,大于PH3,A项错误。
N、P是同主族元素,形成的离子:
N
和P
结构类似,都是正四面体构型,B项正确。
CO2是分子晶体,而SiO2是原子晶体,C项错误。
C2H6中两个—CH3对称,是非极性分子,而C3H8是锯齿形结构,是极性分子,D项错误。
3.下列关于粒子结构的描述不正确的是( C )
A.H2S和NH3均是价电子总数为8的极性分子
B.HS-和HCl均是含一个极性键的18电子粒子
C.CH2Cl2和CCl4均是四面体构型的非极性分子
D.1molD216O中含中子、质子、电子各10NA个(NA代表阿伏加德罗常数)
A项中H2S和NH3都是价电子总数为8的极性分子,正确;
B项中HS-和HCl都只含一个极性键,且都具有18个电子,正确;
C项中CH2Cl2是极性分子,四面体构型,CCl4是非极性分子,正四面体构型,不正确;
D项中1个氘原子D
H)中含1个质子、1个电子、1个中子,故1molD216O中含中子、质子、电子各10NA个,正确。
4.下列描述中正确的是( C )
①CS2为V形的极性分子
②Cl
的空间构型为平面三角形
③SF6中有6对完全相同的成键电子对
④SiF4和S
的中心原子均为sp3杂化
A.①②B.②③C.③④D.②④
CS2与CO2结构类似,为直线形非极性分子,①错误;
由价层电子对互斥理论可知Cl
中中心原子的价层电子数=
(7+1)=4,孤电子对数为1,所以Cl
是三角锥形,②错误;
硫原子最外层有6个电子,和氟原子之间有6对完全相同的成键电子对,③正确;
SiF4和S
的空间构型分别为正四面体和三角锥形,但中心原子均采用的是sp3杂化,④正确。
5.(2014山西沂州实验中学模拟)下列判断正确的是( D )
A.元素周期表中查得的相对原子质量为同位素的相对原子质量
B.化学键的变化一定会引起化学反应的变化
C.只含有共价键的物质一定是共价化合物
D.全部由极性键构成的分子不一定是极性分子
元素周期表中查得的相对原子质量为元素的相对原子质量,A项错误;
化学键的变化不一定生成新物质,所以不一定是化学反应的变化,B项错误;
只含有共价键的物质还有可能是单质,C项错误。
6.(2013山东潍坊模拟)在以下的分子或离子中,空间结构的几何形状不是三角锥形的是( C )
A.NF3B.C
C.BF3D.H3O+
中心原子的价层电子对数目,NF3、C
、H3O+均为4,σ键电子对均为3,孤电子对均为1,所以分子构型为三角锥形;
只有BF3中的价层电子对数=σ键电子对数=3,无孤电子对,所以形成平面正三角形分子。
7.(2013福建师大附中三模)
(1)铬的外围电子排布式是 ,与铬同周期,最外层有3个未成对电子数的元素名称是 ,该元素对应的最低价氢化物分子的中心原子采取了 杂化方式,分子的空间构型是 。
(2)富勒烯(C60)的结构如图,1molC60分子中σ键的数目为 。
继C60后,科学家又合成了Si60、N60。
请解释如下现象:
熔点:
Si60>
N60>
C60,而破坏分子所需要的能量:
C60>
Si60,其原因是
。
(3)氟化氢水溶液中存在氢键有 种。
(4)2011年诺贝尔化学奖授予了因发现准晶体材料的以色列科学家。
某准晶体是锰与另一个短周期元素X形成的凝固态。
已知:
金属的电负性一般小于1.8。
元素X与同周期相邻元素Y、Z的性质如下表:
Y
X
Z
与H+反应放
出H2
与H+、OH-反应
放出H2
与OH-反应放
则X元素符号是 ,锰与X在准晶体中的结合力为 。
(1)24Cr元素原子的外围电子排布式遵从构造原理和洪特规则特例为3d54s1,第四周期元素中原子最外层有3个未成对电子的是砷(As)元素,该元素氢化物AsH3分子结构与NH3分子相似,As原子以sp3方式杂化,分子的空间构型是三角锥形。
(2)富勒烯(C60)中每个C原子与另外3个C原子形成3个σ键,平均每个C原子所有3×
=1.5个,故1个C60分子中有60×
1.5=90个,1molC60分子中有90NA个σ键,组成和结构相似的分子相对分子质量越大,分子间作用力越大,熔、沸点越高,而共价分子的价键越短,键越牢固,分子越稳定,因为相对分子质量Si60>
C60,而原子半径r(N)<
r(C)<
r(Si),故有此现象。
(3)氟化氢水溶液中存在F—H…F、F—H…O、O—H…F、O—H…O4种氢键。
(4)根据短周期元素X具有两性推导出X是Al元素,合金中金属离子间也是通过自由电子形成金属键。
答案:
(1)3d54s1 砷 sp3 三角锥形
(2)90NA 由于结构相似的分子晶体的相对分子质量越大,分子间作用力(或范德华力)越强,熔化所需的能量越多,故熔点是Si60>
C60;
由于成键原子半径越小,形成的共价键越强,断键所需能量越多,故破坏分子需要的能量顺序为N60>
Si60(合理答案均可)
(3)4 (4)Al 金属键
8.(2013武汉二中模拟)试依次回答下列相关问题:
(1)写出磷原子M能层的电子排布式:
。
(2)磷有两种氧化物P4O6和P4O10,其球棍模型结构如图所示。
其中磷元素的杂化类型分别是 。
(3)磷有三种含氧酸H3PO2、H3PO3、H3PO4,其中磷元素均以sp3杂化与相邻原子形成四个σ键,则H3PO3的结构式是 ,写出H3PO2与足量氢氧化钠溶液反应的化学方程式:
。
(4)磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层。
磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成。
①写出合成磷化硼的化学反应方程式:
。
②三溴化硼分子和三溴化磷分子的立体构型分别是 、 。
(1)是3s23p3。
(2)P4O6中每个P与其周围三个O形成三角锥形,故P采取sp3杂化,P4O10中每个P与其周围4个O形成正四面体形,故P也采取sp3杂化。
(3)4个sp3杂化轨道全部参与成键,说明有4个原子直接与P相连,有两种情况:
、(不稳定),只能是,同理可知H3PO2为,只有1个羟基氢显酸性,可被NaOH中和。
(4)②三溴化硼中硼原子采取sp2杂化,是平面三角形,而三溴化磷中磷原子是sp3杂化,有一个杂化轨道被孤电子对占据,是三角锥形。
(1)3s23p3
(2)sp3、sp3
(3)
NaOH+H3PO2NaH2PO2+H2O
(4)①BBr3+PBr3+3H2BP+6HBr
②平面三角形 三角锥形
能力提升
9.下列叙述中正确的是( C )
A.P4和NO2都是共价化合物
B.CCl4和NH3都是以极性键结合的极性分子
C.在CaO和SiO2晶体中,都不存在单个小分子
D.甲烷的结构式:
是对称的平面结构,所以是非极性分子
A中P4属于单质;
B中的NH3属于以极性键结合的极性分子,而CCl4是非极性分子;
D中CH4属于正四面体结构,是非极性分子;
原子晶体和离子晶体中均无小分子,C正确。
10.Co(Ⅲ)的八面体配合物CoClm·
nNH3。
若1mol配合物与AgNO3作用生成1molAgCl沉淀,则m、n的值是( B )
A.m=1 n=5B.m=3 n=4
C.m=5 n=1D.m=4 n=5
由1mol配合物生成1molAgCl知,1mol配合物电离出1molCl-,即配离子显+1价,外界有一个Cl-,又因Co显+3价,故[CoClm-1·
nNH3]+中有两个Cl-,又因为是八面体,配位数为6,所以n=6-2=4。
11.(2012年福建理综)
(1)元素的第一电离能:
Al Si(填“>
”或“<
”)。
(2)基态Mn2+的核外电子排布式为 。
(3)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:
①在Xm-中,硼原子轨道的杂化类型有 ;
配位键存在于 原子之间(填原子的数字标号);
m= (填数字)。
②硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有 (填序号)。
A.离子键 B.共价键 C.金属键
D.范德华力 E.氢键
(1)同一周期元素自左向右第一电离能有增大趋势,故第一电离能Al<
Si。
(2)Mn是25号元素,其核外电子排布式为
1s22s22p63s23p63d54s2,故Mn2+的核外电子排布式为
1s22s22p63s23p63d5。
(3)硅烷形成的晶体是分子晶体,相对分子质量越大,分子间范德华力越强,沸点越高。
(4)①由球棍模型可以看出,大黑球为B原子,灰球为O原子,小黑球为H原子。
2号B原子形成3个键,采取sp2杂化,4号B原子形成4个键,采取sp3杂化;
4号B原子三个sp3杂化轨道与除5号O原子外的三个O原子形成σ键后还有一个空轨道,而5号O原子能提供孤电子对而形成配位键;
由图示可以看出该结构可以表示为[B4H4O9]m-,其中B为+3价,O为-2价,H为+1价,可知m=2。
②在晶体中Na+与Xm-之间为离子键,H2O分子间存在范德华力,而该阴离子能与水分子形成氢键。
(1)<
(2)1s22s22p63s23p63d5(或[Ar]3d5)
(3)硅烷的相对分子质量越大,分子间范德华力越强(或其他合理答案)
(4)①sp2、sp3 4,5(或5,4) 2 ②ADE
12.(2013年新课标全国理综Ⅰ)硅是重要的半导体材料,构成了现代电子工业的基础。
回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号为 ,该能层具有的原子轨道数为 、电子数为 。
(2)硅主要以硅酸盐、 等化合物的形式存在于地壳中。
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以 相结合,其晶胞中共有8个原子,其中在面心位置贡献 个原子。
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备。
工业上采用Mg2Si和NH4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为 。
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
化学键
C—C
C—H
C—O
Si—Si
Si—H
Si—O
键能/(kJ·
mol-1)
356
413
336
226
318
452
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是
②SiH4的稳定性小于CH4,更易生成氧化物,原因是
(6)在硅酸盐中,Si
四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。
图(b)为一种无限长单链结构的多硅酸根;
其中Si原子的杂化形式为 ,Si与O的原子数之比为 ,化学式为 。
(1)基态硅原子有三个电子层,最外层能量最高,其符号为M,3s轨道数为1,3p为3,3d为5,合计轨道数为9,电子数为4。
(2)硅主要以SiO2、硅酸盐形式存在于地壳中。
(3)在硅晶体中,硅原子间以共价键结合,晶胞的6个面中各有一个硅原子,依据均摊法知,面心位置贡献了3个硅原子。
(4)由题干信息知:
Mg2Si与NH4Cl反应,其产物应有SiH4、MgCl2,再结合原子守恒分析知还有NH3,则其反应式为:
Mg2Si+4NH4Cl4NH3+2MgCl2+SiH4。
(5)①物质内化学键的强弱影响物质的稳定性,进而影响物质构成种类数。
②Si—H键的键能小,稳定性差,SiH4易生成稳定性强的氧化物。
(6)因Si与O形成四面体结构,则其杂化形式为sp3杂化,图(b)中每个四面体中有两个氧原子是与其他四面体共用的,则每个四面体占有该氧原子的
所以每个四面体共占有这两个氧原子为:
2×
=1,另1个氧原子为该四面体所有,还含有1个Si—O键属于该四面体,综上所述,一个四面体中,含1个Si原子,氧原子:
1+1+1=3,所以,硅与氧原子数之比为1∶3,其化学式为Si
或[SiO3
(1)M 9 4
(2)二氧化硅 (3)共价键 3
(4)Mg2Si+4NH4ClSiH4+4NH3+2MgCl2
(5)①C—C键和C—H键较强,所形成的烷烃稳定,而硅烷中Si—Si键和Si—H键的键能较低,易断裂,导致长链硅烷难以生成
②C—H键的键能大于C—O键,C—H键比C—O键稳定,而Si—H键的键能却远小于Si—O键,所以Si—H键不稳定而倾向于形成稳定性更强的Si—O键
(6)sp3 1∶3 [SiO3
(或Si
)