近六年全国新课标理综化学考点分布及近五年全国新课标卷化学试题每道题地考点及分值分布表二合一文档格式.docx
《近六年全国新课标理综化学考点分布及近五年全国新课标卷化学试题每道题地考点及分值分布表二合一文档格式.docx》由会员分享,可在线阅读,更多相关《近六年全国新课标理综化学考点分布及近五年全国新课标卷化学试题每道题地考点及分值分布表二合一文档格式.docx(21页珍藏版)》请在冰豆网上搜索。
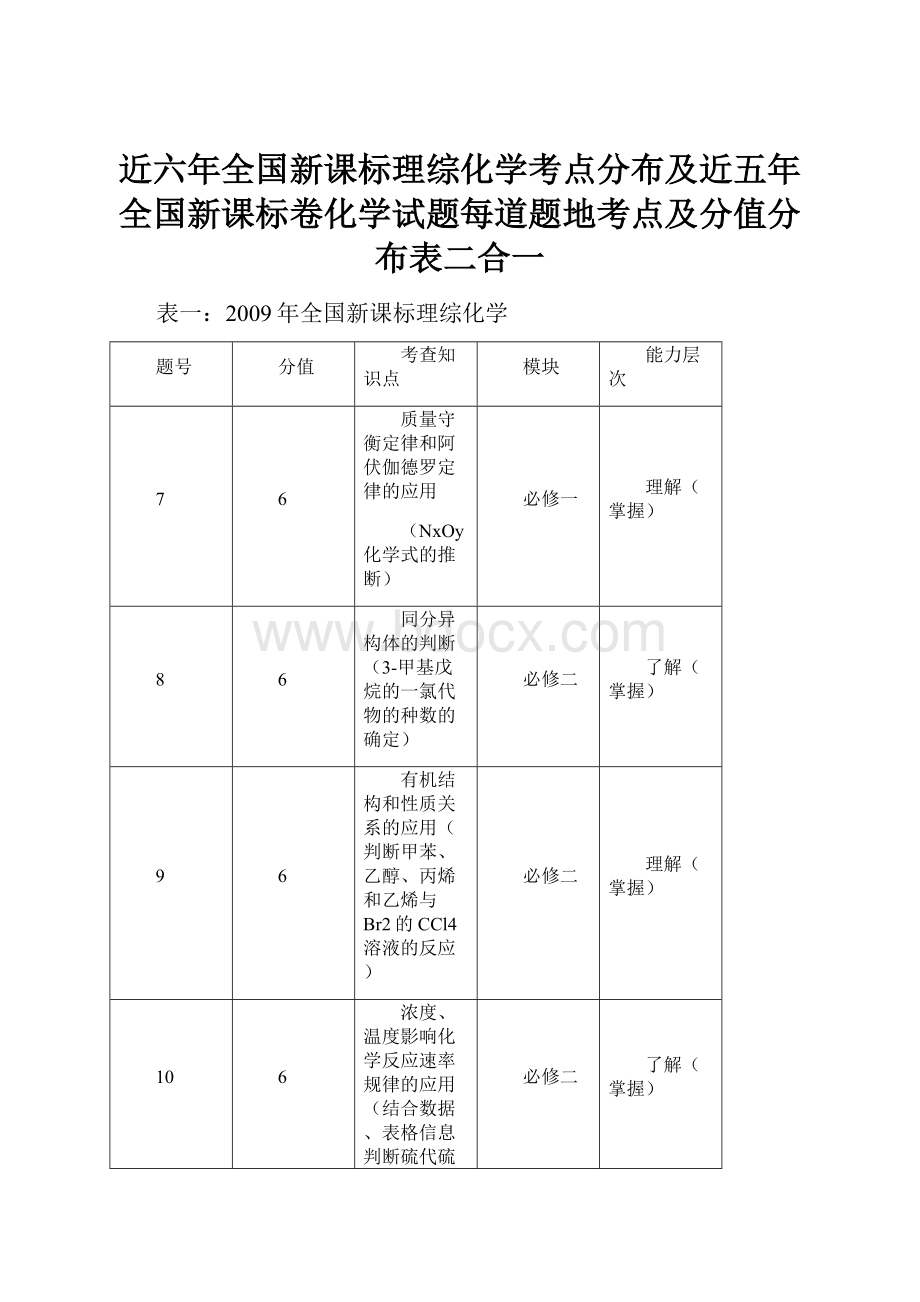
离子方程式的正误判断(次氯酸钙溶液中通过量CO2、SO2、氢氧化钙溶液与硫酸氢镁溶液、氯化亚铁溶液中加入稀硝酸)
13
化学平衡及其常数的计算(正、逆反应的K、三行数据法、反应物的最大分解率)
理解(掌握
26
14
实验方案设计与评价(测定碱式硫酸铜组成的方法、原理、装置仪器连接顺序、有关计算、评价与解释)
综合应用
27
15
无机框图推断综合题(钠、铝、铁、碳、氧及其化合物的性质)
28
化学反应能量变化及化学反应速率计算(结合图像判断说明各点含义,活化能与△H和催化剂关系、热化学方程式、氧化还原反应和系数比规律的应用)
37
氯碱工业(质量比计算、混合物的分离与提纯、电解和燃料电池的工艺流程、电极反应式、评价等)
38
电子排布式、轨道表达式、分子的空间构型、氧化还原反应方程式配平、元素周期律和元素周期表的应用、氢键和分子间作用力对物质沸点的应用
选修三
39
有机综合推断题(结合框图判断有关物质的结构简式、反应类型、官能团名称、书写同分异构体的结构简式和有机反应方程式)
选修五
辽宁、宁夏理综化学共100分,了解内容8分,理解内容30分,综合应用内容62分。
选修必考内容占26分,选修选考内容15分。
表二:
2010年全国新课标理综化学
核素、离子结构示意图、电子式、混合醇燃烧的有关计算
同分异构体的判断(C3H6Cl2的同分异构体确定)
有机结构和性质、反应类型(判断卤代烃的取代、消去,酯的生成与水解,甲苯的硝化与氧化的反应类型)
化学方程式的计算(用电子守恒计算BaCl2和KCl的混合溶液钾离子浓度)
盖斯定律的应用HCN(aq)、HCl(aq)与NaOH(aq)反应的焓变,计算HCN在水溶液中电离的H+焓变
离子方程式的正误判断(写出原电池的反应,找出氧化剂、还原剂的强弱,再判断离子方程式的正误)
离子方程式的正误判断(Fe3O4与稀硝酸、碳酸镁与稀盐酸、硫酸铵溶液与氢氧化钡溶液反应)
无机推断(铜、硫及其化合物转化关系,电解、平衡常数、转化率等计算)
SO2的制备及其性质实验设计
稀硫酸与锌制取氢气的实验中,影响反应速率因素的探究
水的净化与软化,水的硬度的计算
电子排布式、分子的空间构型、F2与水反应方程式、杂化、键角、晶格能、原子的激发及应用、原子结构与周期表
有机综合推断题(结合框图判断写出有关物质的名称、结构简式、判断同分异构体的种类及依据性质写结构简式和有机反应方程式)
2010新课标理综化学共100分,了解内容8分,理解内容30分,综合应用内容62分。
选修必考内容占24分,选修选考内容15分。
表三:
2011年全国新课标理综化学
NA、一定物质的量溶液的配制、电解、Vm
同分异构体的判断(C5H11Cl的同分异构体确定)
有机反应类型——取代(判断烯烃加成、醇的消去,酯的生成,苯的硝化的反应类型)
电解质溶液HF的稀释过程中离子浓度和Ka的变化
二次电池(电极的判断、电解质溶液及变化、电极反应书写)
离子方程式的正误判断(过量不足问题、氧化性强弱问题、强弱电解质问题)
元素周期律、周期表的相关推断
无机推断(由图形图表推结晶水的转化,铜和浓硫酸反应、Ksp、离子浓度等计算)
甲醇燃烧电池、热化学方程式、化学反应速率化学平衡常数
必修二选修四
氢化钙的制备及其性质实验设计
36
纸张的保护、水解规律的应用、氧化还原反应方程式的配平
选修二
电子排布式、分子的空间构型、反应方程式、杂化、键角、电负性
2011新课标理综化学共100分,了解内容8分,理解内容30分,综合应用内容62分。
选修必考内容占24分,选修选考内容15分
表四:
2012年全国新课标理综化学
知识领域
具体内容
基本实验知识与技能
液溴保存、CCl4萃取、淀粉KI试纸、Ag+检验(卤素性质)
基本素养
医用酒精浓度、单质硅的用途、天然高分子的判断、无机非金属材料
以NA视角,观察微观粒子的关系与行为
分子与原子的关系、质量与原子数量关系、体积与电子转移关系
有机物中碳成键的多样性
同分异构体,碳链异构、位置异构
水的电离平衡及影响
电离平衡,C(H+)与Kw关系、酸碱反应、离子浓度关系
构造数学模型
烯烃、烷烃、饱和二元醇通式规律
元素周期表、周期律与性质预测
元素推断、半径大小、共价键判断、沸点高低判断
定性、定量研究化学反应规律
利用计算确定化学式、铁的变价特征、离子方程式书写、电极方程式的书写、中和滴定、氧化还原反应
必修一必修二选修四
化学基本理论
化学反应原理综合:
燃烧热、结合信息书写化学方程式、盖斯定律、平衡图像、平衡计算、元素化合物、化学计算
实验的基本知识与技能
装置的功能判断、气体吸收与除杂、分离和干燥技能、仪器的选用。
有机化学实验、有机物制备、提纯、分离
必修一必修二
金属冶炼及提纯
焙烧反应原理与除渣、转炉反应、电解精制原理,氧化还原反应
结构对性质的影响及规律
原子结构、结构与酸性强弱的关系、晶体结构及内部数量关系
有机物合成与逆向合成法
结构式、反应类型、化学方程式书写、同分异构体书写
2012新课标理综化学共100分,了解内容8分,理解内容30分,综合应用内容62分。
必修一37分,必修二18分,选修必考内容占30分,选修选考内容15分.
表五:
2013年全国新课标理综化学
无机化合物
NaHCO3溶解度、HCl与NH3反应、补碘、黑火药
了解
有机化学
碳碳双键的性质、醇羟基的性质、结构式
周期表与离子水解
短周期元素判断、离子水解的判断
选修4
原电池
产物判断、正负极判断、总反应判断
Ksp
判断沉淀顺序
酯水解、碳链异构、位置异构
实验基本操作
萃取、分液、结晶、蒸馏
实验
仪器的识别与使用、实验基本方法、基本计算
氧化还原反应与元素化合物的性质
离子反应方程式书写、氧化还原反应、化合价判断
元素化合物、热化学反应、平衡移动与速率、原电池
铝土矿提纯、热化学方程式书写、条件与速率的关系、条件与平衡移动的关系判断、电极反应方程式书写、能量密度计算
草酸制取化学原理、工艺及操作、计算
反应原理、工艺分离操作、工艺流程、氧化还原反应计算
原子结构、晶体结构、结构与稳定性的关系、离子结构中的数量关系
命名、结构式、反应类型、化学方程式书写、同分异构体书写
表六:
2014年全国新课标理综化学
同分异构体(戊烷、戊醇、戊烯、乙酸乙酯)
必修二(渗透选修五)
化学与社会、生活;
热碱去油污,漂白粉变质,FeCl3制作电路板,草木灰与氯化铵施肥。
必修一选修四
化学反应速率,催化剂的概念、催化机理;
用化学方程式表示催化过程。
物质结构与元素周期律
沉淀溶解平衡,溶解度;
Ksp与溶解度曲线相结合
实验操作题:
酸碱滴定及滴定管得润洗,一定物质的量浓度的配制,仪器的烘干。
实验证明题:
溶解性比较,浓硫酸的脱水性、氧化性,SO2的制取及与钡盐的反应,硝酸、碳酸、硅酸的酸性比较。
有机物的制备:
仪器的识别,洗涤目的,萃取,除杂的方法,产率计算及误差分析。
蒸馏装置
氧化还原与电化学,弱电解质的电离平衡,盐类水解,方程式的书写技巧和电解池的原理运用。
化学反应原理综合题:
无机酸酯化反应;
分压平衡常数;
压强不变,物质比例对平衡的影响。
化学与技术
物质结构与性质:
杂化方式判断,晶胞体积的计算
有机化学:
信息的应用和同分异构体的书写
板块
化学科学特点和化学研究基本方法
12(14%)
化学基本概念和基本理论
36(42%)
常见无机物及其应用
10(12%)
常见有机物及其应用
化学实验基础
16(17%)
11年至15年全国新课标卷化学试题每道题的考点及分值分布表
2011年
2012年
2013年
2014年
2015年
NA题(离子晶体的组成、原子结构、浓度的有关计算、电解的有关计算)(6分)
化学实验(试剂保存(液溴)、物质的检验(KI、Ag离子、碘离子)(6分)
元素化合物(与氨、碘、氮有关的常识(候氏制碱法、氨管检验、碘、黑火药)(6分)
有机性质(油脂的性质:
生物柴油)(6分)
物质氧化性的判断,硝酸的氧化性
(6分)
有机结构(卤代烃的同分异构体C5H11Cl)(6分)
元素化合物(酒精、硅、天然高分子化合物、无机非金属材料的有关常识)(6分)
有机性质(碳碳双键及醇羟基的化学性质:
香叶醇)(6分)
有机性质(碳碳双键及苯的化学性质)(6分)
阿伏伽德罗常数与微粒数的关系判断
有机性质(取代反应类型的判断(四个反应)
NA题(混合气体原子数的计算、电子转移数)(6分)
元素周期律推断(影响水电离平衡的因素)(6分)
NA题(原子数、石墨结构、离子数目、所含电子数)(6分)
元素守恒法的应用,该有机物的分子式为C6H12N6,分子中的C与N原子的个数比即为甲醛与氨的物质的量之比为6:
4=3:
2(6分)
电解质溶液(弱电解质HF的电离平衡)(6分)
有机结构(醇的同分异构体:
C5H12O)(6分)
电化学原理(银器与铝)(6分)
离子方程式正误判断(铁与盐酸的反应、钠的化学性质、氯化铁的性质等)(6分)
对反应现象、结论的判断,稀硝酸与过量的Fe分反应,则生成硝酸亚铁和NO气体、水,无铁离子生成,所以加入KSCN溶液后,不变红色,现象错误等(6分)
电化学原理(爱迪生电池的充放电原理)(6分)
电解质溶液(中性的条件)(6分)
电解质溶液(氯离子、溴离子、铬酸根离子与银离子的沉淀溶解平衡)(6分)
电化学原理(“ZEBRA”蓄电池)(6分)
电化学原理对原电池反应的判断,微生物电池(6分)
离子方程式的判断(硝酸的性质、苯酚的性质、醋酸的酸性)(6分)
有机化学式的推断(依据表格找分子组成规律)(6分)
有机结构(酯的水解、酯化反应、同分异构体的数目:
C5H10O2)(6分)
盖斯定律(盖斯定律的有关计算)(6分)
元素周期表、周期律的应用,元素的判断及元素的性质(6分)
元素周期律推断(原子结构、分子类型)、铝的性质)(6分)
元素周期律推断(原子半径判断、原子结构、化学键类型、分子沸点)(6分)
化学实验(实验基本操作(萃取、分液、重结晶、蒸馏)
电解质溶液(溶度积及水的离子积、pH的相关计算)(6分)
电解质强弱的判断,溶液稀释的判断(6分)
无机综合计算(氧化还原反应原理在反应分析中的应用、溶解平衡原理、铜与浓硫酸的反应方程式、物质的量的有关计算、溶解平衡的有关计算)(14分)
无机综合计算(氧化还原反应原理在配平中的应用、原电池原理、铁与盐酸、氯气、氢碘酸、次氯酸钾的反应、物质的量的有关计算、物质的分数的计算)
(14分)
化学实验(醇的性质、仪器名称(直形冷凝管)、实验安全(防暴沸)、生成醚的反应、分液操作、提纯(除醇、水)、蒸馏操作(蒸馏所需要仪器)、产率的计算(环已烯产率)
(13分)
化学实验,实验安全(防暴沸、防飞溅)、分液操作、提纯、蒸馏操作(所需要仪器)、产率的计算率)(15分)
化学实验(草酸的性质、分解实验,溶液的pH,草酸的酸性比碳酸强、仪器名称、冰水浴的使用,实验安全(防倒吸)。
(15分)
化学反应原理拼凑(影响化学平衡的因素、平衡常数的有关判断、燃料电池原理、盖斯定律的有关计算、化学反应速率的计算、能量的计算)(14分)
化学反应原理拼凑(氧化还原反应原理在反应分析和配平中的应用、化学平衡原理、氯气的制备原理、盖斯定律的有关计算、平衡常数的计算、物质浓度及速率的计算)(15分)
工业流程推断(化合价标定(Co)、氧化还原反应原理(两个化学方程式)、原电池原理(锂离子电池)、铝与碱的反应、氯离子及双氧水的性质)(15分)
工业流程推断(氧化还原反应原理在产物分析及配平中的应用、铁、锰与硫酸的反应、过滤及沉淀洗涤检验方法、物质组成的有关计算)(14分)
以铁硼矿为原料制备硼酸(H3BO3)的工艺流程,氧化还原反应原理在产物分析及配平中的应用,元素及化合物的性质。
14分
化学实验(仪器的识别与连接、物质鉴别、实验安全及实验评价)(15分)
化学实验(苯与液溴的取代反应、基本实验操作(除杂、提纯等)(14分)
化学反应原理拼凑(影响化学平衡的因素、盖斯定律、燃料电池原理、铝及其化合物的性质(工业上铝土矿制备三氧化二铝)、盖斯定律的有关计算、能量密度的计算)(15分)
化学平衡(影响化学平衡的因素、化学平衡及平衡常数的有关计算)(14分)
AgCl的溶解平衡,盖斯定律的有关反应热的计算,影响化学反应速率,化学平衡的因素、平衡常数的有关判断(14分)
38有机
有机(甲苯的性质、卤代烃及醛的性质、酯化反应、反应类型、同分异构体的判断及书写、核碰共振氢谱)
有机(烯、醇、酚的性质、反应类型、同分异构体的判断及书写、核碰共振氢谱)
有机物的性质、反应类型、同分异构体的判断及书写
A(C2H2)是基本有机化工原料。
由A制备聚乙烯醇缩丁醛和顺式异戊二烯的合成路线,考查化学与生活,化学常识、涉及物理变化和化学变化的判断及相关物质的性质。